概論
fibrosis:変わりつつある概念,現在から未来へ
Current understanding and future perspectives in “fibrosis” research
菅波孝祥,柳田素子,武田憲彦
Takayoshi Suganami1)/Motoko Yanagita2)3)/Norihiko Takeda4):Department of Molecular Medicine and Metabolism,Research Institute of Environmental Medicine,Nagoya University1)/Department of Nephrology, Graduate School of Medicine, Kyoto University2)/Institute for Advanced Synthesis of Human Biology(ASHBi)3)/Division of Cardiology and Metabolism, Center for Molecular Medicine, Jichi Medical University4)(名古屋大学環境医学研究所分子代謝医学分野1)/京都大学大学院医学研究科腎臓内科学2)/京都大学構成的ヒト生物学研究拠点3)/自治医科大学分子病態治療研究センター循環病態・代謝学研究部4))
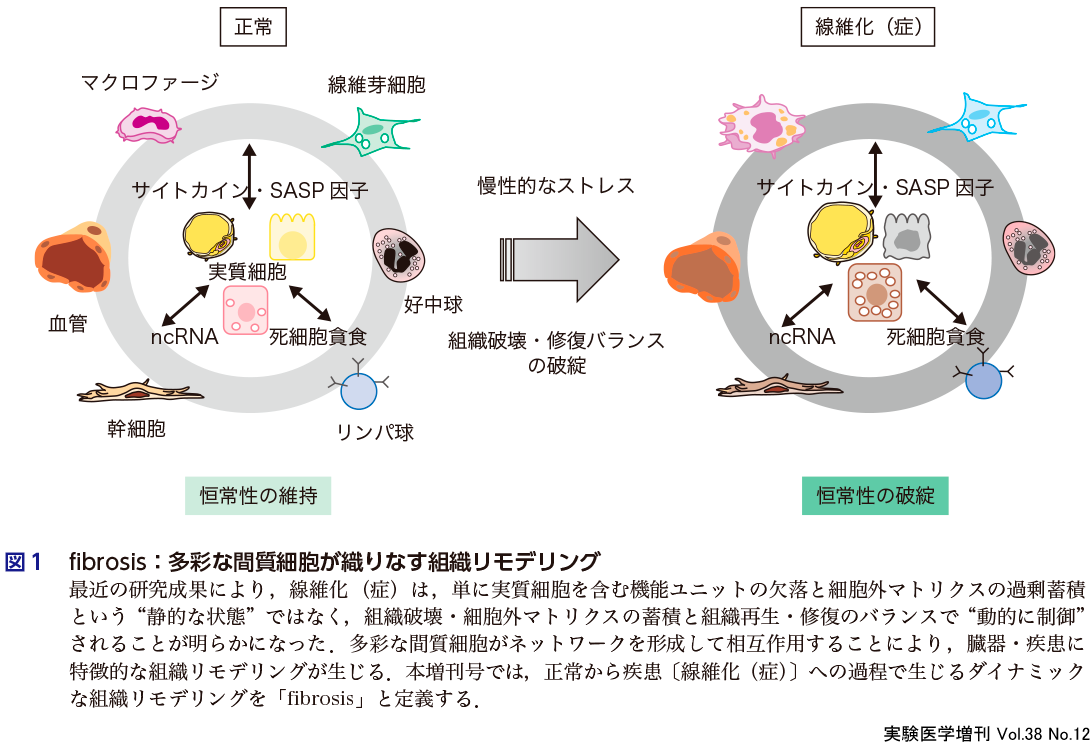
従来,線維化(症)は,慢性的な臓器障害のなれの果てで,不可逆的かつ予後不良の状態と考えられてきた.しかしながら近年,想定されていた“point of no return”を超えても一定の可塑性が残存する事例が次々に報告され,線維化(症)はアンメット・メディカル・ニーズのきわめて高い疾患として注目されるとともに,抗線維化薬の世界的な開発競争が生じている.そこで本書では,正常から疾患〔線維化(症)〕への過程で生じるダイナミックな組織リモデリングを「fibrosis」と定義し,ミクロ(線維芽細胞,細胞間ネットワーク)からマクロ(臓器・疾患)の視点で俯瞰することで,「fibrosis」研究の現状と今後の方向性をご紹介したい.
はじめに
肝線維化(肝硬変)—肝不全,腎線維化—腎不全,肺線維化—呼吸不全など,従来,臓器の線維化(症)は不可逆的な機能不全状態とほぼ同義に捉えられ,もはや治療による改善は見込めない状態と考えられてきた.実際,ある時点(point of no return)を超えると,たとえ原因が排除されても線維化や機能障害は進行することが臨床的に経験されてきた.しかしながら最近,病因や病理組織に基づく分類学的な議論から,治療戦略の開発に向けた議論へとパラダイムシフトが生じている.例えば,1型糖尿病に対して膵移植を実施すると,長期的には糸球体硬化病変が改善したり1),間葉系幹細胞移植療法により肝硬変の改善が認められるという2).このように,進行期においても可塑性が残存する事例が次々に報告され,従来の予防のみならず,線維化(症)に対する治療の可能性が注目されてきた.すなわち,線維化(症)は,単に実質細胞を含む機能ユニットの欠落と細胞外マトリクスの過剰蓄積という“静的な状態”ではなく,組織破壊・細胞外マトリクスの蓄積と組織再生・修復のバランスで“動的に制御”されると考えることができる(図1).一方,線維化のプロセス自体は,線維症として認識されるよりもずっと早い段階で始まっており,これをどのように可視化して捉えるかは喫緊の課題である.さらに,生体イメージングや細胞系譜追跡実験など解析技術の進歩により,線維化プロセスを担う細胞群や細胞間ネットワークも明らかになってきた.これらの細胞には,例えば腎臓におけるエリスロポエチン産生など3),きわめて重要な生理的役割を担うものがあり,正常から疾患への過程を俯瞰する視座が必要不可欠と言える.このような背景を踏まえて本書では,正常から線維化(症)に至るダイナミックな組織リモデリングを「fibrosis」と定義し,以下の4つの項目に注目して,「fibrosis」研究の現状と今後の方向性をご紹介したい.
[略語]
- CTGF
- :connective tissue growth factor
- EMT
- :epithelial mesenchymal transition(上皮間葉転換)
- NASH
- :nonalcoholic steatohepatitis(非アルコール性脂肪肝炎)
- SASP
- :senescence-associated secretory phenotype
- TGF-β
- :transforming growth factor-β
1.線維芽細胞の多様性
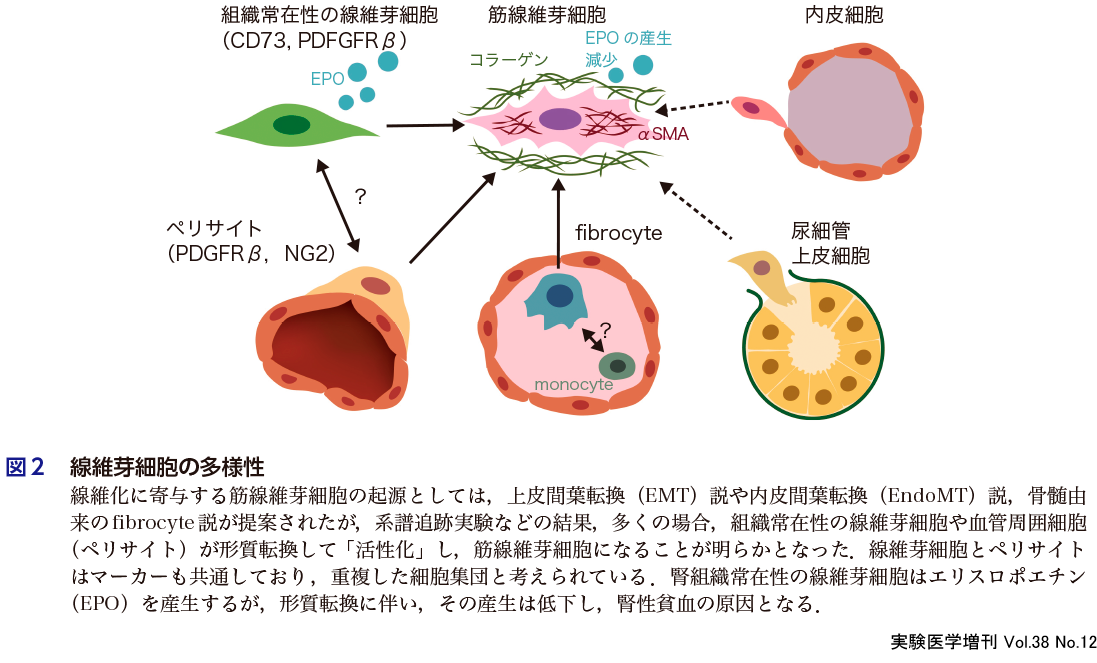
すべての臓器は,その臓器を特徴付けている実質細胞,血管や免疫細胞,線維芽細胞などの間質細胞,そして細胞外マトリクスから構成されている.従来,間質細胞はどの臓器においても一様と考えられてきたが,例えば,組織に常在するマクロファージには,肝臓のクッパー細胞,中枢神経系のミクログリア,肺の肺胞マクロファージなど,各臓器に特徴的なサブタイプが存在することが明らかになってきた.これに対して線維芽細胞は,細胞外マトリクスを活発に産生する筋線維芽細胞(myofibroblast)に注目が集まり,活性化プロセスや細胞外マトリクスの産生機序に関して積極的に研究が行われたが,その起源や生理的役割についてはあまり注意が払われてこなかった.実際,生理的な線維芽細胞は,血管や免疫細胞,幹細胞などを除外した残りの間質細胞と位置づけられ,特異的なマーカーに乏しい点が技術的な障壁であった.
近年,線維芽細胞や筋線維芽細胞は,従来想定されていたよりも多様であることが明らかになってきた(図2)4).発生起源の異なる筋線維芽細胞が線維化において独自のふるまいをするという仮説のもとに,上皮間葉転換(EMT)説や内皮間葉転換(EndoMT)説,骨髄由来のfibrocyte説が提案されたが,系譜追跡実験などの結果,多くの場合,組織常在性の線維芽細胞や血管周囲細胞(ペリサイト)が形質転換して「活性化」し,筋線維芽細胞になることが明らかとなった(第1章-1, 2, 6).一方,その活性化様式は一様ではない.例えば,肝臓で線維化を担う肝星細胞は,活性化誘導シグナルの違いによって,複数の活性化経路が存在するのみならず,活性化した星細胞を脱活性化させる手法も報告され,その可塑性が明らかになった(第1章-5).さらに,筋線維芽細胞が組織修復にもたらす影響も多様である.従来,線維化は「悪者」と考えられてきたが,近年,筋線維芽細胞が組織修復に寄与する「正の側面」が注目されている.例えば腎臓では,筋線維芽細胞が活性化の過程でレチノイン酸産生能を獲得して尿細管修復を促進し,筋線維芽細胞の多彩な機能が周囲環境に大きな影響を及ぼすことが示唆される(第1章-1)5).この二面性は「がん関連線維芽細胞」でも報告されており,がん細胞の増殖や浸潤能を促進する線維芽細胞が存在する一方,がんを抑制する線維芽細胞の存在が報告されている(第1章-4).さらに,組織常在性の線維芽細胞は三次リンパ組織形成にも寄与することが知られているが,その形質を獲得するメカニズムは明らかでない(第1章-3).
2.fibrosisを制御する細胞間ネットワーク
従来,線維化のマスターレギュレーターであるTGF-β(transforming growth factor-β)による筋線維芽細胞への分化など,単一細胞,単一サイトカインによる線維化機序が精力的に研究されてきたが,最近,多彩な細胞種,新たな伝達物質による複雑な細胞間ネットワークの存在が明らかになってきた.例えば,慢性炎症と線維化におけるマクロファージの重要性は広く認識されているが,線維化の制御に決定的な役割を果たす少数のマクロファージ集団が新たに同定された(第2章-3).また,細胞死は慢性炎症や線維化の起点となることが知られているが,最近,非アルコール性脂肪肝炎(NASH)や肥満(脂肪組織)において,死細胞を核としてマクロファージや筋線維芽細胞が集積し,線維化の駆動エンジンとして働くユニークな微小環境が同定された6)(第2章-2).一方,従来は主にマクロファージが担当すると考えられてきた死細胞の貪食・処理を線維芽細胞も担うことが明らかになり,線維化の新たな分子メカニズムとして注目されている(第2章-6).慢性炎症が持続するためには,細胞間のポジティブフィードバック機構の形成が必要であり,特に非免疫細胞を中心にIL(インターロイキン)-6を基軸とする分子メカニズム(IL-6アンプ)が提唱されている(第2章-5).線維化(症)は高齢者に多く認められるため,老化した細胞が産生する分泌因子〔SASP(senescence-associated secretory phenotype)因子〕の病態生理的意義が注目されている(第2章-4).また,高齢者でしばしば認められる三次リンパ組織は,臓器局所における免疫応答の制御に加えて,線維化の促進に働くことが明らかになってきた(第2章-1).さらに,新たな線維化メディエーターとして,non-coding RNAの役割も注目されている(第2章-7).
3.各臓器・疾患におけるfibrosis
従来から広く認識されている肝臓や腎臓,肺などの臓器に加えて,最近,脂肪組織や骨格筋,消化管などの線維化が明らかになり,新たな病態の理解が進んできた.また,各臓器における線維芽細胞の同定が進み,その生理的役割も明らかになりつつある.ここには,臓器間で共通の病態メカニズムや臓器特異的な分子機序が存在し,臓器横断的な理解が新たな治療法の開発を志向するうえで必要と考えられる.線維化(症)は,アンメット・メディカル・ニーズのきわめて高い疾患であり,世界的な抗線維化薬の開発競争が繰り広げられている.すでに,第Ⅱ相,第Ⅲ相の臨床試験が数多く実施されている一方,上市に至った例はきわめて少ない.本項では,各臓器・疾患における抗線維化薬の開発状況や今後解決すべき課題についても紹介する(図3).
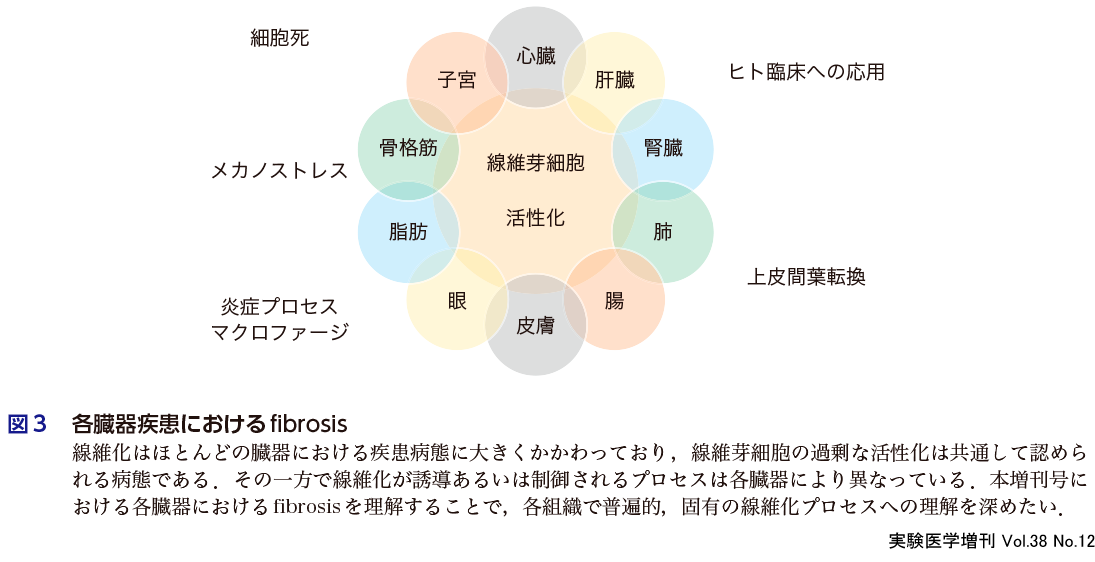
近年,各臓器における線維芽細胞の活性化機構が明らかになってきた.例えば,CTGF(connective tissue growth factor)による皮膚線維芽細胞の過剰な活性化は全身性強皮症(第3章-6),STAT3シグナルの活性化は子宮筋層での細胞外マトリクスを増加させ子宮腺筋症(第3章-10)の原因になる.また,骨格筋で活性化する線維芽細胞はPDGFRα陽性の間葉系前駆細胞に由来するが,α-SMAを発現しないという(第3章-9).IL-36を標的として,炎症性腸疾患や腸管線維化の病態を軽減する治療法の開発も精力的に行われている(第3章-5).一方,線維芽細胞の活性を調節する環境因子についても多くの知見が集積している.心臓では炎症惹起型のM1マクロファージ(第3章-1),肝臓では炎症抑制型のM2マクロファージが(第3章-2),それぞれ組織線維化の抑制に働く.腎臓では,虚血による尿細管上皮細胞の障害が炎症プロセスを活性化し,腎線維化を引き起こす(第3章-3).細胞死も,線維化の起点として注目されている.肺では,RBM7が細胞死を誘導し,ユニークなマクロファージ系細胞を動員して肺線維化を発症する(第3章-4).さらに網膜では,ペリサイト消失による網膜症モデルが樹立され,その病態機構解明が期待されている(第3章-7).このような組織の線維化は,その臓器だけにとどまらず,他臓器や個体全体の生理機構に悪影響を及ぼすことがある.例えば,脂肪組織の線維化は,肝臓の異所性脂肪蓄積を促進することで全身の糖代謝異常を惹起するという(第3章-8)7).このように,各臓器における線維芽細胞の活性化様式が明らかになり,病態解明や新規治療法開発への展開が期待されている.
4.fibrosisに対する次世代アプローチ
今後,線維芽細胞の生体恒常性維持における役割と線維化(症)の病態における意義を理解し,新たな治療戦略の創出につなげるためには,どのようなアプローチが必要であろうか? 最近,エラストグラフィーや原子間力顕微鏡(atomic force microscopy)など新技術の導入により,過剰に産生された細胞外マトリクスがもたらす“組織の硬さ”が注目され,がんの進展や肺機能などにおける意義が明らかになってきた(第4章-4).1細胞トランスクリプトーム解析は,近年の目覚ましい技術発展によって急速に普及し,fibrosis領域においても報告例が相次いでいる.すでに,遺伝子発現プロフィールを利用した線維芽細胞の同定や細胞間ネットワークの解明などに成果が上がっており,今後のさらなる技術の発展や1細胞トランスクリプトームを活かした研究手法の開発が期待されている(第4章-2).二光子励起イメージングなど生体イメージングの技術革新もめざましく,新たな細胞種や細胞間ネットワークを可視化し,病態を時空間的に理解する試みが進んでいる.将来的には,線維化(症)の非侵襲的診断につながることが期待される(第4章-1).一方,線維芽細胞は,組織幹細胞を維持する微小環境(ニッチ)の主要な細胞成分として,臓器の恒常性維持に働いている.最近,特異的なマーカーや機能に必須のサイトカイン,発生や維持に必須の転写因子などが次々と報告され,臓器特異的な役割が明らかになってきた(第4章-3).このように本項では,fibrosis領域における解析技術の進歩や新たな概念の導入を紹介し,今後の研究の方向性について議論したい.
おわりに
線維化(症)の重要性は広く認識されているが,実験医学誌において「線維化(症)」,あるいは「線維芽細胞」が真正面からとり上げられたのは,意外にも本増刊号が初めてという.その理由として,主に臓器・疾患別に研究されてきたこと,ヒトにおける解析手法が限定的であったこと,基礎研究の成果が臨床応用につながった事例が限られていたことなどがあげられる.最近,解析技術の飛躍的な進歩や臓器・疾患横断的な理解,ヒトに関するデータの蓄積などを踏まえて,抗線維化薬の開発も進んできたため,本増刊号はまさに時宜を得たものと考えられる.生物学・医学分野における国際的なシンポジウムのKeystone Symposiaでは,数年おきにfibrosisをトピックスとする集会を開催している.最近では2020年2月にカナダのビクトリアで行われ,世界中から500名を超える研究者が参加した.今回,最も目を引いたことは,1細胞トランスクリプトーム解析を用いた研究報告の多さで,新しい線維芽細胞の同定や細胞間ネットワークの理解が進み,fibrosisを動的に捉える試みも紹介されていた.この技術により,臓器・疾患横断的な比較が日常的に行われるとともに,限られたヒトサンプルが最大限活用化され,実験動物から得られた膨大なデータ・知識との対比が可能になった.誌面の都合により本増刊号ではとり上げることができなかったが,オルガノイドや生体機能チップなど新技術が次々に導入されており,異分野融合によるfibrosis領域の研究発展と臨床応用に今後も目が離せない.
文献
- Fioretto P, et al:N Engl J Med, 339:69-75, 1998
- Terai S & Tsuchiya A:J Gastroenterol, 52:129-140, 2017
- Yamazaki S, et al:Nat Commun, 4:1950, 2013
- Mack M & Yanagita M:Kidney Int, 87:297-307, 2015
- Nakamura J, et al:Kidney Int, 95:526-539, 2019
- Itoh M, et al:JCI Insight, 2:doi:10.1172/jci.insight.92902, 2017
- Tanaka M, et al:Nat Commun, 5:4982, 2014
参考文献
- 菅波孝祥,小川佳宏:炎症疾患としての肥満/メタボリックシンドローム.「実験医学増刊」(松島綱治/編),pp201-207,羊土社,2014
- 菅波孝祥,小川佳宏:肥満・メタボリックシンドローム.「実験医学増刊」(井村裕夫,稲垣暢也/編),pp58-64,羊土社,2015
- 菅波孝祥,他:メタボリックシンドロームと細胞死.「実験医学増刊」(田中正人,中野裕康/編),pp135-141,2016
- 菅波孝祥,他:メタボリックシンドロームとリポクオリティ.「実験医学増刊」(有田 誠/編),pp174-179,2018
- 菅波孝祥:脂肪の量と質を制御する.「実験医学」(菅波孝祥/企画),pp2698-2704,2018
著者プロフィール
菅波孝祥:1994年京都大学医学部卒業,同大学院医学研究科(中尾一和教授)を経て,2003年東京医科歯科大学難治疾患研究所助手(小川佳宏教授),’11年同准教授,’12年科学技術振興機構さきがけ研究者(兼任),’13年東京医科歯科大学大学院医歯学総合研究科特任教授,’15年より名古屋大学環境医学研究所分子代謝医学分野教授.研究テーマは,生活習慣病の成因と治療に関する分子医学的研究および医工連携による新しい生活習慣病治療戦略の開発.臨床応用を見据えた基礎医学研究に取り組む若手研究者を募集しています(http://www.riem.nagoya-u.ac.jp/4/mmm/index.html).
柳田素子:1994年京都大学医学部卒業,同大学院医学研究科(北 徹教授)を経て,2001年ERATO柳沢オーファン受容体プロジェクト研究員,’04年京都大学21世紀COE“病態解明をめざす基礎医学研究拠点”COE助教授,’07年京都大学医学研究科キャリアパス形成ユニット講師,’10年京都大学次世代研究者育成センター「白眉プロジェクト」特定准教授を経て,’11年より京都大学大学院医学研究科腎臓内科学教授.’18年よりWPIヒト生物学高等研究拠点の主任研究者兼任.研究テーマは,腎臓の障害と修復の制御メカニズムの解明.臨床の疑問に立脚した基礎医学研究に取り組む若手研究者を募集しています.(https://www.kidney-kyoto-u.jp)
武田憲彦:1996年東京大学医学部卒業.2005年東京大学大学院医学系研究科博士課程修了.’08年日本学術振興会海外特別研究員としてカリフォルニア大学サンディエゴ校へ留学.Randall Johnson教授のもとで酸素シグナルによる炎症制御機構の研究に従事.’11年より東京大学医学部附属病院循環器内科にて助教,特任講師として勤務.’11年JSTさきがけ研究員“慢性炎症”,’14年“生体恒常性”を兼任.’20年4月より自治医科大学分子病態治療研究センター教授.酸素生物学からのアプローチにより循環器疾患の診断・治療に貢献したいと考えています.