第2章 インスリンの基本と使い方
2.インスリン導入のABC(外来)
紅林昌吾
(くればやし内科 糖尿病・内分泌内科)
Point
- インスリン導入は患者交渉で始まる.事前から具体的に,簡便さをアピールする
- 持効型インスリン1回注射を用いた導入で,スムースにBOT(basal supported oral therapy)をはじめる
- 少量で開始,急がず空腹時血糖110 mg/dLを目標に増量調整する
- コントロール不十分であれば,GLP-1受容体作動薬を追加する.超速効型インスリン注射を追加してBOT plusへ治療をステップアップする方法もある
はじめに
血糖コントロール不良が続く場合や急激にコントロールが悪化した場合,また高血糖症状が出現している場合であっても,入院困難な患者は少なくない.働き盛りの世代,家事や介護で家を空けられない糖尿病患者からは,インスリン治療を開始するために入院を勧めても,「入院は無理です!」と返事される.このようなときは,外来でのインスリン導入を提案してみよう.
症例1:経口薬で血糖管理が得られない
66歳男性,BMI 20.1 kg/m2.2型糖尿病の内服治療歴は19年で,最近でシタグリプチン50 mg,グリメピリド2 mg,メトホルミン1,000 mgの併用療法で,HbA1c 9%台が続いている.仕事と家庭菜園の趣味で忙しく入院治療は拒否.「ごはんも美味しく体調良好」というが,HbA1c 9.9%,随時血糖362 mg/dLであった.
症例2:糖毒性を解除したい
39歳男性,口渇と体重減少を主訴に初診外来を受診した.年末よりスナック菓子や炭酸飲料の暴飲暴食あり,その3カ月後には口渇が出現し,気づくと体重は6 kg減少していた.身長168 cm,体重83.0 kg,BMI 29.4 kg/m2,HbA1c 12.5%,随時血糖値 509 mg/dL,尿ケトン体(3+).
1.外来で経験するインスリン導入の適応症例
インスリンの相対的適応となる場合は
著明な高血糖(空腹時血糖値250 mg/dL以上,随時血糖値350 mg/dL以上)
経口薬療法のみでは良好な血糖管理が得られない
やせ型の高血糖
ステロイド治療時の高血糖
糖毒性を積極的に解除する
とされている1).
相対的適応とはいうものの,症例1,2は今回はインスリン導入の方針とすべき2症例であり,よく糖尿病外来で導入する代表的なケースである.
それでは「今日からインスリン注射始めますよ」と患者に治療方針を話して,即座に受け入れてくれるだろうか.症例2はペットボトル症候群である.こちらは高血糖症状があり困って受診しているので,受診当日にインスリンを開始することはそれほど難しくない.
難しいのは症例1の方である.外来導入で一番よく経験するのが,この経口薬療法の二次無効のケースである.困る症状もないうえに,内服治療と注射治療のギャップが大きく,患者は「はいわかりました」と即答してくれない.
2.インスリン導入交渉:合併症の脅かしよりも具体的な注射療法の紹介
症例1のような場合に,経口薬が効いていない病状を説明,さらに「コントロールが良くなります」,「合併症のリスクを防ぎましょう」という説得は,もっともなことであるが,なかなか患者の心に届かない.
インスリン注射を始める患者の心理は,「怖い,面倒,痛い,操作が難しい,一生打つのは嫌だ」という負のイメージが大きいものである.患者にはインスリンのメリットを強調するよりも,これらの負のイメージにかかわる不安を払拭することに重点をおいて,説得交渉しよう.できるだけインスリン導入を決定する前から自己注射に関して話しておく.
●ここもポイント
インスリンを始めたら止められない,またインスリンは糖尿病治療の最終手段だと心配している患者もいる.嫌になったら止めてもよいことを一度話しておき,「注射を始める前に戻るだけ,止めても決して今よりも悪くなることはありません」,また「適切なタイミングで用いれば,後々の治療が簡単になる可能性もありますよ」というように,インスリンの離脱や先々で治療簡略化が図れる可能性があることを説明しておこう.
1 百聞は一見にしかず
注射針を見せたり,デバイスを手にとったりしながら説明してみよう.例えば31G針は外径0.25 mmで細い(vs.通常の静脈針22Gは外径0.7 mm)ので痛みはわずかであること,注射部位は腹部皮下であって静脈血管に刺す注射ではないことなど具体的に紹介する.また針刺しを実演してもよい.インスリンがペン型で操作簡単,使い捨てであることも,患者はこのときにはじめて知るものだ.
2 簡便さをアピール
症例1では経口糖尿病薬に基礎インスリンを追加する治療法であるBOT(basal supported oral therapy)への治療変更を想定して患者説明した.ポイントとして注射回数が1回,生活時間に合わせて好きな時間に注射,使用製剤は1種類,低血糖が発現しにくい持効型製剤の点を強調すればよい(表1).
このあたりで患者が「できそうだなぁ」と感想をもてれば,もう受け入れは間違いない.
3. 外来導入にふさわしいBOT(持効型1回注射)
1 シンプルにはじめやすいレシピが持効型インスリン1回注射
症例1のような場合でインスリン導入する方法は,① 持効型1回注射(BOT),② 混合型2回注射,③ 超速効型3回注射の3通りがある.いずれも1種類の製剤で開始できるが,3つのレシピを比較した4-T Studyの成績2, 3)や表1に示すように患者にも医師にも利点のあることを考慮すると,BOTを行う持効型が外来導入に最適なインスリンと考えられる.
2 さあBOTを開始しよう(表2)
1) 導入初日:持効型インスリンを4~5単位で始める
●処方例
初日:インスリングラルギン(インスリングラルギンBS注ミリオペン®「リリー」)4単位,夕食後
1週間後の再診:6単位に増量
低血糖にならないよう,まずは少量単位で開始する.注射時間は朝食前か,夕食前後や就寝前であれば,自宅で打てるので喜ばれる.
これまで併用していた内服薬は止めないことがポイントである.外来導入では,インスリン導入とともに膵β細胞を休ませようと思ってSU薬を中止すると,コントロールはさらに悪化してしまう.効きが悪いSU薬でも,止めてしまうとインスリン増量がまだまだ追いついていないのでコントロールが悪くなる.一方,入院導入ではSU薬を中心に内服薬を休止しても,短期間でインスリン治療を強化しているので,コントロールが悪くならないのである.インスリンの外来導入の際にSU薬を高用量で使用している場合には,持効型インスリンの増量を進めながら,低用量に減量(例えばグリメピリド2 mg/日以下に減量)する.
2) 導入1週間後
初回再診で,手技を確認,自己注射の不安なところをしっかり聞く.
3) 導入2~4週後
インスリンの増量は受診ごとに2単位ごとゆっくり増量する.朝空腹時血糖110 mg/dL以下を目標に増量する.
4) 血糖自己測定(self-monitoring of blood glucose:SMBG)の導入は急がない
注射導入開始期は自己注射に専念させ,自己測定の開始は負担分散化のため遅らせる.1カ月後くらいで十分だ.インスリン導入後の診察の際は,院内採血でなくSMBG器具を用いた指尖採血で血糖値を測る.これをくり返しているうちに便利そうだと患者が思えば,そのときがSMBGを勧める絶好の機会だ.
SMBGを使えば,インスリン注射を始めて血糖値が下がってきていることを実感でき,それが治療意欲とモチベーションの維持につながる.そして容易に朝の血糖値をモニターすることができるので,基礎インスリンの増量作業がしやすくなる.はじめは朝の血糖値の測定だけでもよい.自己管理ができる患者では,アルゴリズムに従いインスリン投与量を自己調節させることも可能である.
早朝空腹時血糖値の平均値(1週間測定)からの用量調節アルゴリズム4)
- ▶140 mg/dL以上 :+2単位
- ▶110~140 mg/dL未満 :+1単位
- ▶80~110 mg/dL未満 :変更なし
- ▶<80 mg/dL:2単位を減量(内服薬を併用している場合は,特にSU薬を減量)
また日中に低血糖が出現するようであれば,SU薬やDPP-4阻害薬を減量する
ただし高齢者や,腎機能不良者,合併症の併発,欠食など不規則な食生活の患者では,攻めすぎてはいけない.低血糖を回避するよう,実臨床では各症例の背景に応じた目標を設定することが大切である.例えば早朝空腹時血糖140 mg/dL程度に目標を修正することもある.
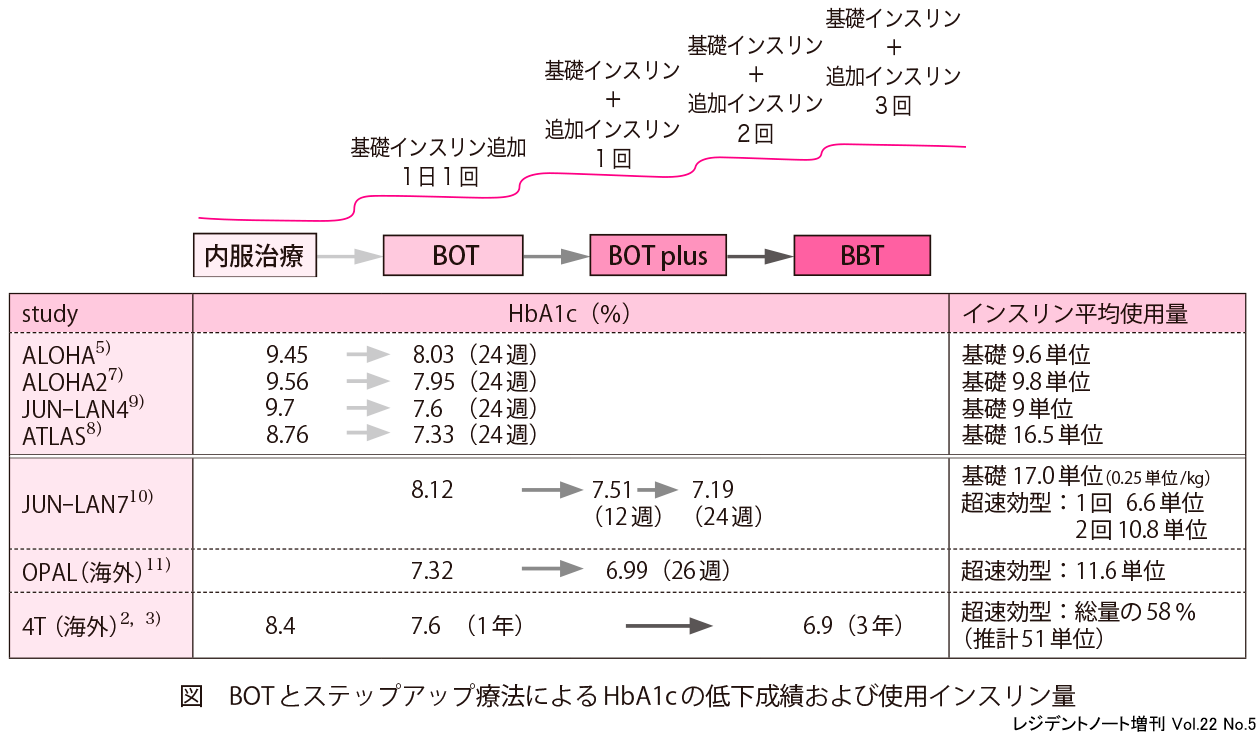
本邦でのBOTの実態を示した特定使用成績調査であるALOHA study 5)では,日常診療で行われた増量の成績が示されている.開始24週後のインスリングラルギン使用量は平均9.6単位(0.154単位/kg)であった.HbA1cの変化は平均-1.42%(開始前9.45%→24週8.03%)で,よく下がっていた.しかしHbA1c 7.0%未満の達成者は24.5%にすぎなかったのだ.どうすれば,もっと改善させることができるのであろうか.
ALOHA studyでの朝血糖値は最終評価時137.6 mg/dLであった.さらに持効型インスリンを増やす余地はあったように見える6).ALOHA 5)やALOHA2 7)が実臨床でのアプローチであるのに対して,アルゴリズムをもとに基礎インスリン量が調節されたATLAS study 8)では,空腹時血糖110 mg/dLを目標に調節すると,日本人では平均16.5±13.1単位(0.23単位/kg/日)の使用量であった.これは本邦で使用する目安となる単位数なのだろうが,SD値が大きく症例ごとのばらつきがありそうだ.
そして,もう1つこれらのBOT研究で考察された課題があった.コントロール目標未達成のケースでは,治療強化を図る対応が次に求められるということであった.
4. BOTでコントロール不十分の場合のステップアップ これが重要!
1 GLP-1受容体作動薬を追加しよう!
BOTで早朝空腹時血糖値が低下してきたにもかかわらず,HbA1cが目標に近づかない場合や,食後や眠前血糖値が高い場合に,GLP-1受容体作動薬の追加を行う.
以前は超速効型インスリンを追加して治療強化を進めていたが,GLP-1受容体作動薬の追加による治療効果のメリットは大きく,現在はこの選択が主流である.BOTの次の治療としてどちらが有用であるのか,2つの治療群成績を比較した報告では,血糖コントロールにおいてはほぼ同等の改善であり,体重増加や低血糖はGLP-1受容体作動薬の追加群で明らかにリスクが低かった12, 13).インスリン注射だけで治療ゴールを狙っていると,体重増加や低血糖に直面すること,また患者には注射回数が増えて嫌がられることもある.これらのインスリン療法のデメリットを軽減回避できるのがGLP-1受容体作動薬であり,基礎インスリンの良きパートナーとなる併用注射薬である.
BOT療法で基礎インスリンのタイトレーション途中であっても,上記のGLP-1作動薬の利点を活かしたいケースであれば,早めにGLP-1受容体作動薬を併用してもよい.最近では基礎インスリンとリラグルチドの配合注射剤(ゾルトファイ®)が臨床使用可能となり,注射導入時から両者を併用する外来導入例も経験するようになった.
2 超速効型インスリンの追加
GLP-1受容体作動薬が向かない場合は,超速効型インスリンの追加での治療強化となる.例えば消化器症状がある場合,食欲低下,やせのケース,GLP-1受容体作動薬の効果が乏しいケースである.
まず1日の食事のなかで食後血糖値が最も高そうな食前(main meal前)に超速効型インスリン3~4単位を追加する.持効型インスリン注射と同じタイミングで,かつ家で打てる点では,朝食前か夕食前の同時注射がよい.食後2時間血糖180 mg/dL以下を目指して,受診時に1~2単位増やす調整を進める.他の食事後血糖値が不十分であれば,もう1回超速効型インスリンを追加,最終的には3回追加してBBT(basal-bolus therapy)の強化療法へ移行する.
インスリン製剤だけの注射治療強化を行った成績を示す代表的な臨床研究では,BOTからBOT plusやBBTへ治療強化することで,HbA1cほぼ7%前後を達成できている(図中の表下段)2, 3, 10, 11).これは良好な治療成績であるが,GLP-1受容体作動薬を用いることができる場合よりも,体重増加や低血糖のリスクは高いことや,インスリンの1日使用量は多くなることから,注射調整が複雑であった診療の過程があったと思われる.
■ ステップアップの具体例(症例1)
1)導入3カ月後にGLP-1受容体作動薬を追加
- インスリングラルギン(インスリングラルギンBS注ミリオペン®「リリー」)16単位,夕食前
- デュラグルチド(トルリシティ®) 0.75 mg,週1回
2)導入3カ月後にBOTからBOT plusに変更
- インスリングラルギン(インスリングラルギンBS注ミリオペン「リリー」)16単位,夕食前
- インスリンアスパルト(ノボラピッド®注フレックスペンタッチ),夕食前6単位
米国糖尿病学会のコンセンサスが推奨する2型糖尿病における血糖治療の強化においては,インスリン製剤より先にGLP-1作動薬を導入する治療戦略が示されている14).これは両注射治療成績に歴然とした差が明らかであったからである.メタ解析の報告では,GLP-1受容体作動薬導入群でHbA1c低下の差は小さいながらも有意に大きく(-0.12%,p<0.0001),体重変化差は有意に大きく(-3.71 kg,p<0.0001),低血糖頻度は大幅に減っていた(-36.2%,p<0.0001)13).またアテローム動脈硬化性心血管疾患を有するケースでも,心血管ベネフィットのエビデンスが証明された理由で本薬を選択することは妥当であるといえよう.
一方インスリン製剤を考慮すべき場合として,以下の3点があげられている.
- HbA1cが非常に高値(>10%)や著しい高血糖(≧300 mg/dL)である
- 異化代謝亢進を示す体重減少や,高血糖症状(多尿,口渇)を認める
- 1型糖尿病の可能性がある
わが国でもGLP-1受容体作動薬が先であるというコンセンサスが得られるのだろうか.メタ解析13)の対象となった研究のなかに2つ日本人研究者の成績も含まれている.それぞれの対象患者の平均BMIは26.0 kg/m2 15)と26.1 kg/m2 16)であり,海外14報のBMI 30.4~34.2 kg/m2とは大きく異なっていた.しかしながらGLP-1受容体作動薬の臨床効果は,メタ解析全体の結果と同じく,基礎インスリンよりも優位であった.このことから日本人であっても,BMI 26 kg/m2前後であればGLP-1受容体作動薬の選択が優位といえよう.果たしてBMI 20~22 kg/m2以下の日本人ではどうなのであろうか.当面はやせやサルコペニア,高齢,消化器症状のある患者での使用は避けておきたい.
文献
- 「糖尿病治療ガイド2018-2019」(日本糖尿病学会/編・著),pp61-62,文光堂,2018
- Holman RR, et al:Addition of biphasic, prandial, or basal insulin to oral therapy in type 2 diabetes. N Engl J Med, 357:1716-1730, 2007
- Holman RR, et al:Three-year efficacy of complex insulin regimens in type 2 diabetes. N Engl J Med, 361:1736-1747, 2009
↑インスリン導入方法の文献と言えば2),3)の2つ! 本文中(p113)の3つの導入レシピによる成績を比較した臨床試験が4-T Studyである.3群に割り付けて治療1年の結果,HbA1c低下度は③超速効型3回注射≧②混合型2回注射>①持効型1回注射の順に良好で,低血糖と体重増加の頻度は③>②>①であった.そして1年後に血糖コントロール不良の場合はインスリン療法が強化され,①で開始した群では超速効型3回を追加,②の群では昼食前に超速効型を追加,③の群では基礎(持効型)を追加して,さらに2年間追跡された.その結果,3年後にHbA1c7.0%未満を達成した患者割合は,①および③開始群では②開始群に比べて有意に良好だった. - 「続・これなら簡単 今すぐできる外来インスリン導入」(弘世貴久/著),メディカルレビュー社,2009
- Odawara M, et al:Dosing of insulin glargine to achieve the treatment target in Japanese type 2 diabetes on a basal supported oral therapy regimen in real life:ALOHA study subanalysis. Diabetes Technol Ther, 14:635-643, 2012
- Kadowaki T, et al:Potential formula for the calculation of starting and incremental insulin glargine doses:ALOHA subanalysis. PLoS One, 7:e41358, 2012
- Kobayashi M, et al:Safety and efficacy of combination therapy with insulin Glargine and oral hypoglycaemic agents including DPP-4 inhibitors in Japanese T2DM patients:ALOHA 2 study, a post-marketing surveillance for Lantus®.Journal of Diabetes Mellitus, 4:273-289, 2014
- Garg SK, et al:Patient-led versus physician-led titration of insulin glargine in patients with uncontrolled type 2 diabetes:a randomized multinational ATLAS study. Endocr Pract, 21:143-157, 2015
- 後藤広昌,他:2型糖尿病のスルホニル尿素薬効果不十分例におけるインスリングラルギンの上乗せ効果―18カ月間の長期治療効果の検討―.糖尿病,50:591-597, 2007
↑本邦ではじめて示されたグラルギンを用いた前後比較試験. - 岡山かへで,他:2型糖尿病のSU薬とグラルギン併用療法効果不十分例における超速効型インスリンの段階的追加法の検討(JUN-LAN Study 7).糖尿病,52:197-202, 2009
↑BOTで8%以上の患者を対象に,超速効型インスリンを朝か夕に順次追加したBOT plusの本邦の成績. - Lankisch MR, et al:Introducing a simplified approach to insulin therapy in type 2 diabetes:a comparison of two single-dose regimens of insulin glulisine plus insulin glargine and oral antidiabetic drugs. Diabetes Obes Metab, 10:1178-1185, 2008
↑main meal(食後血糖値が最も高い食事)時に,BOTにグルリジン1回注射を追加することによるベネフィットがはじめて示された臨床試験. - Billings LK, et al:Efficacy and safety of IDegLira versus Basal-bolus insulin therapy in patients with type 2 diabetes uncontrolled on metformin and basal insulin;DUAL Ⅶ randomized clinical Trial. Diabetes Care, 41:1009-1016, 2018
↑基礎インスリンでコントロール不十分な2型糖尿病患者に対する次の治療として2つの治療成績を比較した.基礎インスリン+リラグルチド(配合剤)治療群と基礎インスリン+インスリンアスパル治療群で26週間の経過を比較すると,HbA1cの低下は-1.5% vs -1.5%,体重変化は-0.9 kg vs +2.6 kg,低血糖回数(患者1人・年あたり)は1.07 vs 8.17,インスリン総量は40単位(リラグルチド1.44 mg含)vs 84単位であった. - Abd El Azz MS, et al:A meta-analysis comparing clinical effects of short- or long-acting GLP-1 receptor agonists versus insulin treatment from head-to-head studies in type 2 diabetic patients. Diabetes Obes Metab, 19:216-227, 2017
↑BOTでコントロール不十分な2型糖尿病患者に対する次の治療追加としてGLP-1受容体作動薬 vs 超速効型インスリンの治療成績がメタ解析の一部で示されている.26~30週の観察期間で,GLP-1受容体作動薬群はHbA1cの低下幅に差を認めず(+0.02%),体重変化に有意差あり(-1.28 kg, p<0.0001),低血糖頻度は大幅に減っていた(-35.5%,p<0.0001). - American Diabetes Association:Pharmacologic Approaches to Glycemic Treatment:Standards of Medical Care in Diabetes-2020.Diabetes Care, 43:S98-S110, 2020
- Araki E, et al:Efficacy and safety of once-weekly dulaglutide in combination with sulphonylurea and/or biguanide compared with once‐daily insulin glargine in Japanese patients with type 2 diabetes:a randomized, open‐label, phase ⅡI, non-inferiority study. Diabetes Obes Metab.17:994-1002, 2015
- Inagaki N, et al:Efficacy and safety profile of exenatide once weekly compared with insulin once daily in Japanese patients with type 2 diabetes treated with oral antidiabetes drug(s):results from a 26-week, randomized, open-label, parallel-group, multicenter, noninferiority study. Clin Ther, 34:1892-1908 e1891, 2012
著者プロフィール
紅林昌吾(Shogo Kurebayashi)
くればやし内科 糖尿病・内分泌内科 院長
日本糖尿病学会専門医,日本内分泌学会専門医,総合内科専門医
昨年よりクリニックでの糖尿病診療をはじめています.病院外来で出会うよりも多彩な糖尿病患者さんに対応できるように,治療の引き出しをたくさんもっていなければならないと感じています.インスリンや注射治療の導入も然りで,選択肢が増えた今はあれこれ考えながら楽しく外来診療を行っています.