第1章 医学・生命科学におけるビッグデータ時代
1 医学・医療におけるビッグデータとは
医学・医療さらには創薬の分野において,近年,これまでの医学・医療の情報・データにはなかった新しいタイプの生命医療情報が,急速な勢いで産生され蓄積・波及しつつある.1つは,次世代シークエンサーの登場で,大容量・超高速に生成されるゲノム・オミックスなどの「網羅的分子情報」であり,もう一つはスマート革命と生体センサリング技術の融合によって生まれた「モバイルヘルス情報」である.これらは,その膨大な容量・際立った多様性,およびデータ生成・処理の高速性ゆえに,まことに医学・医療のビッグデータとよぶべき生命医療情報であり,これまでの医学や創薬のあり方を根底から変革する力をもっていて,それゆえ「ビッグデータ医療(big data medicine)」や「ビッグデータ創薬」という概念が生み出されつつある.本章では,これら新しい生命医療情報のビッグデータが従来の医学・医療情報とどこが根本的に違うのか,また,医学・医療・創薬の既存のパラダイムをどう変えようとしているのか,その基本的なコンセプトについて述べよう.
Keyword❖ゲノム・オミックス医療 ❖網羅的分子情報 ❖モバイルヘルス ❖ビッグデータ医療
1網羅的分子情報の急速な生成と集積
新しい医療ビッグデータの一番手は,いまさら言うまでもないが,ヒトのゲノムやオミックス※1情報をはじめとする網羅的分子情報の測定技術の急激な発展とその先端医療への応用の波及である.
1)網羅的分子情報の収集
2003年の国際的な「ヒトゲノム解読計画」の完成と相前後して,さまざまな網羅的分子情報の測定が可能になった.ゲノムのみならず,オミックス情報,すなわち,細胞内で発現している遺伝子の網羅的情報(遺伝子発現プロファイル)である「トランスクリプトーム」や,細胞内に存在するタンパク質の総体を示す「プロテオーム」,さらには,細胞内や組織に存在する代謝分子の全体である「メタボローム」などは代表的である.さらにさまざまな新しい種類の分子情報,例えば生体内でのタンパク質の相互作用の網羅的全体を示す「タンパク質インタラクトーム」,その他にも,多くの多様な網羅的分子情報が収集できるようになった1).
2)「シークエンス革命」――次世代シークエンサーの登場
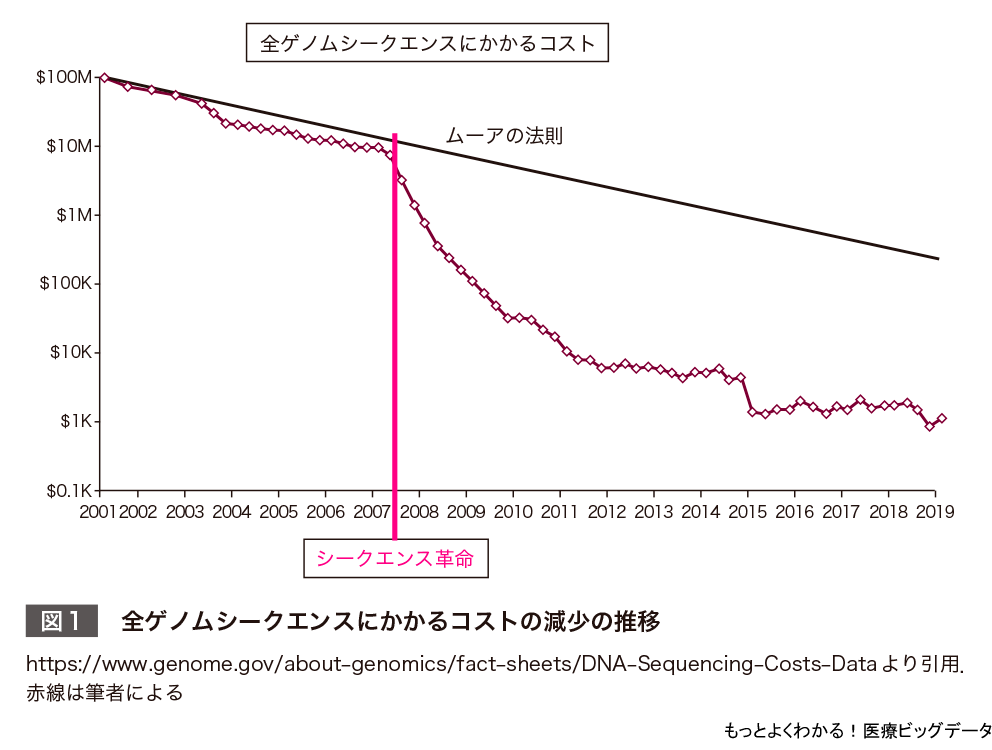
2003年に終了した「ヒトゲノム解読計画」では,ヒトゲノムの解読に13年の年月と3,500億円の費用がかかった.1人分のヒト全ゲノム配列の解読も,2007年の次世代シークエンサーの登場によるシークエンス革命によって,現在では精度確保のために30回くり返し読んでも,1日で約10万円程度の経費で配列解読できるようになった.この10年でデータ生成速度にして5,000分の1,費用にして300万分の1に減少した(図1).次世代シークエンサーはさらに,ゲノム(DNA)の配列解読だけでなく,ゲノムの発現情報である遺伝子発現プロファイル(mRNA)の配列解読など,ゲノム以外の網羅的分子情報の測定も可能になりつつある.
このようなゲノム配列解析の急速な高速化とコストの急激な低廉化によって,米国をはじめとして,全ゲノムシークエンシング(whole genome sequencing:WGS)や,遺伝子部分だけを配列解析する全エキソームシークエンシング(whole exome sequencing:WES)などの網羅的ゲノム解析が怒涛のごとく広がった.この流れは生命科学研究を根底から変革させただけでなく,その影響は臨床医学の分野にも及びつつある.
次世代シークエンサーは,米国では臨床医療の現場,すなわち病院においても急速に普及し,がんや稀少疾患などについて,疾患の網羅的分子機序を,臨床の現場で明らかにした.米国では,現在,ゲノム解析が病院で頻繁に実施され,多くの臨床的意義のあるゲノム変異情報が発見され集積されつつある.疾患原因遺伝子の診療の現場での同定による稀少疾患の発症機序解明,また,がんを駆動する主要な後天的体細胞変異(ドライバー変異)の同定による分子標的抗がん剤の適切な選択など,臨床実践が広く進められ,全米で大学病院を中心に数十という病院が,疾患に関するクリニカルシークエンスを実施して,治療医学の飛躍的向上に目覚ましい成果を上げている.クリニカルシークエンスは,米国では民間医療保険の償還の対象となっており,患者への負担は軽減されている.ゲノム情報解析の波及によって,臨床医学の実践は,根底から変革しつつある.その意味で米国では,ゲノム医療はもうすでに臨床実装されていると言えよう2).
3)欧州のゲノム・コホート型バイオバンクの急速な普及
一方,欧州は,米国に比べゲノム医学の臨床実装が進んではいないが,別のコンテキストで,すなわち,欧州の各地で推進されているバイオバンク事業において,参加者のゲノムを解析するゲノム・コホート計画が急速に広がっている.
バイオバンクは,疾患の発症や経過を長期追跡し,疾患の発症要因や進行機構を解明する大規模な疫学的調査事業であるが,ゲノム情報の大規模な収集は,疾患の遺伝的要因や分子的機序の解明を促進し,それに基づいて疾患の発症を防ぐ「個別的予防医学」のレベルの飛躍的な向上をもたらす.
このように欧州においても大量のゲノム配列情報の収集が,米国のゲノム医療の臨床実装とは別のコンテキストであるが,急速に実施され普及している3).国民的規模における予防医学に対するゲノム情報の活用は,高齢化に伴う慢性疾患などの増加に対して,発症過程の分子的理解に基づいて,発症を未然に防ぐ「予測的医学」や「先制医療(preemptive medicine)」などの「個別化予防」を飛躍的に発展させるものである.
4)ゲノム・オミックス情報の爆発的集積
このような大容量の網羅的分子情報の生成・蓄積速度の高速化の結果,米国NCBI(国立バイオテクノロジー情報センター)において,次世代シークエンサーのゲノム配列を蓄積しているデータベースであるSRA(Sequence Read Archive:ゲノム配列書庫)に格納されているゲノム登録量は,2017年初頭で9,000兆塩基を超え,1京塩基(1016)に達した.
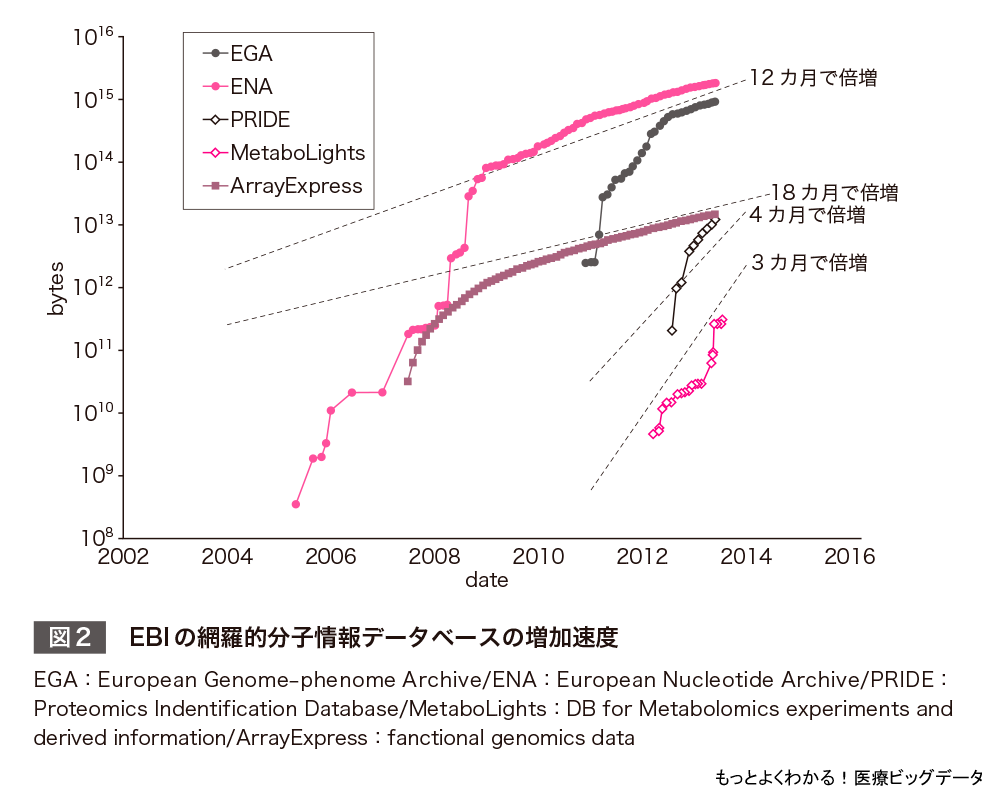
また,欧州においても,米国のNCBIに対応する機関であるヨーロッパ生命情報学研究所(European Bioinformatics Institute:EBI,英国ケンブリッジ近郊に所在)でも,SRAに対応するENA(European Nucleotide Archive,欧州核酸書庫)でのデータベースは,2017年3月の時点で4,200兆塩基を登録している.このENAデータは1年で倍増している(図2).
次世代シークエンサーによるゲノム配列の蓄積だけでなく,他の網羅的分子情報,すなわちDNAアレイによる遺伝子発現プロファイル(トランスクリプトーム)情報や質量分析器によるプロテオーム,メタボローム情報なども,図2にあるように急速に増加している.EBIの統計では,これらのオミックス情報のデータ蓄積量はゲノムより高速の増加速度を示し,その登録量はゲノムに迫る勢いである.
2モバイルヘルスによる医療ビッグデータ
1)モバイルヘルス革命の到来
もう一つの医学・医療の新しいタイプのビッグデータは,近年の「モバイルヘルス(mobile health:mHealth)」が生み出す医療ビッグデータである.モバイルヘルス革命とは,①近年のインターネットやスマートフォンなどのスマートメディアの急速な発展による「スマート革命」と,FacebookやTwitterなどのSNSの波及などによる,デジタル通信技術の革新的な展開,②有機伝導繊維などの開発による非拘束型生体モニタリング技術や「ウェアラブル生体センサー」の技術的発展,③米国をはじめとした,医療における「患者中心主義」,「患者参加主義」運動の拡大――という,デジタル技術・センサー技術・患者中心運動の3者の合体によって到来した,新しい医療の流れに伴って生み出されたビッグデータである.
2000年代のはじめ頃から,米国ではウェアラブルコンピューターと生体センシングを結合して自己の健康・行動をモニターする「Quantified Self運動」(自己定量化運動)がシリコンバレーのある米国西海岸からはじまった.
この運動は完全なボランティア運動で,メンバーは,例えば30~40年間にわたって自分の体脂肪率,血圧やコレステロール値などを記録し続け,生涯のいろいろな出来事が自分の体力や健康にどのように影響を与えたかなどを分析したりしていた.この運動はいまや全世界に広がっている.
このQuantified Selfの例だけでなく,近年米国では,医師や医療施設の医療職に自らの健康や疾患の治療選択を任せるのではなく,身体情報の自己測定や医学知識の収集に積極的にかかわることによって,「知識をもった患者(intelligent healthcare consumer)」として医療に参加する「患者中心主義(patient-centered)」の概念や「参加医学(participatory medicine)」の概念が全米に広まりつつある.
この概念や運動に,2010年からのスマートフォンによる「スマート革命」と,近年技術発展の著しい「生体センサー技術」,各種の「ウェアラブル装置」の発明が結びつき,健康や医療に関する多様な生体情報が,非拘束で継続的に測定できるようになった.装着した生体センサーの測定情報をBluetoothなどの近距離通信系を用いて携帯電話に伝送し,そこからインターネットを介してクラウド上に伝送することによって,健康医療情報などを連続的に蓄積し解析できるようになった.生体センサーもかつてのように脈拍や酸素飽和度などだけでなく,心電図や血糖値,体表からの生体ガスなど,さまざまな生体量の計測へ範囲を広げつつある.さらにICタグやRFIDなど,非接触ユビキタスICチップを環境に埋め込むことによって,環境との知的な相互作用や行動のモニタリングも可能になった.計測器に通信モジュールを装着し計測機器とデータのやりとりを行う方式は「物のインターネット;IoT(Internet of Things)」とよばれていて,近年のITの新しい流れである.医療分野ではIoHT(Internet of Healthcare Things)ともよばれている.
モバイルヘルスは,近年の高齢化に伴う慢性疾患の罹患の増加に対して,「生涯にわたる医療」の概念からも推進され,その発症を予防する方式としても期待されている.
2)モバイルヘルス革命がもたらす医療ビッグデータ
このような近年の発展が,モバイルヘルスによる医療ビッグデータを生み出している.モバイルヘルスにおいて,それぞれ生体センサリングされる生理変量は,それ自体は大容量情報ではないが,個人データとしては24時間連続した測定によって膨大な時系列データが生成されること,また,これら個々人の生体モニタリングデータは,近距離通信系やインターネットによって伝送されてクラウドに集積し,この蓄積された大多数の参加者データの集合に照らして,それぞれの個人の特性や疾患発症への可能性などが評価される.したがって,モバイルヘルスの情報はクラウド上で膨大な数の個人の,長時間にわたる連続データ集合として集積され,個人の健康状態の個別性は,その「ビッグデータ」と比較して解析される.
さらにモバイルヘルス情報は,単に体の生理的状態をモニターするだけでなく,生理的状態の情報に基づいて,治療を行う段階に達している.著者はこれを「情報による治療」とよんでいるが,最近では「デジタル治療法(digital therapeutics:DTx)」と世界的によばれている.メンタルヘルスや行動障害,あるいは生活習慣病の治療には,行動変容が目的となる.これには自己状態の認識が契機となる.例えばWellDoc社のBlueStarというシステムは,2型糖尿病の患者の血糖値・服薬状況・生活情報を基に,患者にスマートフォンでアドバイスし,行動支援・服薬支援・生活支援のメッセージをフィードバックする.薬剤治験を行うときと同様な厳密さで無作為比較試験(RCT)を行うことによって,患者の糖尿病の指標であるHbA1cにおいて,有意な改善がみられたため,2017年米国のFDAに薬事承認された.また米国Akili社のビデオゲームは,ADHD(注意欠陥多動性障害)の小児の治療のために開発されたビデオゲーム療法で,やはり無作為比較試験で有意な改善がみられたため,2017年にFDAに承認された.このようなデジタル治療アプリは,米国では現在100件を超え,多くがFDA承認を得ている.また,これまでのモバイルヘルスのアプリは健康管理支援が多かったが,近年では疾患管理・デジタル治療関係のアプリが著明に増加している.
この2番目の医療ビッグデータであるモバイルヘルス情報においては,将来ゲノム・オミックス情報も日常的に測れるようになれば,これらを含んだ情報となることによって,1番目の網羅的分子情報のビッグデータと統合される時期が来ると予測される.すでに現状でも血液中の浮遊DNA・RNAを日常的に測定する「リキッドバイオプシー(liquid biopsy)」が試みられている.これらが日常的な生体測定量として健康や疾病管理に使用される日は近い.
先端医療における網羅的分子情報のゲノム・オミックス医療も,生涯的なヘルスケアの視座のもとに行う日常的な生体情報収集によるモバイルヘルスも,将来的にはシームレスにつながり,日常的な「生涯にわたる」健康管理・疾患予防であるモバイルヘルスと,先進的な「網羅的分子情報に基づく医療」が,境なく融合するとき,IT技術と生命分子技術が統合したビッグデータ医療あるいはデジタル医療が将来の医学・医療・ヘルスケアのパラダイムとして到来する時代も近いと予測される.
3従来型の医療情報のビッグデータ
1)従来型の医療情報も含めた医療データの大規模化
医学分野以外で,ビッグデータという場合は,インターネットの発達,スマートメディアによる個人情報の大量蓄積,コンビニのPOS(point of sales:販売時点情報管理)データの集積など,デジタル革命に伴ったデータの大容量蓄積情報に基づいた社会状況の把握と,消費者の個々の行動の予測や対策を指すことが多い.その意味ではモバイルヘルスや参加医学によって生み出される医療ビッグデータは,他の分野のビッグデータと多くの点で共通する性質がある.むしろ医学生命科学に特徴的なのは,網羅的分子情報の爆発的な増大による医療ビッグデータが,医学・医療そのものの土台や枠組みを変えつつあるということである.
もちろんゲノム・オミックス情報の網羅的分子情報やモバイルヘルスの24時間連続個人生体モニタリング情報だけで,医療全体が実施できるわけではない.従来型の医療情報と統合されて,これら新しいタイプの医療ビッグデータがその価値を発揮するのである.
2)従来型の医療情報の大規模データベース
従来型の医療情報も,これまでの紙媒体での情報から電子化の進行によって大容量化し,これをビッグデータとよぶ場合もある.しかし,これらは,次章で展開するように真の意味での医療ビッグデータとは言い難い.本書では,網羅的分子情報やモバイルヘルス情報の新しいタイプの医療ビッグデータとは区別して扱う.新しいタイプの医療ビッグデータはその収集の目的から,データの構成形式の点や,また医学・医療を将来に向けて根底から変革する力をもっている点で,真の意味での革新的なビッグデータ医療を支えるものである.ただデータが大規模なだけで医療ビッグデータとよぶのは,医療ビッグデータのパラダイム変換的な意義を不分明にする怖れがある.
しかし,従来型の医療情報も電子化により大容量化が進んでおり,まだまだ電子カルテ情報の全国的な統合的データベース化は進んでいないものの診療報酬明細書である通称「レセプト」データの国家的データベースである「ナショナルデータベース(NDB)」には100億件近くのレセプトデータが収載されている.また,包括医療費支払い制度であるDPC/PDP(diagnosis procedure combination/per-diem payment)の集計表データ,処方の副作用情報を集めたMID-NETなど,レセプトデータベースよりも診療内容が詳しく記載されている従来型の医療情報ビッグデータも存在し,薬剤の市販後調査,治療法選択の地域別の特性など,さまざまな分析に利用できるよう政府・厚生労働省は推進している.
次世代シークエンサーをはじめとするゲノム・オミックス情報の急速な発展と蓄積に目を奪われ気味であるが,電子カルテから収集される従来型の医療情報も,臨床的表現情報として,ゲノム医療の推進にとって重要な役割がある.ゲノムなどの分子情報だけでは疾患の機序を明らかにできない.それがどのような臨床的な表現型をとって経過するか,網羅的分子機序と疾患としての表現型の両方の情報がなければ,疾患の機序を解明することはできない.したがって,従来型の医療情報のビッグデータも臨床表現型情報を収集するという意味では重要性が高い.
従来型の医療情報の大規模データは,これまでの薬剤治験の無作為比較試験のデータの限界性を乗り越えるリアルワールドデータ(real world data)として近年注目を集めている.これに関しては,後の第1章-3-2で詳しく述べるので参照されたい.
文献
- 「疾患システムバイオロジ―」(田中 博/編著), 培風館, 2012
- 田中 博:実験医学増刊, 34:709-716, 2016
- 田中 博:実験医学増刊, 35:3023-3036, 2017

