第2章 腸内細菌叢と疾患研究でわかっていること,いないこと
1 炎症性疾患・免疫関連疾患
 炎症性腸疾患(IBD)
炎症性腸疾患(IBD)
潰瘍性大腸炎(ulcerative colitis:UC)とクローン病(Crohn’s disease:CD)からなる炎症性腸疾患(inflammatory bowel disease:IBD)の原因は不明であり,慢性に経過し,寛解と再燃をくり返す難治性炎症性疾患です.残念なことに両疾患ともに右肩上がりで急増しています.2016年の指定難病登録者数は潰瘍性大腸炎167,872人,クローン病42,789人となっています.さらに,両疾患ともに20〜30歳代をピークに発生するために,長期に治療を必要とする点も大きな問題です.
最近では,抗TNFα抗体(レミケード®,ヒュミラ®,シンポニー®),抗IL-23抗体(ステラーラ®),抗α4β7抗体(エンタイビオ®)などのいわゆるバイオ製剤が臨床で使用できるようになり,良好な治療経過をたどる患者さんも増加してきていますが,治療効果には個人差もあり,不幸にして薬剤が有効でない方,副作用でつらい思いをされる方,手術をせざるをえなかった方も比較的多く,根本治療,治癒に迫る新規治療法を一刻も早く開発することが私たちに与えられた重要な課題です.
IBDと腸内細菌叢に関する研究はこの10年間で大きな進歩がみられています.例えば,炎症を抑制するサイトカインとして有名なインターロイキン10(IL-10)を欠損したマウスは,通常飼育中にUCに類似した腸炎を発症します.しかし,こうしたマウスの腸炎は腸内細菌がいない無菌環境下では発症しません.また,IBDの病変は腸内細菌叢が豊富に存在する回腸末端から大腸で好発します.これらのことは腸内細菌叢に対する免疫の異常がIBDの発症に重要な役割を担っていることを示す根拠となっています.
1)IBDのディスバイオーシス
IBDの腸内細菌叢の異常(ディスバイオーシス)についての解析も進んでいます.滋賀医科大学の安藤朗博士のチームは糞便の腸内細菌叢に関する先駆的な研究を続けています.2011年にT-RFLP法※1により寛解期のUCとCDの腸内細菌叢を健常者と比較した結果,UC寛解期では健常者と大きな差はみられませんが,CDにおいては寛解期であっても多様性が低下し,Clostridium属の低下がみられました1).その後,京都府立医科大学では内視鏡下で粘膜上皮表層の粘液層をブラシで採取し,いわゆる粘膜関連細菌叢(mucosa-associated microbiota:MAM)を16S rRNAシーケンスにより解析する手法を確立し2),糞便と比較してより上皮に近い粘液層の細菌叢が,宿主である粘膜細胞に影響を与えているのではないかと考え,研究を開始しました.
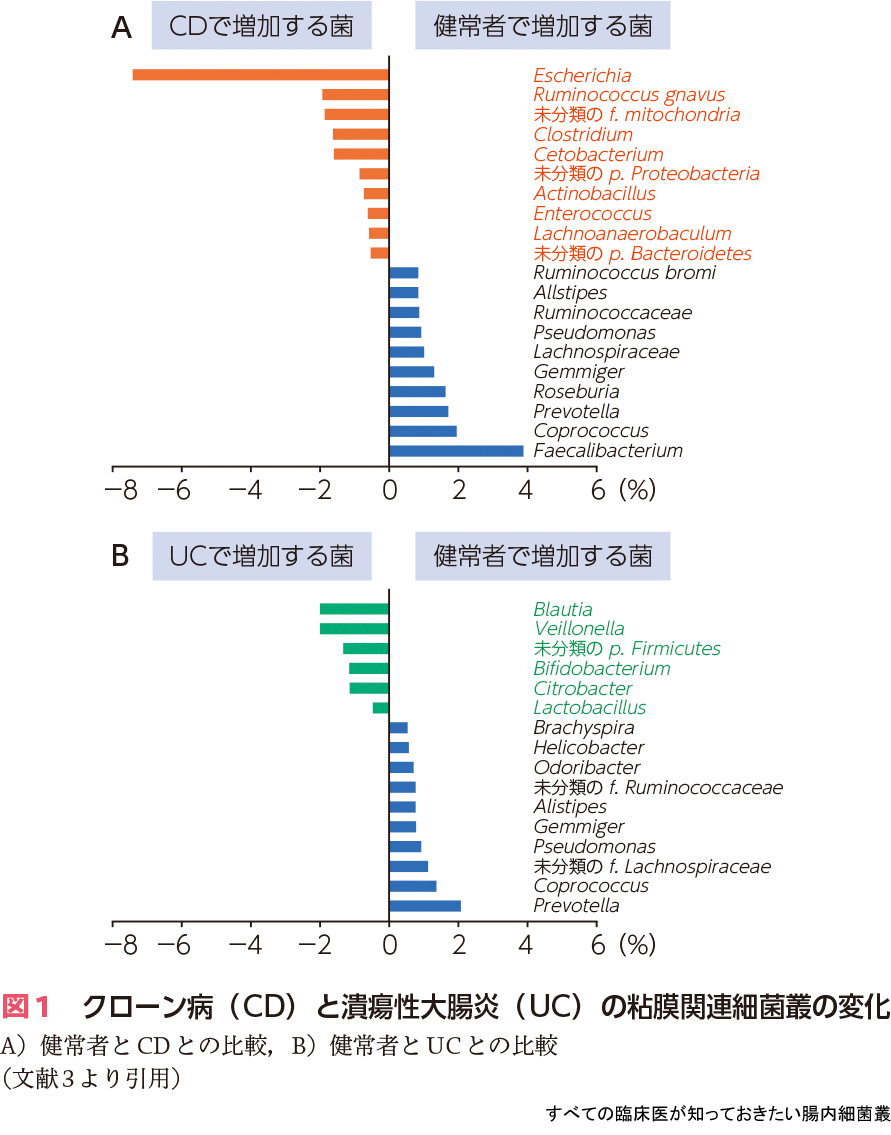
安藤博士らのチームとの共同研究を実施し,UCとCDにおけるMAMの解析をしたところ,健常者に比較してCDにおいては腸内細菌叢の多様性が低下しており,ファーミキューテス門,バクテロイデス門の細菌が減少し,プロテオバクテリア門の細菌が増加していることが明らかになりました(図1)3).特に,ファーミキューテス門の細菌のなかでもFaecalibacterium prausnitziiがCDのMAMで減少していることは他研究によっても検証されており,世界中で注目されています.
2)IBDと酪酸産生菌
Faecalibacterium prausnitziiは強力な抗炎症作用を有していて4),特にCDの病態との関連がさかんに研究されています.この細菌はヒト腸内細菌叢のなかでは比較的優勢な菌であり,重要な酪酸産生菌として知られ(p107,表2),CD患者の腸内細菌叢では酪酸産生菌が低下していることも確認されています5).酪酸は短鎖脂肪酸(SCFA)の一つであり,炎症を抑制する制御性T細胞を誘導することが知られています.つまり,CD患者における酪酸の低下は炎症の発症あるいは持続にかかわっている可能性があるわけです.すでに報告されているように,17種類のClostridia綱細菌のカクテルが酪酸産生を介して制御性T細胞の誘導に関与していることも明らかにされています.CD患者における酪酸産生菌の低下の理由については未解決ですが,病態のキーワードの一つが酪酸であることは明らかなようです.
最近,神戸大学の大澤朗博士は,神戸大学ヒト腸管モデル(Kobe University Human Intestinal Model:KUHIMM)という新規の人工腸管モデルを確立し,UCの患者さんの糞便を培養・解析した結果,Lachnospiraceaeが減少し,酪酸の産生が低下していることを見出しました6).さらに,Clostridium butyricum MIYAIRIを加えることで低下していた酪酸産生が回復することを証明することに成功しました.

興味深いことに,Faecalibacterium prausnitziiは多発性硬化症の糞便においても低下していることが見出されています.CDと多発性硬化症において類似の炎症を亢進させるシグナルが作用していることが推定され,Faecalibacterium prausnitziiの低下→制御性T細胞の減少→Th17リンパ球の活性化→組織障害といった系が消化管だけでなく,脳組織でもあることが明らかになりつつあります7,8).表1にも示していますが,本菌は糖尿病,神経変性疾患などさまざまな疾患の病態にかかわっています.
3)IBDは感染症?
UCやCDにおいて炎症を抑制する細菌叢が低下することが明らかになりましたが,逆に増加している細菌もいくつか報告されています.CDではRuminococcus gnavusの増加が注目されています.この菌は10年以上前にCDで増加することが報告されていましたが,最近の私たちのMAM解析でも健常者に比較して増加する菌の二番目に位置していました(図1).Ruminococcus gnavusは腸管粘液を攻撃する作用があり,粘液層の減少と関係し,さらには産生する多糖類が炎症応答を誘導することも報告されています9).今後の解析が待たれるところです.
しかしながら,最近報告されたエンテロタイプ4型分類(p24参照)では,CDにおける腸内細菌叢はB2型(Bacteroides 2型)が増加し,R型(Ruminoccoccaceae型)が減少することが特徴と報告されており,B2型の増加とカルプロテクチン量や便水分量が相関することなども明らかにされています10).
一方,UCの発症に関与する細菌がいるのではないかと研究が続けられています.UC患者から分離同定した細菌として,嫌気性菌のFusobacterium variumが注目され11),その菌に対する抗菌薬多剤併用療法の有効性が報告されています.順天堂大学大草敏史博士のチームは,このFusobacterium variumを除菌するために,アモキシシリン(A),テトラサイクリン(T),メトロニダゾール(M)を併用したATM療法を開発し,210人の難治性UC患者を対象にした二重盲検比較試験(プラセボとの比較)において,内視鏡的にも臨床的にも有意に改善することを報告しています12).現在,日本において多施設での有効性評価が行われています.胃潰瘍におけるピロリ菌の除菌療法のような劇的な効果はUCではみられないようですが,ATM療法の副作用は比較的少なく試みるだけの価値はあり,今後,ATM療法が有効な症例群の絞り込みを行うことが重要ではないかと考えます.
4)粘膜治癒と腸内環境
IBDの治療に対して多くのバイオ製剤が使用できるようになり,治療の目標も臨床的な寛解から粘膜治癒(mucosal healing:MH)が重要視される時代になりました.臨床的な寛解の指標よりも,粘膜治癒をしっかりと評価し,治療の強化や中止を判断していくストラテジーが患者さんのアウトカムの向上に役立つことが報告されています.特に,内視鏡による治癒の評価がより重要視され,京都府立医科大学においても画像強調内視鏡画像(linked colour imaging:LCI)を治癒判定に応用し,その有用性を報告しました13).現在,多施設共同試験,国際共同試験が実施されています.
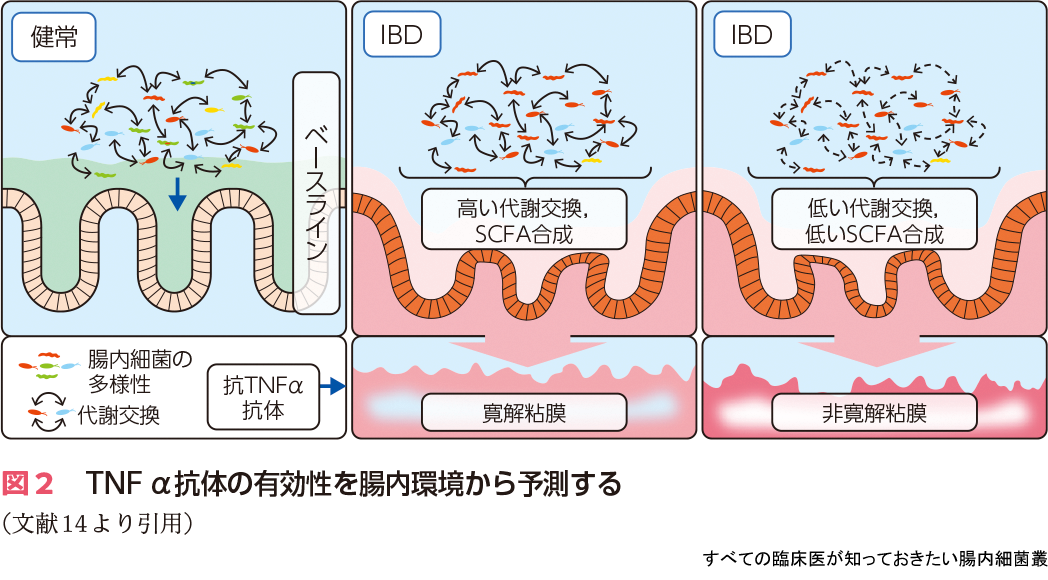
この粘膜治癒評価に腸内環境からのアプローチも報告されています.Adenらは,抗TNFα抗体で治療をしたUCとCDを対象に糞便の腸内細菌叢に対するメタゲノム解析,代謝物に対するメタボローム解析を実施し,内視鏡的な寛解粘膜では非寛解粘膜に比較して腸内細菌の発酵代謝産物のSCFAが有意に回復していることを明らかにしました14).特に,酪酸産生菌と酪酸が治療のアウトカムを予測するよい指標となる可能性が指摘されました(図2).
5)現状と今後に向けて
これまでの情報を整理すると,原因は不明ですが,IBDの患者さんの腸内細菌叢のなかでFaecalibacterium prausnitziiを代表とする酪酸産生菌の低下があり,寛解期でもその傾向が観察されました.酪酸を補充することが患者さんによい効果をもたらす可能性が高いわけですが,残念ながら食事に含まれる酪酸は大腸には到達できません.やはり大腸で酪酸を増加させる必要があると考えます.
日本ではずいぶん古くから医療の場で酪酸産生菌Clostridium butyricumをプロバイティクスとして使用してきました.ミヤBM®やビオスリー®がそうです(p256).実際に,Clostridium butyricumをIBDに使用した報告もありますが15,16),検討は十分ではなく,無作為化前向き比較試験は実施されていません.
文献
- Andoh A, et al:Comparison of the fecal microbiota profiles between ulcerative colitis and Crohn’s disease using terminal restriction fragment length polymorphism analysis. J Gastroenterol, 46:479-486, 2011
- Kashiwagi S, et al:Mucosa-Associated Microbiota in the Gastrointestinal Tract of Healthy Japanese Subjects. Digestion, 101:107-120, 2020
- Nishino K, et al:Analysis of endoscopic brush samples identified mucosa-associated dysbiosis in inflammatory bowel disease. J Gastroenterol, 53:95-106, 2018
- Sokol H, et al:Faecalibacterium prausnitzii is an anti-inflammatory commensal bacterium identified by gut microbiota analysis of Crohn disease patients. Proc Natl Acad Sci U S A, 105:16731-16736, 2008
- Takahashi K, et al:Reduced Abundance of Butyrate-Producing Bacteria Species in the Fecal Microbial Community in Crohn’s Disease. Digestion, 93:59-65, 2016
- Sasaki K, et al:Construction of a Model Culture System of Human Colonic Microbiota to Detect Decreased Lachnospiraceae Abundance and Butyrogenesis in the Feces of Ulcerative Colitis Patients. Biotechnol J, 14:e1800555, 2019
- Miyake S, et al:Dysbiosis in the Gut Microbiota of Patients with Multiple Sclerosis, with a Striking Depletion of Species Belonging to Clostridia XIVa and IV Clusters. PLoS One, 10:e0137429, 2015
- Leylabadlo HE, et al:The critical role of Faecalibacterium prausnitzii in human health: An overview. Microb Pathog, 149:104344, 2020
- Henke MT, et al:Ruminococcus gnavus, a member of the human gut microbiome associated with Crohn’s disease, produces an inflammatory polysaccharide. Proc Natl Acad Sci U S A, 116:12672-12677, 2019
- Vieira-Silva S, et al:Quantitative microbiome profiling disentangles inflammation- and bile duct obstruction-associated microbiota alterations across PSC/IBD diagnoses. Nat Microbiol, 4:1826-1831, 2019
- Ohkusa T, et al:Induction of experimental ulcerative colitis by Fusobacterium varium isolated from colonic mucosa of patients with ulcerative colitis. Gut, 52:79-83, 2003
- Ohkusa T, et al:Newly developed antibiotic combination therapy for ulcerative colitis: a double-blind placebo-controlled multicenter trial. Am J Gastroenterol, 105:1820-1829, 2010
- Uchiyama K, et al:Assessment of Endoscopic Mucosal Healing of Ulcerative Colitis Using Linked Colour Imaging, a Novel Endoscopic Enhancement System. J Crohns Colitis, 11:963-969, 2017
- Aden K, et al:Metabolic Functions of Gut Microbes Associate With Efficacy of Tumor Necrosis Factor Antagonists in Patients With Inflammatory Bowel Diseases. Gastroenterology, 157:1279-1292.e11, 2019
- Yoshimatsu Y, et al:Effectiveness of probiotic therapy for the prevention of relapse in patients with inactive ulcerative colitis. World J Gastroenterol, 21:5985-5994, 2015
- Yasueda A, et al:The effect of Clostridium butyricum MIYAIRI on the prevention of pouchitis and alteration of the microbiota profile in patients with ulcerative colitis. Surg Today, 46:939-949, 2016

