第1部 感染症の基礎
4章 病原体と宿主の攻防─生存戦略と感染戦略のせめぎ合い
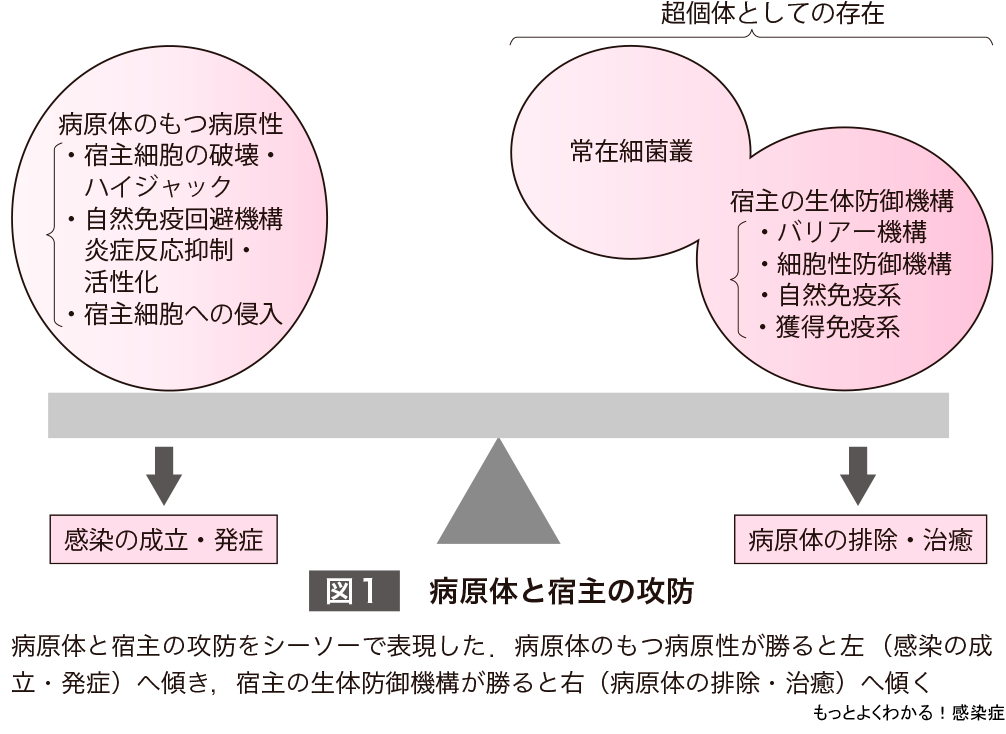
われわれ宿主側は,ウイルス,細菌,寄生虫などの病原体の侵襲に絶えず曝されている存在であり,これらの侵襲に対して自然免疫や獲得免疫を駆使することで,侵入してきた病原体の排除をおこなっている.排除に成功したある個体は,病原体の侵襲にさえ気づかずに治癒するであろう.その一方で,排除に失敗したある個体は,顕性感染を起こして命を落とすかもしれない.
第1部2章:感染症が起こるしくみで述べたように,ある個体が病原体に感染し発症するかどうかは,病原体がもつ病原性と宿主側免疫応答のバランス・オブ・パワー(勢力均衡)に大きく左右される(図1).
ただし病原体と宿主の関係は,もう少し複雑である.それは,皮膚や腸管の上皮細胞に終生定着している細菌(常在細菌)が,免疫応答に少なからず影響をおよぼしているからである.
第2部:わが国で危惧される感染症に入る前に,病原体と宿主の攻防について,まとめてみたい.
1宿主のバリアー機構 ─非選択的な病原体の排除システム
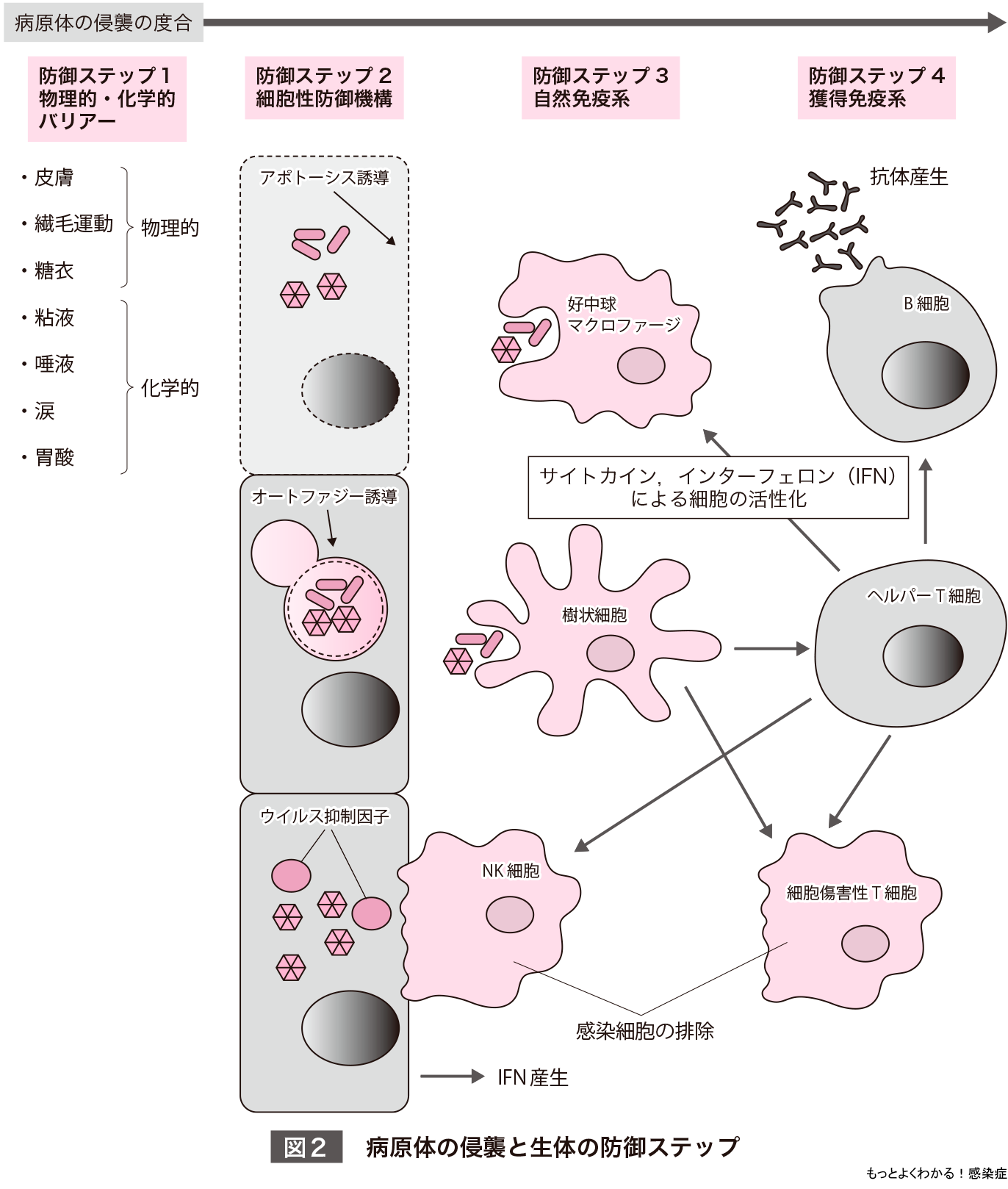
われわれの体表面を被っている皮膚は,強固な物理的バリアーとして機能している(図2防御ステップ1).また,口腔や鼻腔より侵入した病原体は,気道上皮の繊毛運動で行く手を阻まれ,さらにそれを乗り越えたとしても,強力な胃酸に曝される運命にある.また,粘液,唾液,涙のなかにはディフェンシンとよばれる抗菌ペプチド※1が含まれ,胃酸と同様に化学的バリアーとして機能している.一方,多くの微生物がひしめきあう腸管上皮細胞は,糖衣(glycocalyx)とよばれるムチン様の糖タンパク質で被われ,病原体との直接的な付着を回避している(物理的バリアー).
このように,生体がもつ種々の物理的・化学的バリアーは,病原体の侵入初期において非選択的な防御機構として機能している.
2免疫システム ─宿主による病原体の認識と応答
1)細胞性防御機構
一方,病原性が強い病原体は,このような物理的・化学的バリアーを克服し生体内の深部へ侵襲する能力をもつ.この能力に対抗するため,宿主は細胞内に侵入してきたウイルスや細菌に対し,アポトーシスやオートファジーを誘導することで,感染細胞の拡散を防いでいる.また,細胞のなかで発現しているウイルス抑制因子は,侵入してきたウイルスの増殖を阻害することが,最近の研究で明らかとなってきた(第2部6章).(図2防御ステップ2).
われわれの身体を構成する細胞のすべては,病原体に対するセンサーを有している.このセンサーによって体内に入ってきた異物を認識し自然免疫の誘導をすばやく惹起する.食細胞※2だけではなく,すべての細胞がもつ病原体センサーとはどのようなものなのか,もう少し詳しく解説したい.
2)自然免疫系と獲得免疫系
感染初期の病原体排除に働くのは,自然免疫系である(図2防御ステップ3).自然免疫系では,細菌やウイルスなどの病原体が共通して発現しているタンパク質,糖・脂質,核酸などを,病原体関連分子パターン(pathogen-associated molecular patterns:PAMPs)として認識している.これら病原体に共通した分子パターンを認識する受容体が,パターン認識受容体(pattern recognition receptors:PRRs)であり,その代表的なものとして,Toll様受容体(Toll-like receptors:TLRs)があげられる.TLRはすべての細胞膜上に発現しており,病原体のセンサーとして働いている.
TLRにPAMPsが結合すると,細胞内のシグナル伝達経路が活性化され,炎症性サイトカインやインターフェロン(IFN)の産生が誘導される.これにより,好中球やマクロファージが感染局所に浸潤し病原体は速やかに排除される(自然免疫系の初動).さらに,処理された病原体断片(抗原)は,樹状細胞を介してT細胞へ提示され,最終的にB細胞による抗体産生がおこなわれる.特異的な抗体がつくり出されるまでに2週間ほどかかるので,獲得免疫系とよばれている(図2防御ステップ4).獲得免疫系では感染を記憶しており,同じ病原体(抗原)に侵襲された場合は,素早く強力な免疫応答が可能である.さらに,ウイルスの感染細胞を排除するシステムについても,自然免疫系と獲得免疫系の両者が存在している.前者はNK(natural killer)細胞が担当しており,感染細胞をみつけ次第,排除する.一方,後者は細胞傷害性T細胞が担当しており,感染細胞を抗原特異的に探し出し排除している.これら一連の免疫応答については,河本 宏先生が執筆されている本書と同じシリーズの「もっとよくわかる!免疫学」で,その詳細をみることができる.オススメの参考書である.
3「超個体」 ─ヒト細胞と常在細菌の相互作用システム
1)超個体の概念
われわれの身体を構成する細胞数は,約37兆個である.一方,体内に常在している細菌の数は,100兆個を軽く超えるといわれている.このように,われわれの身体のなかにある半分以上の細胞は,われわれのものではない.また,遺伝子総量においてもヒト細胞のゲノムは,優位な存在ではない.数の論理でいえば,われわれが細菌叢に間借りしている状態なのである.
さらに,免疫応答の成熟や感染に対する防御力は,常在細菌との相互作用によって成り立っており,切り離すことができない関係にある.これらのことから,われわれはヒト細胞と常在細菌との相互作用のなかで1つのシステム「超個体(superorganism)」として存在している,という考え方が徐々に浸透しつつある.なお,超個体という言葉は,元来,ハチやアリ(分類学上はハチに含まれる)などの社会性をもつ昆虫の集合体を表す用語として,使われてきたものである.
2)超個体としての免疫応答
皮膚や腸管に常在している細菌叢は,その圧倒的な数により,外来の病原体の定着を阻むだけではなく,腸管免疫の活性化にも直接関与している.ここで筆者の話を少しだけしてみたい.筆者は,ウサギに下痢を起こす腸管病原性大腸菌の研究をおこなっていた時期があった.ある種のウサギは,この大腸菌の感染をまったく寄せ付けずに,実験結果に大きなブレをもたらした.しかしよく観察してみると,病原菌に耐性を示したウサギの腸管上皮には,きまってセグメント細菌(segmented filamentous bacteria)が存在していたのである.詳しいメカニズムはわからなかったが,セグメント細菌は病原菌から宿主を守る,という論文を2000年に発表した(巻末の文献1). 今では,このセグメント細菌が腸管のTh17細胞※3数を増加させることで,宿主の感染防御力を増強することが明らかになっている.プロバイオティクス※4の観点からも,この細菌は大いに注目されている.このように,腸管免疫の世界では,超個体としての免疫応答の研究が精力的に繰り広げられているのである.
4病原体の感染戦略 ─宿主細胞をハイジャックするものもいる
感染の成立過程において,病原体と宿主のバランスが大きく影響することを述べてきたが,BSL3やBSL4などに分類される圧倒的に病原性が強い微生物の存在も忘れてはならない.病原性の強い細菌のなかには,積極的に宿主側因子の機能をハイジャックするものが存在する.例えば,赤痢菌(第2部8章参照)やリステリア属細菌は,Arp2/3複合体(アクチン重合に関与する宿主側因子)を菌体一極に集め,アクチン重合を推進力として,感染細胞内で運動している.一方,ヒト免疫不全ウイルス(HIV)(第2部6章参照)は,ヘルパーT細胞やマクロファージに感染することで,免疫抑制を誘導し最終的にAIDSを発症させる.
これから登場する病原体の多くは,巧妙な感染戦略をとっているものが多い.第2部:わが国で危惧される感染症では,わが国で問題となっている感染症が,病原体のどのような病原性発揮により起きているのか,詳しく解説している.本書が感染症研究者の,ひいてはわが国の感染制御の一助となれば,幸いである.
文献
- 『銃・病原菌・鉄 上下』(ジャレド・ダイアモンド/著, 倉骨 彰/訳),草思社,2012

