概論
“サイズ”で斬る生物学への誘い〜
A prelude to “size” biology
山本一男
Kazuo Yamamoto:Division of Cell Function Research Support, Biomedical Research Support Center, Nagasaki University School of Medicine(長崎大学医学部共同利用研究センター細胞機能解析支援部門)
「大きさ」はすべての物体が有する根源的な特性である.それは生命体においても例外ではなく,われわれが肉眼で確認できる表面的な意味のみならず,個体の内部に分け入った器官や組織,それを構成する細胞,さらにそれらを支える細胞内構造に至るまで「適正なサイズ」が設定されていることが見てとれる.ではこれら多様なスケールにおいてそれぞれのサイズを規定しているものは何であろうか.近年の技術革新により,どちらかといえば古典的なこの疑問に,実験と理論の両方から迫る研究が世界的に増えてきている.例えば,がんに代表される疾患は,サイズ制御の破綻と関連させて理解できるかもしれない.今回,本邦にて独自のアプローチで「大きさ」の問題を視野に入れながら研究を展開されている7名の執筆陣を迎え,「サイズ生物学」というくくりでこの潮流を感じてもらえるよう特集を組んでみた.
はじめに
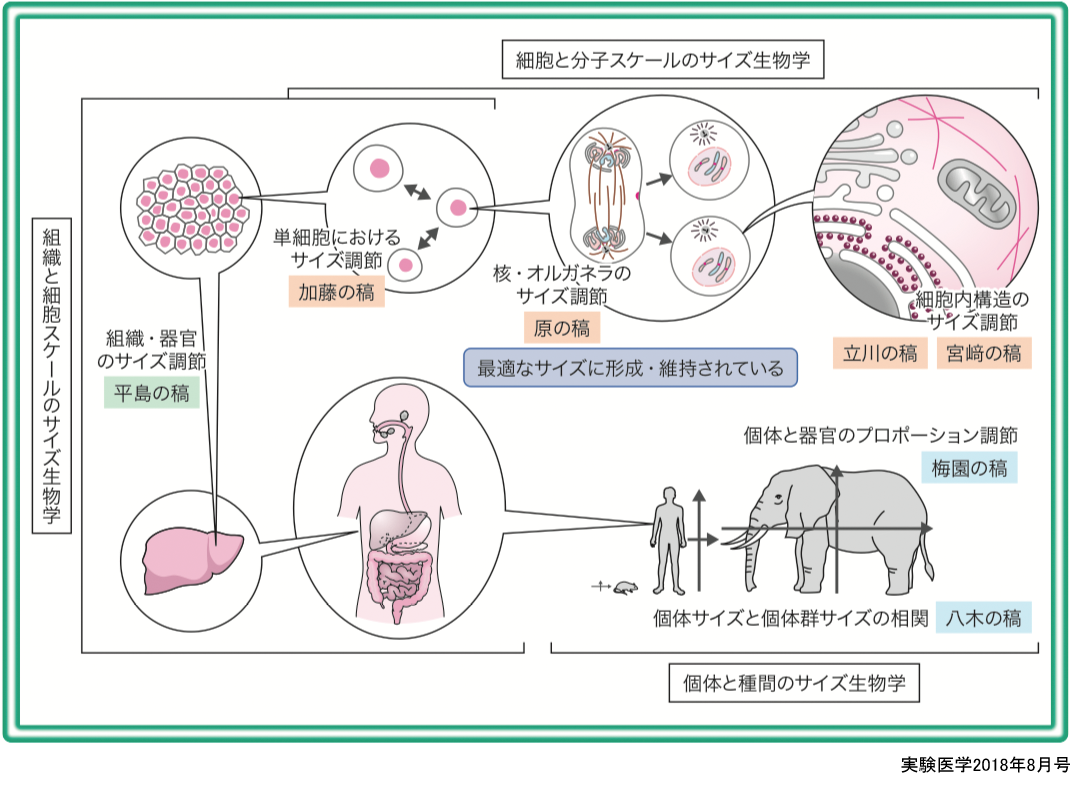
人が生まれてからはじめて認識する物理量は何であろうか? 「熱い・冷たい」「明るい・暗い」といった体感ではなく意識のレベルで認知するもの,という制約をつけるとその答えはおそらく「大きさ」に落ち着くのではないだろうか.「大きい!」その言葉自体は知らなくとも,何か途方もないものを目にして驚く感慨を胸に刻むことが人間としての原体験としてあるのではないかと私は思う.実際,われわれが目にするものはすべて固有の形と大きさをもっている.そもそも「物体」の定義が「形と大きさを有して存在するもの」であるからこれは当然とも言えよう.しかしそれは,生命体というまだわれわれが定義しきれないものについても正しく当てはめることができる.すなわち,われわれが普段目にするさまざまな「個体」のレベルだけでなく,その内部に配置された器官や組織,それら一つひとつを構成する細胞群,さらにその細胞を支える内部構造体から生体高分子に至るまで,世界は「適正なサイズ」に収められているように見える(概念図).「そう進化してきたものが生物なのだから,これは当然の結果である」という意見もあるかもしれない.しかしいかにしてその大きさに至りそれを維持しているのか,そのメカニズムを探ることは,また新たな生命の構築原理を知ることにつながるのではないだろうか.このような考えから,生物にかかわるさまざまなスケールの問題に「大きさ」の観点からメスを入れる研究の指向を「サイズ生物学」とよんでみたいと思う.
組織と細胞スケールのサイズ生物学
科学の実践は「見る」ことからはじまる.古の科学者も生命なるものを理解するにあたりその内部を見ることが糸口となると考え,顕微鏡の発明に至った.そこで最初に確認されたものが「細胞」というユニットである.その記載は17世紀のRobert Hookeに遡り,それ以降から近代に至るまでの細胞に関する観察の集大成がEdmund B. Wilson による『The Cell in Development and Inheritance』である(1896年初版~1925年第3版:この間に書物のボリュームは3倍以上に膨れあがった).そのなかにはすでに生物の体や組織のサイズと細胞サイズの関係についての言及がなされている.いわく,「体のサイズは,個々の細胞のサイズよりも体を構成する細胞の総数に相関して規定されるようだ」.この結論は,貝類やウニといった現代生物学の礎を築くのに役立ってくれた生物たちの幼生などの観察に基づいたものであり,脊椎動物などもっと複雑な構造をもつ生物に対して単純に適用できるものではない.また,Wilson自身も触れているように,統計的な正確さを担保しながら体・組織サイズと細胞サイズの相関を測るのはデザインが難しい実験でもある.しかしながらそれ以降も細胞の大きさについての考察は,主に疾病に関連する臓器の局所的な異常に付随する形で記述を重ねていく.この,いわば受動的な立場にしばらく置かれていた「サイズ」の問題を,看過すべからざる科学的興味の対象に引き上げたのが遺伝子ノックアウト動物の登場である.特に,ホスホイノシチド3キナーゼ(PI3K)シグナル経路やインスリン受容体経路におけるさまざまな分子の機能欠損型変異がショウジョウバエの体,器官,細胞のサイズを軒並み小さくし,反対に機能獲得型変異では大きくなるという衝撃的な報告が1999年に相次いで発表され,細胞の大きさが臓器や体サイズに与える影響についての議論を再燃させることとなった1).
ここで問題となったのがまたしても「数」と「大きさ」である.細胞は分裂周期を経てその数を増やす.分裂するためには少なくとも遺伝情報を倍加させ,タンパク質やその他の成分も娘細胞2個分を賄う程度に増やさなければならない.直感的には,周期を早く回す方向に作用する分子が活性化すると細胞の数は増え,細胞の構成成分を増やす役割を担う分子が活性化すると細胞は大きくなると考えられるだろう.これらは相互に作用しあう部分もあるため,ある分子の活性化が数とサイズの両方に対して正の作用をもつ場合もあるはずだ.一方で,細胞はただ増えるだけでなく積極的に死ぬことで全体のバランスをとろうともする.現在のところ少なくとも臓器サイズについては,こういった細胞の数の調節と個々の大きさの両方が影響するという理解に落ち着きそうである2).本特集では,さらに踏み込んで細胞自身にかかる力学的要素(圧迫・伸展)により組織・器官サイズがダイナミックに制御される姿を紹介する(平島の稿).
細胞と分子スケールのサイズ生物学
さてそれでは細胞自身のサイズはどのように決められるのであろうか.前項で触れた細胞周期に照らしてみると,周期をゆったりと回る細胞は大きくなる余裕をもち,逆にせわしなく周期を終える細胞は小さいまま次の周期に入り縮んでいくように思える.しかしながら多くの細胞集団はある一定の大きさの範囲に収まっているのが現実である.その恒常性を維持しているものは何か.この困難な問題への挑戦については,バクテリアや酵母など単細胞のモデル生物を使った研究が先行しており,そこでの議論を理解することは他のサイズ問題を考えるうえで大いに参考となるだろう(加藤の稿).マイクロデバイスの加工技術の進歩により,最近は哺乳類の細胞を対象にした精密で興味深い研究も展開されつつある3).
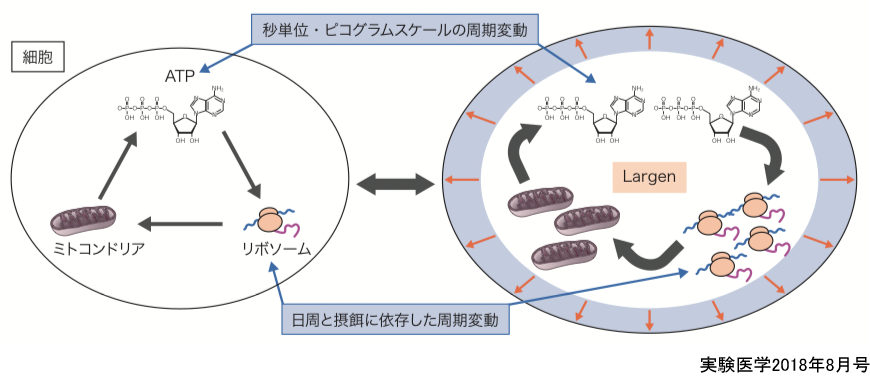
詳細については本文とコラム参照.
筆者は,細胞サイズ恒常性の維持機構を遺伝子のレベルで記述できないかと考えヒトの細胞を用いた遺伝子スクリーニングを行い,いくつかのサイズ調節候補遺伝子を同定した.そのうちの1つで過剰発現により細胞を大きくすることからLargenと名付けた遺伝子産物は,ミトコンドリアの量を増やしタンパク質合成を活性化することで細胞マスを増加させると考えられた(図)4)5).この事実によってのみならず,細胞サイズはそれが内包する成分に影響を受けうることは容易に予想される.特に細胞核や有糸分裂の際に形成される紡錘体,中心体などの大きさが細胞自体のサイズと相関があることが古くから指摘されている6).しかしその相関を生み出す機構についてはまだ完全には理解されていない.この問題について,本特集のもう一人の編者である原が歴史を紐解きつつさまざまな角度から考察する(原の稿).
ミトコンドリアやゴルジ体などの細胞小器官も,核と同様に細胞サイズを規定するのに少なからぬ影響を与えていると考えられる.かの複雑な袋状構造物はいかにして形成され集積し細胞内に収まるのか.この問題にリン脂質を成分とする物理モデルの構築から迫る取り組みを紹介する(立川の稿).また,細胞質にはタンパク質分子が自己集合して形成する細胞骨格というネットワークも存在する.その形状と構造によって保持されるテンションや骨格自身の流動性・可塑性も細胞サイズの調節には欠かせないと考えられる.この点に関し,実験的にサイズ調節が可能な人工細胞という閉鎖空間に封じ込められたアクチンとミオシン分子のふるまいからもたらされた気鋭の研究成果を披露してもらう(宮﨑の稿).細胞に含まれる分子として主要な成分であるタンパク質や脂質と,それらが集合して生み出される中間的なサイズの構造物が細胞スケールのサイズ調節にどのようにかかわりうるか,また逆に決められたサイズの細胞に包まれているがために生じる分子の挙動から細胞小器官,ひいては生命現象全体を捉えるユニークな視点を提供してくれるものと期待している.
個体と種間のサイズ生物学
「大きい」ことへの驚きに導かれながら,ここに至って話題の目盛りはどんどん小さく細かになってしまった.再び肉眼で観察することができる世界に目を向けよう.最も身近にあるのが,われわれ自身の身体のサイズの個体差だ.毛髪や肌,眼の色といった,色素合成に関連すると予想される限られた数の遺伝子の差によって生み出される違いとは異なり,体サイズは遙かに多様な要素により左右される.そのなかにあって成人の身長は遺伝的要因によるところが大きいため,全ゲノムシークエンシングを用いた分子集団遺伝学の研究対象として精力的に解析が進められている7)8).もう少し多彩な表現型に目を向けるとすればそれはイヌの世界になるだろう.体重2 kg前後のチワワから100 kgを超えるセントバーナードまで,陸生哺乳類としてこれほどの体重差を示す種は他に見当たらない.その多様性は体重のみにとどまらず,毛並みや体型,耳や尻尾の長短など広範囲にわたる.発生生物学者ならば特に胴体と四肢の長さの比率の調節機構に興味をそそられるのではないだろうか.しかしながら体サイズ制御にかかわる遺伝子の解析に比べると,イヌの四肢の長さの調節についてはまだあまりわかっていない9).この体と器官のプロポーション(配置・比率)という問題に対し,イヌよりはかなり平坦な見かけになってしまうが,プラナリアの再生系と遺伝学を駆使して挑んだ研究の最前線を紹介したい(梅園の稿).さらに,バクテリアからクジラ,化石から原生生物,細胞から臓器,個体にわたって時間と空間の尺度を乗り越え,各段階で考えられる種々の制約から「サイズ」の問題を考察してもらった(八木の稿).本特集を締めくくるにふさわしい,スケールの大きな話題になると確信している.
おわりに
本特集は,2017年12月に神戸で開催された生命科学系学会合同年次大会(Con Bio 2017)におけるワークショップ「“サイズ”で斬る分子細胞生物学」を契機としている.トピックの構成と誌面の都合上,先のワークショップ演者のごく一部にのみ執筆を依頼することになってしまったが,あの会場の熱気がなければここにつながることはなかった.すべての演者とご来聴の各位にあらためて感謝の意を表したい.その火をともし続けるべく,2019年3月19日から2日間の日程で「サイズ生物学ワークショップ」と題し,前述演者と本特集の執筆陣を中心とした集会を下関市海峡メッセにて催すことにした.ご興味がおありの方は,筆者Profile欄のURLをご参考にお問い合わせのうえ,奮ってご参加いただきたい.
「サイズ生物学」という旗印の下,足早にミクロからマクロの世界を剪断してみたが,斬るべきものはまだ至るところに転がっている.またその切り口は人それぞれに見え方が違うかもしれない.例えば細胞サイズに関しては,ミトコンドリア機能との関連が深いことから代謝への影響が強く示唆される.このことから潜在的に多くの疾患の裏側で細胞サイズの変換が生じているかもしれない4)10).
さらに踏み込んで言えば,「斬る」道具は何も「サイズ」だけであるとは限らない.つまるところ,これまで目にしてきたことやこれから目にすることを,少し違った(おかしな)角度から見つめ直すと,思いもしなかった世界が拓けるかもしれないということだ.われわれはこれからも「サイズ生物学」の旗を振り続けるが,それに共感してこの流れを広げてもらえればよし,さらに全く違った刀で別の世界を斬って見せてもらえるのであればなおのことよしと考えている.読者諸氏が抱える諸々を叩き斬り,何かに踏み出すきっかけとしていただけるなら,本特集もそこそこの成功を収めたと言わせてもらえるだろう.
文献
- 1) Kozma SC & Thomas G:Bioessays, 24:65-71, 2002
- 2) Tumaneng K, et al:Curr Biol, 22:R368-R379, 2012
- 3) Varsano G, et al:Cell Rep, 20:397-410, 2017
- 4) Yamamoto K, et al:Mol Cell, 53:904-915, 2014
- 5) Yamamoto K & Mak TW:Dev Growth Differ, 59:33-40, 2017
- 6) Heald R & Gibeaux R:Curr Opin Cell Biol, 52:88-95, 2018
- 7) Lango Allen H, et al:Nature, 467:832-838, 2010
- 8) Marouli E, et al:Nature, 542:186-190, 2017
- 9) Schoenebeck JJ & Ostrander EA:Annu Rev Cell Dev Biol, 30:535-560, 2014
- 10) Miettinen TP, et al:Bioessays, 39, 2017
- 11) Sinturel F, et al:Cell, 169:651-663, 2017
- 12) Martínez-Martín D, et al:Nature, 550:500-505, 2017
著者プロフィール
山本一男:1992年 大阪大学大学院理学研究科生物科学専攻後期課程修了,同年より埼玉医科大学医学部第二生化学教室助手.学部・大学院では大阪大学蛋白質研究所にて転写因子と核酸の構造と機能について京極好正教授のご指導をたまわる.埼玉医科大学では村松正實教授のもと,リボソームRNAの転写制御の研究に携わる.このとき核小体が細胞の状態によって大きさを変えることを知り,「サイズ」問題に興味を抱くようになった.’97年 長崎大学医学部講師,同大学院医歯薬学総合研究科助教授を経て2004年に渡加,トロント大学・キャンベルファミリーがん研究所Tak W. Mak所長の後押しを得て細胞サイズ研究に着手する.’07年 同研究所上席研究員を経て’12年より現職.「サイズ生物学」をともに盛り立ててくれる若者を広く募集中.http://www.med.nagasaki-u.ac.jp/brsc/dcfrs/

 Fantastic Voyage
Fantastic Voyage










