概論
RNA修飾研究の新展開〜遺伝子発現制御に隠されたシステム:エピトランスクリプトーム
Beyond genome and epigenome:Emerging impacts of epitranscriptome
深水昭吉,五十嵐和彦
Akiyoshi Fukamizu/Kazuhiko Igarashi:Life Science Center for Survival Dynamics, Tsukuba Advanced Research Alliance, University of Tsukuba/Department of Biochemistry, Tohoku University Graduate School of Medicine(筑波大学生存ダイナミクス研究センター/東北大学大学院医学系研究科生物化学分野)
真核細胞のエピゲノム(epigenome)の根幹であるクロマチンの構成因子,DNAとヒストンが修飾されると同様に,遺伝子発現からリードアウトしてきた転写産物(transcript)であるRNAが修飾されるエピトランスクリプトーム(epitranscriptome)が注目を集めている.mRNA,tRNAやrRNAなどの個別分子の修飾が担う役割を考える分子生物学的視点と,修飾が特定の機能にかかわる一群のRNAセットの発現をどう変化させるのかというネットワーク生物学的視点からの研究が進展することが,発生,分化,細胞増殖,生殖,神経,免疫や寿命など複雑な生命現象の解明につながるだけでなく,病気の理解と診断・治療への新しいアプローチとなることが期待される.
はじめに―エピゲノムの歴史
1942年にWaddingtonが提唱したエピジェネティクスは,細胞分化のように一つの遺伝型が複数の表現型をつくり出すプロセスを意味していた1).その後,哺乳類のゲノムには約20,000個の遺伝子がコードされていて,それらの遺伝子が転写された後に,翻訳されたタンパク質が細胞機能を発揮するというセントラルドグマの概念は,1958年に提唱された.転写を誘導するしくみの研究から,遺伝子の上流に位置するプロモーターやエンハンサーのDNA配列が同定され,それらのDNAに特異的に結合する転写因子の発見が相次いだ.これを皮切りに,転写因子と共役して遺伝子発現を活性化,あるいは抑制する制御因子も多数見出されてきた.まさに,シスエレメントとトランス因子の研究が大きく発展し,日本人の多くの研究者が貢献してきた.
それと相まって,基本転写因子の精製や同定の研究が進展し,転写の活性化や抑制のメカニズムが,DNAエレメント・転写因子・制御因子・基本転写因子と組合せて,ゲノムDNAから転写されるRNAの「量」の調節として説明されるようになってきた.そして,もう一つの大きな潮流が,リン酸化,アセチル化,ユビキチン化やメチル化など,化学修飾によってこれらの転写因子群の活性や分子間の結合が調節されるという制御因子の『質』の研究である.このような『質』の調節では,転写因子群(タンパク質)のみならず,クロマチン化学修飾,すなわち後述のようにエピゲノムが注目されてきた.
ゲノムとエピゲノムは,われわれの細胞がもつ2つの遺伝情報であるが,ゲノムについては,ヒトをはじめ多くの生物種のゲノムDNAの塩基配列の全容が明らかになっている.一方,エピゲノムは,DNAとヒストンから構成されるクロマチンが修飾されて,遺伝子発現の調節に重要な役割を果たしていることが解明されつつある.すなわち,DNAのメチル化や,ヒストンのリン酸化,アセチル化,ユビキチン化やメチル化などが目印となって,クロマチン構造が閉じることで遺伝子発現が抑制され,あるいは開くことによって遺伝子の発現が誘導されるしくみとして理解されてきた.
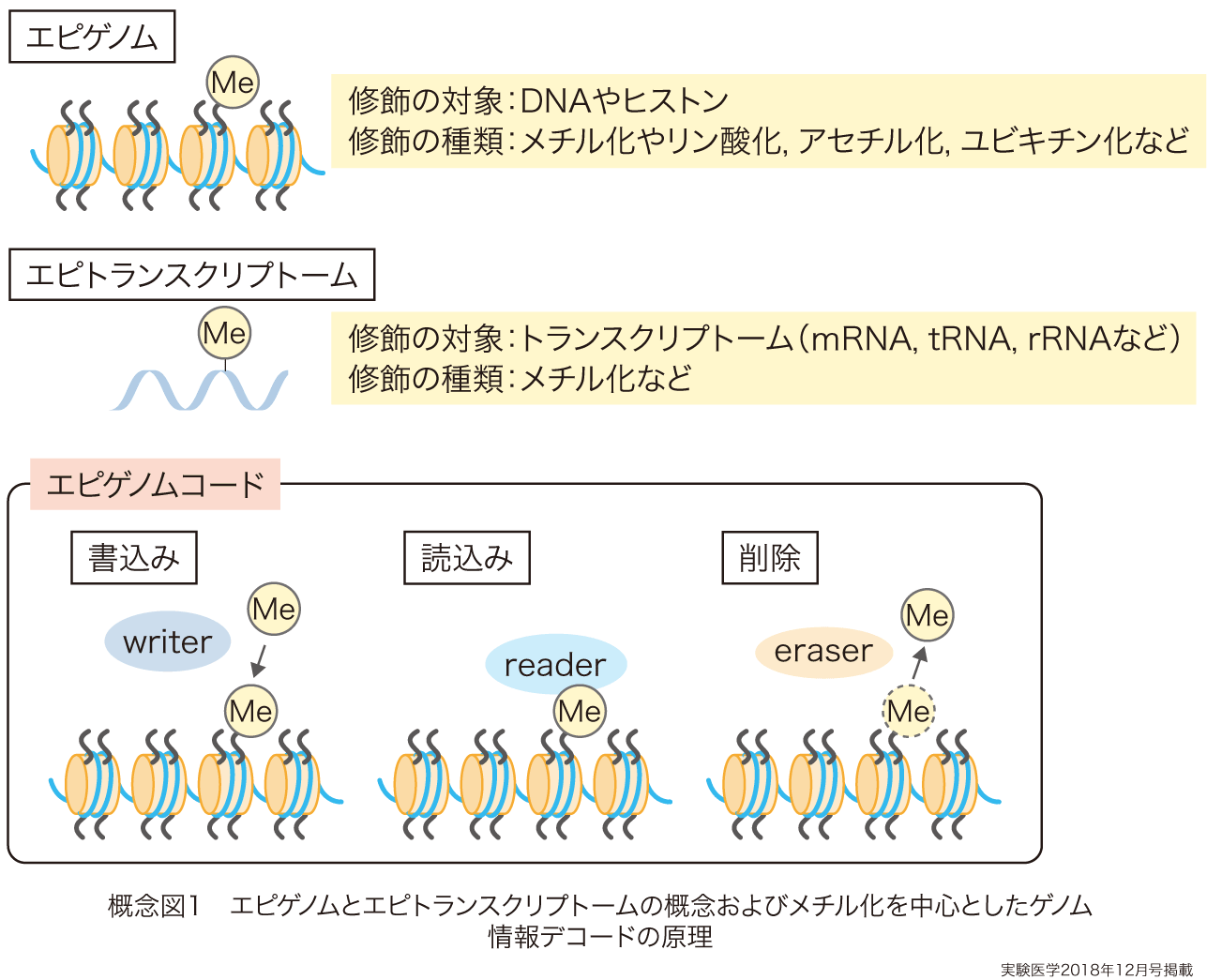
細胞をとり巻く環境の変化は,ホルモンなどのリガンドは細胞膜上の受容体を介して,あるいは栄養分子などは物質交換を経て細胞内代謝を介して入力され,その一部がエピゲノム情報に変換されていく.その過程では,まず触媒酵素(writer)によってDNAやヒストンが修飾されることでエピゲノム状態が変化し,その修飾基(リン酸化,アセチル化,ユビキチン化やメチル化など)が化学的目印となって結合タンパク質(reader)がリクルートされ,さらに大きな複合体が形成されることで転写が活性化,あるいは抑制される.一度書き込まれた修飾情報は,修飾基を外す脱修飾反応を触媒する酵素(eraser)によってエピゲノム状態がリセットされることで,遺伝子発現が調節されている.これらの修飾調節因子はdecoderとして作用し,書き込み,読み出し,消去するしくみはエピゲノムコードとよばれている(概念図1).このように,Waddingtonの提唱した一つの遺伝型から複数の表現型をつくり出すという意味でのエピジェネティクスは,シグナル伝達や代謝,転写因子,エピゲノム修飾関連因子などを含む分子のネットワークとして理解できる可能性がある.
1エピトランスクリプトームとは
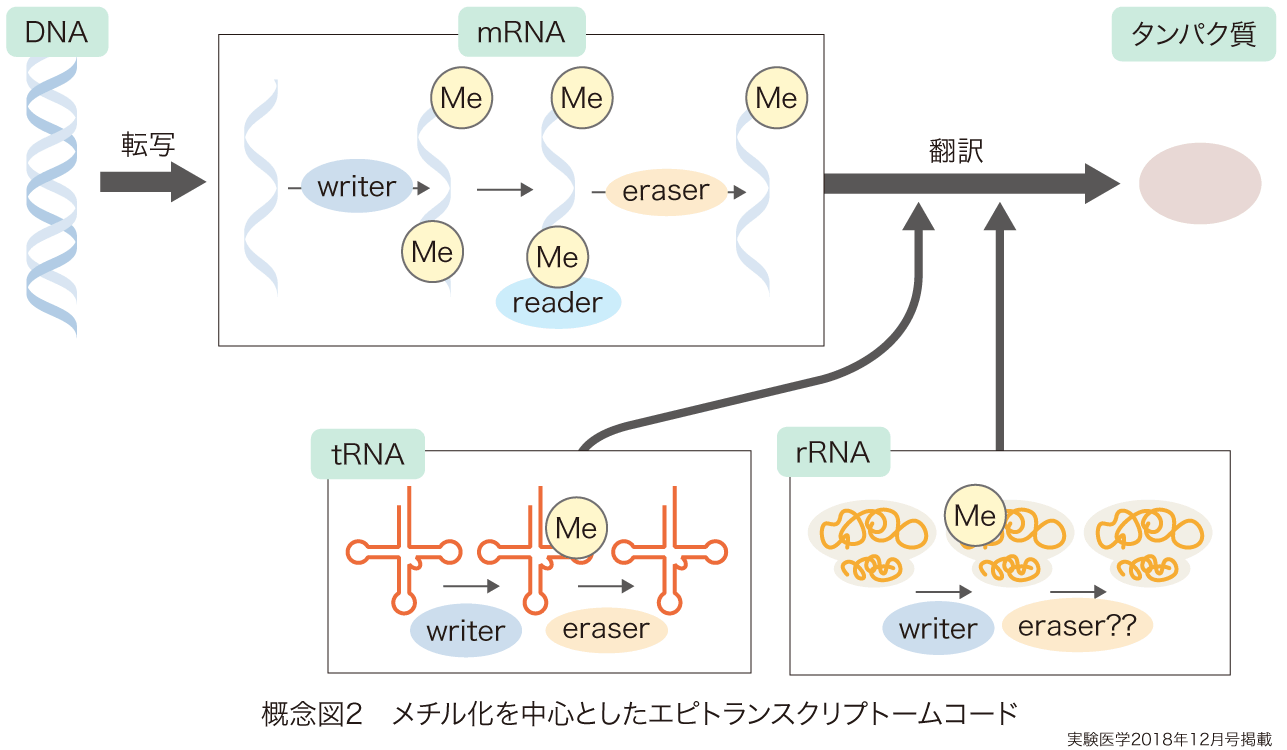
それでは,RNA情報はどのようにリードアウトされるのであろうか? 最近,エピトランスクリプトームコード2)(概念図2)とよばれる新しい考え方が提唱されているが,それは,エピゲノムコードとよく似たしくみが利用されている.例えば,mRNA,tRNAやrRNAをメチル化する触媒酵素が明らかになりつつあり,これらはwriterとしての役割を果たす.修飾RNAのreaderやeraserも報告されつつある.
本特集の主題の一つとして,鈴木の稿,島・五十嵐の稿,Fustin・柏﨑の稿,飯田・王の稿,宮田らの稿でRNAのメチル化をはじめとした修飾に関する話題を取り上げた.RNAに転位されたメチル基をreaderが認識し,RNAの局在などに影響を及ぼしていることが報告され3),readerの多様な機能が注目される.また,メチル化されたRNAを脱メチル化する酵素,eraserが見出されて機能的役割の解明が進展しており,上田・辻川の稿で取り上げた.これらの生物学的意義の解明の研究には,RNAにどのような修飾が生じているかを検出・同定する高精度な解析技術や,特定の修飾を改編するRNA編集技術の進展が不可欠である.これらについて櫻井の稿,福田の稿,飯田・王の稿で,応用面を含めて詳細に解説されている.さらに,堀の稿ではtRNA研究の最新の話題がとり上げられている.
2エピトランスクリプトームの今後の展望
エピトランスクリプトームとエピゲノムのアナロジーから,今後の研究の方向性を考えてみたい.まず,RNA,DNA,そしてヒストンの修飾は,これら修飾自体を直接操作してその結果を見るという実験は現実的ではなく,生物学的意義は長いこと不明であった.大きなブレークスルーはエピトランスクリプトームでもエピゲノムでも,writer,reader,そしてeraserの同定であり,これらタンパク質を操作することで修飾状態を変え,あるいは修飾下流で起きる反応を操作することが可能となった.エピトランスクリプトームの生物学的意義をさらに理解していくうえでは,かかわるタンパク質の全貌とそれぞれの機能を解明することが急務と思われる.
遺伝子産物のタンパク質は,複数のタンパク質と相互作用し,ネットワークや複合体を形成し,そのコンテクストのなかで機能する.すなわち,各タンパク質の機能はネットワークや複合体を形成することで多様化する可能性がある.だからこそ,一つの遺伝子の機能を考えるうえで,ネットワークや複合体の解明が必要とされてきた.このような考え方は分子生物学からネットワーク生物学4)(モジュール生物学という言葉も提唱されている)へのターニングポイントであり,iPS細胞5),iCM細胞6)やiHep細胞7)などの転写因子による細胞の運命転換への意義とつながっている.
このような流れのなかでエピゲノム研究を振り返ってみると,RNA修飾の役割を考える視点として,2つの見方があると思われる.1つは,個別のRNAについて,その修飾が担う役割を考える分子生物学的視点である.もう1つは,ある修飾がトランスクリプトームの亜集団,特定の機能にかかわる一群のRNAセットの発現をどう変化させるのかという,ネットワーク生物学的視点である.エピゲノムでは,しばしば特定の遺伝子セットが共通の制御を受けることで発現の統合性が担保される.同様のしくみがエピトランスクリプトームにも見出される可能性は高い.エピトランスクリプトームの役割を理解するうえでは,両方のアプローチを組合わせていく必要があると思われる.
エピゲノム制御とエピトランスクリプトーム制御にかかわる修飾は,いずれも代謝中間体を修飾反応の基質とする8).この事実と,細菌や酵母などの単一細胞生物における遺伝子発現制御は主に栄養源も含めた環境応答にかかわることをふまえると,エピゲノム制御やエピトランスクリプトーム制御は環境応答,なかでも,栄養応答に起源があるとも予想できる.もしそうだとすると,栄養や代謝にかかわる遺伝子・RNAセットに特異的なエピトランスクリプトーム制御が見出される可能性も考えられる.
おわりに
上に述べたように,エピゲノムとエピトランスクリプトームの情報のリードアウトのコードは,メチル化のwriter,readerやeraserという観点からは確かに類似しているように見える9).しかし,現時点においては,2つのコードでdecoderとして重複利用されている同じ分子は見あたらない.今後,2つの情報のリードアウトに重複利用される分子(例えば,タンパク質とRNAの両者を基質とするメチル化酵素など)が見出されるのか,研究の展開に注目したい.また,ゲノム,エピゲノム,エピトランスクリプトームの分子の進化を考えた場合,writer,readerやeraserのしくみが,クロマチンを中心に発展したのか,RNAが中核となって構築されてきたのか,どのように進化してきたのかもたいへん興味深いところである.
本特集号が,RNA修飾ネットワーク研究の端緒となれば幸いである.
文献
- Morange M:Ann N Y Acad Sci, 981:50-60, 2002
- Kadumuri RV & Janga SC:Trends Mol Med, 24:886-903, 2018
- Zhou J, et al:Nature, 526:591-594, 2015
- Cahan P:Nat Genet, 48:226-227, 2016
- Takahashi K & Yamanaka S:Cell, 126:663-676, 2006
- Ieda M, et al:Cell, 142:375-386, 2010
- Sekiya S & Suzuki A:Nature, 475:390-393, 2011
- Campbell SL & Wellen KE:Mol Cell, 71:398-408, 2018
- Kako K, et al:J Biochem:10.1093/jb/mvy075, 2018
著者プロフィール
深水昭吉:1983年筑波大学第二学群農林学類卒業,’87年筑波大学農学研究科単位所得退学,遺伝子実験センター助手,’94〜’95年SALK生物学研究所博士研究員,’95年筑波大学応用生物化学系助教授,’99年筑波大学先端学際領域研究センター(現 生存ダイナミクス研究センター)教授.遺伝情報に大きな作用をもつメチル化について,線虫とマウスの遺伝学.生化学を活用し,新しいメチル基転移酵素を同定しながら,生物学的意義の解明に取り組んでいる.
五十嵐和彦:1987年東北大学医学部卒業,’91年東北大学大学院医学研究科修了,’91年シカゴ大学リサーチアソシエート,’93年東北大学医学部助手,’95年筑波大学先端学際領域研究センター講師,’98年東北大学医学部助教授,’99年広島大学医学部教授,2005年東北大学医学系研究科教授.赤血球やリンパ球の分化や応答を制御する遺伝子とタンパク質のネットワークの解明に取り組んでいる.がんや貧血の病態を分子ネットワークに基づいて理解したい.












