概論
さあ皆さん,一緒にヒト免疫学をしませんか
ヒト免疫学の最新アプローチと今後の展開Let’s roll the human immunology together! : New approaches for human immunology research and its perspective
上野英樹
Hideki Ueno:Department of Immunology, Graduate School of Medicine, Kyoto University/ASHBi Institute for the Advanced
Study of Human Biology, Kyoto University(京都大学 大学院医学研究科 免疫細胞生物学/京都大学 高等研究院 ヒト生物学高等研究拠点)
革新的なマウスモデルを用いた“マウス免疫学”の発展により,私たちの免疫学の知識は格段に増加した.しかし一方で,マウスで得た知見のヒト臨床への応用には限界があることもわかってきた.ヒト免疫機構の理解,さらにヒト疾患病態の解明には,ヒト由来検体を用いたヒト免疫研究が重要である.ヒト免疫学を支えるテクノロジーはこの10年で飛躍的に進歩し,アプローチも大きく変革した.21世紀のヒト免疫学は「健常人検体を用いたヒト基礎免疫研究」,「患者検体を用いたヒト臨床免疫研究」,「ヒト免疫学の技術革新」の融合により今後一層飛躍し,その重要性,役割,魅力は増し続けると考えられる.さあ,皆さん,一緒にヒト免疫学をやりませんか?
はじめに
ジェンナーが牛痘ウイルスの接種による天然痘感染予防の発見,いわゆるワクチンの開発に世界で最初に成功したのは1798年である.抗体反応やT細胞反応の詳細なメカニズムが判明したのは1980年代であり,ワクチンによる免疫学的機構が解明されるまでに実に200年近く要したことになる.免疫学が飛躍的に発展したのはここ50〜60年程度のことで,主に哺乳類が免疫学の実験に多用されるようになってからである.それ以前の研究では,1883年にメチニコフが最初に血液中の貪食細胞を見つけたのはヒトデの幼生であったし,1950年代にグリックが最初にB細胞とT細胞の存在を示したのはニワトリであった.哺乳類が実験に多く使われるようになった20世紀半ば以降になると,例えばMHC(major histocompatibility complex)やHLAの作用に関する理解にはマウスを用いた移植拒絶の研究と,ヒトHLAと疾患との関連の研究がともに重要な役割を果たした1).したがって近代免疫学の黎明期には,動物モデルとヒトでの解析が等しく重要であったように思われる.しかし近年,遺伝子工学と解析技術が格段に進歩し,革新的なマウスモデルが実験に多く使われるようになり,マウスを用いた免疫学が世界的に主流になった.一方で,マウスモデルでの知見をヒト臨床に応用するには多くの限界があることが明らかになり,ヒト免疫学の重要性が広く再確認されるようになってきている.
本稿では,マウスとヒト,ヒト間での免疫系の違いを概説したのち,最近のヒト免疫学の手法における技術革新,今後の展望について説明する.さらに,本特集でご執筆いただいた先生方の内容についても少し触れたい.
1マウス免疫学の利点と限界
遺伝子工学の進化は革新的なマウスモデルの作製を可能にし,1980年代以降免疫学においてマウスを用いた実験系が世界的に主流になった.これらのマウスを用いて多くの謎が解明され,私たちの免疫学の知識は格段に増加した.間違いなく近年の免疫学の発展はマウスモデルとその解析手法の発展とともにあったと言える.これら,“マウス免疫学”の進歩に伴い,ヒト疾患における標的分子が多く発見され,そのいくつかは実際に非常に有効な治療に結び付いた.しかしその一方で,最終的に医薬品として認可されるのは臨床試験に至った候補のごく一部に限られていることも事実である.これは,マウスとヒトでの免疫系の違いのために,マウスで得た知見のヒト臨床への応用に限界があることを端的に示している.Davisが数年前の総説で述べているように,“NODマウス(Ⅰ型糖尿病モデル)やEAEマウス(多発性硬化症モデル)は何百通りの治し方が存在するのに,まだⅠ型糖尿病も多発性硬化症も克服できていない”のが現況である2).また,関節リウマチ治療で広く使用されている抗TNF-α抗体は,最初にその効果が認められたのはマウスではなくヒト炎症滑膜を使ったin vitroの実験からである3).
マウスとヒトの進化の分岐は約9,600万年前に起こり,その長い時間をかけて生態系に適する形でそれぞれ進化した.マウスとヒトは寿命も異なるし,もちろん住環境,食物も大きく異なる4).常在菌叢も異なれば,生涯にかかる感染症の種類も回数も異なる.独自の進化を遂げた免疫機構の違いにより,マウスモデルで得た知見とヒトの臨床試験で食い違いが出てくること自体は仕方がないことかもしれない.
2マウスとヒトでの免疫系の違い
ヒトとマウスの免疫系に違いがあることは以前から知られており,MestasとHughesは2004年に種差を網羅した総説を発表した5).有名な一例として,パターン認識受容体の一つであるTLR9(CpGなど病原体由来のDNAを認識する)がヒトでは形質細胞様樹状細胞やB細胞に発現されているのに対し,マウスでは加えて骨髄球系細胞にも広く発現されている.したがって,CpGをアジュバントに用いたワクチン,例えばHBV-CpG(Heplisav-B)B型肝炎ワクチンによる抗体産生機構はヒトとマウスで異なる.著者らは,“マウスの系でみられた反応がそのままヒトでは起こらないという可能性を常に考慮せよ”と書いている.
免疫システムのヒトとマウスでの差異は現在でも報告され続けている.2013年にはアメリカのImmGen(Immunological Genome Project)コンソーシアムがRNAシークエンスを用いた解析で免疫関連169遺伝子の免疫系での発現パターンの違いを報告している6).このリストのなかには,2019年にT細胞の腫瘍領域での疲弊化に重要な因子であることが判明した転写因子TOXが含まれる7).実際,TOXやTOX2のT細胞での発現制御機構がマウスとヒトで異なることを筆者も最近確認している8).また,筆者のグループを含む複数のラボが,抗体産生とB細胞の記憶形成に重要な役割を果たすCD4陽性T細胞サブセットである,濾胞性ヘルパーT細胞(follicular helper T,Tfh細胞)の分化経路,分画の機能などがヒトとマウスで異なることを報告している9).
2014年には,アメリカのMouse ENCODE(encyclopedia of DNA elements)コンソーシアムが,マウスの多彩な細胞のゲノム,エピゲノムのデータを公表し,ヒトとマウスのゲノムとエピゲノムの直接的な比較が可能となった10)11).結果,マウスとヒトで遺伝子の発現調節機構自体の多くが共有されている一方で,多くの差異も明らかになった.例えば,マウスとヒトではタンパク質をコードしている遺伝子の共有は約70%であること(しかもこれらは全ゲノムの1.5%に過ぎない)が判明した.また,ヒトとマウスの臓器ごとのゲノム,エピゲノムの比較では,一部の解析において同種内での臓器間の差よりもヒト・マウス間での同じ臓器の差の方が大きかった10).特筆すべきこととして,免疫に関与した遺伝子の遺伝子調節領域(cis-regulatory elements,CREs)に多くの種差が認められた.ヒトとマウスの免疫反応やその制御システムの違いの多くはこのCREsの違いによると考えられる4).
3生活環境の違いによる免疫系の差異
ヒト検体を用いて実験をしていると,検体間での差が概して大きいことに気が付く12).実際に,ヒト免疫応答はゲノムのみならず,ゲノム情報非依存性因子にも大きく影響される.例えば,一卵性双生児での比較において,血液中の細胞分画,免疫細胞の活性化能,血清中タンパク質分画は大きく双子間で異なり,ゲノム情報に依存しないさまざまな環境由来因子(多くは住環境,食物由来12))の違いが免疫応答に大きく影響を及ぼしている2).したがって,疾患においてどのようにヒト免疫がかかわっているかを理解するためには,ゲノム情報に加えて,各個人,各患者から実際に得られる検体の解析が非常に重要である.
マウスもヒトに近い環境で生育されると免疫系がヒトに近づくことが明らかになってきている.例えば,クリーンな研究室で飼育されたマウスよりも自然に生息するマウスの方がよりヒトに近い免疫応答をすることが2016年に報告された13).このいわゆる“dirty mice”がどの程度ヒト免疫モデルの代替として使用できるかは今後の検討を要するが,現在全世界的にいろいろな手法を用いて,ヒト化マウスモデルの進化など,よりよいヒトモデル作製方法が模索されている14)15).強調したいが,今後免疫学におけるマウスモデルの重要性が減っていくとは思えない.逆にヒトで得られた知見の生体内での検証や,ヒトモデルマウスを用いた前臨床試験になど,ヒト免疫学を補完する系として今後も重要であり続けるだろう.
4最新のヒト免疫研究のテクノロジー
つい最近までヒト免疫の実験は,サンプルの採取にかかわるさまざまな制限(例えば採取可能な血液サンプルの量,頻度,それに伴う倫理的,宗教的,文化的問題など)のために実施が非常に困難であった.しかしヒト免疫学を支えるテクノロジーはこの10年で飛躍的に進歩し,少量のサンプルからでも膨大な情報が得られるようになった.
まず免疫細胞解析で広く使われるフローサイトメトリー(FCM)が格段に進化した.1990年代のFCMは2レーザー仕様,4色対応がほとんどであったが,2000年代に入り,Violetレーザーが使用されるようになり,8色対応になった.2010年代後半にはYellowGreenレーザーやUVレーザーが追加され,BD FACSymphony,Cytek Aurora,Sony ID7000などFCMが4レーザーや5レーザーを備えるようになると最大測定カラー数は30〜40色と飛躍的に増加し,自然免疫系,獲得免疫系細胞のさまざまな細胞の評価が1滴の血液検体で可能となった.同様に40色以上の超多色解析が可能なマスサイトメトリー(Fluidigm Heliosなど)も2010年代中盤から広く使用されるようになった.
また,トランスクリプトミクスに使われる手法がマイクロアレイからRNAシークエンスへと移行し,microRNAやlong noncoding RNAの評価が可能となった.またここ5年ほどで10x Genomics Chromiumなどを用いてシングルセルレベルでのRNAシークエンス解析方法(scRNAseq)が急速に進化,普及し,新規免疫細胞分画の発見,検体内での免疫細胞分画の評価の効率が格段に改善した.クロマチン・アクセシビリティの評価が可能なATAC-seqも広く普及し,最近では10x GenomicsからシングルセルレベルでのATAC-seq手法がキット化された.これにより,遺伝子発現に関与するエピゲノム制御機構の評価がより詳細に行えるようになった.
さらに,血清,血漿などを用いたプロテオミクス,メタボロミクスの解析法,精度,情報量も進化した.トランスクリプトミクスを含むこれらオミクス手法,データを統合したsystems biologyのアプローチを用いると,仮説に依存せずバイアスのかからない方法で新規免疫応答制御機構の発見も可能になってきている.例えばワクチン接種後の抗体産生や細胞傷害性T細胞(CTL)反応を予測するバイオマーカー,免疫応答に関与する新規経路が発見されている4).
そして,従来ヒト免疫学には血液検体が主に使われていたが,最近10年ほどで組織検体を用いた解析が非常に重要であることがわかってきた.臓器にはマクロファージ,T細胞,B細胞,NK細胞など組織常在型免疫細胞が多く存在し,各臓器でのホメオスターシスの維持,免疫応答に重要な役割を果たしている16).組織での免疫細胞の評価(例えばがん免疫におけるチェックポイント阻害によるがん微小環境での免疫細胞の評価)は病態の理解,予後関連免疫応答の同定に重要な知見をもたらす.これら組織空間的免疫解析手法も近年進歩が著しい分野である.現在,イメージングマスサイトメトリー(Fluidigm Hyperionなど)や核酸バーコード付加抗体を用いた多重染色法(Akoya CODEXなど)を用いてFFPE切片で40種類程度のタンパク質マーカー解析が可能であり,免疫細胞が組織のどこでどの細胞と会合し,どのような表現型を示すかが詳細に解析できる.
今後は,これらテクノロジーの発展とともに,自家製データのみならず公共ドメインに蓄積されていくデータがヒト免疫学推進の非常に有用なリソースになっていくことは想像に難くない.拡大するデータベースから有効で確かな情報を発掘するために,今後はヒト免疫学者とバイオインフォマティシャン,数学者,統計学者などとの連携がますます重要になってくると考えられる.
521世紀のヒト免疫学
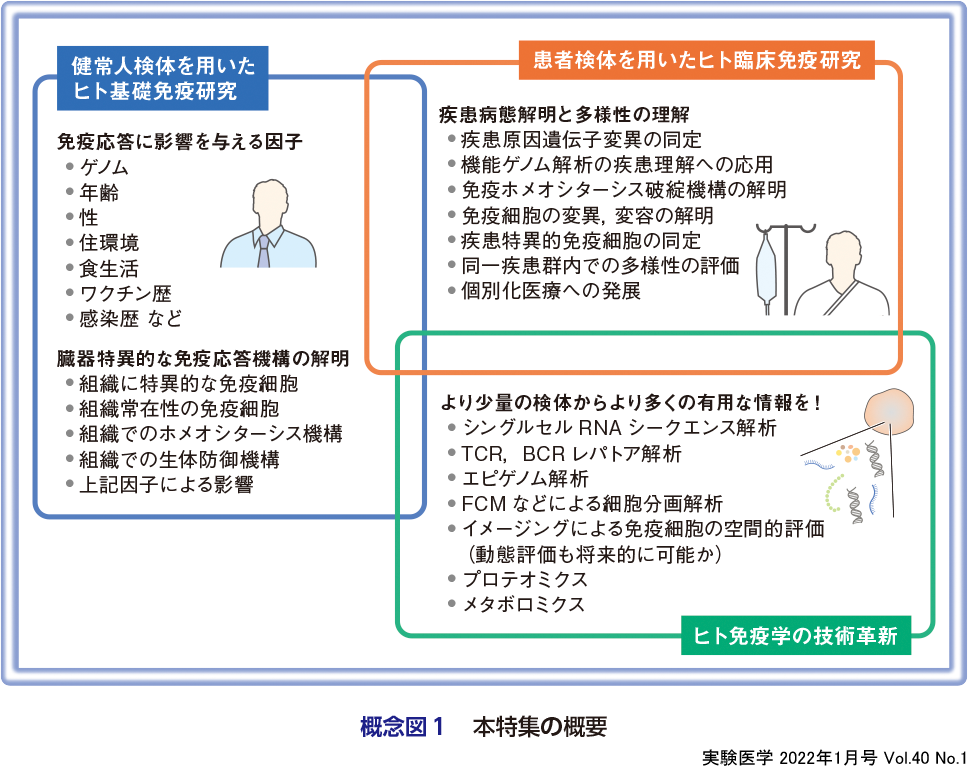
このようなマウス免疫学やテクノロジーの発展を受けて,「ヒト免疫学のいま」を整理する.まず,「健常人検体を用いたヒト基礎免疫研究」は今後も重要性がどんどん増していくと考えられる(概念図1).例えば新生児期から老年期に至るまで加齢がどのようにヒト免疫系に影響するか,ほぼ何も明らかでない.性差がどのように免疫系に影響するかもほとんどわかっていない.臓器特異的な免疫機構解明もまだ世界的に研究がはじまったばかりである.一方「患者検体を用いたヒト臨床免疫研究」は疾患病態解明と多様性の理解が今後進んでいくと考えられる.これらの臨床研究は疾患理解のみでなく,ヒト免疫機構の本質にも重要な示唆を提供する.例えば先天性免疫異常症において免疫応答異常を明らかにすることにより,担当遺伝子がどのようにヒト免疫細胞の分化,機能に影響するかが明らかになる.これらヒト基礎,臨床免疫研究を支えるのは「ヒト免疫学の技術革新」であり,データの質と量の改善,データ統合,解析方法の革新が今後加速度的に起こり続けると予想され,それに伴いヒト免疫学が発展していくと考えられる(概念図1).
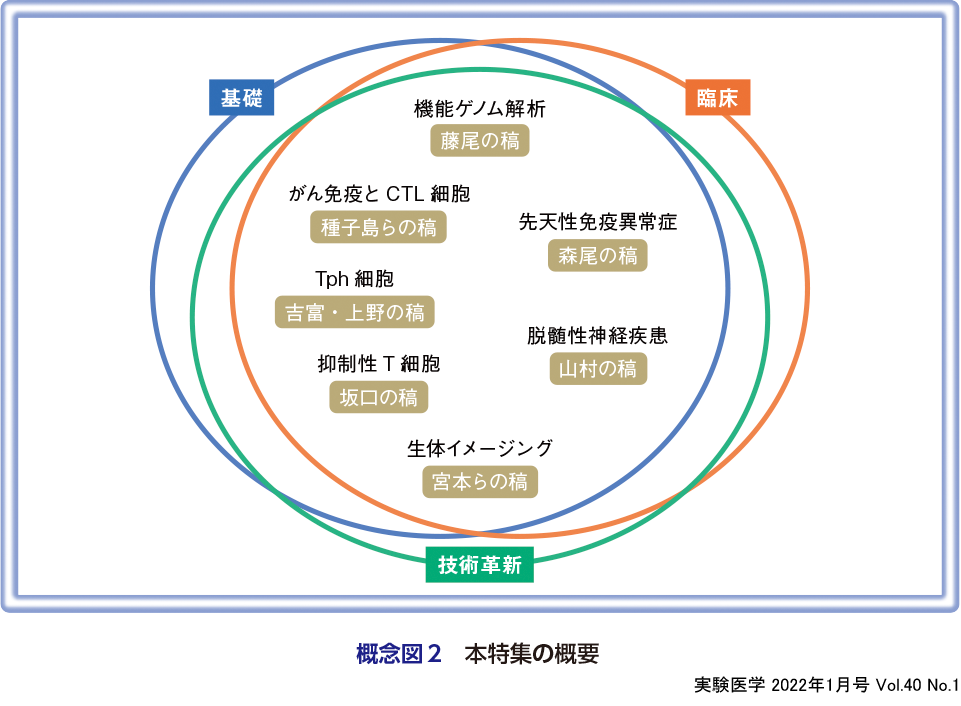
今回の特集では,ヒト検体を用いたヒト免疫研究を展開する先生方に最先端のご研究についてご執筆いただいた.当初は概念図1に従ってヒト免疫学の基礎,臨床,技術革新,の3つの分野を少しずつカバーできればと考えていた.しかしいただいた原稿を拝読すると,すべての原稿に基礎,臨床,技術革新の部分を含んでいることを再確認し,三者の密接な融合こそがこれからのヒト免疫学と確信した(概念図2).以下で,それぞれの各論について紹介する.
藤尾圭志先生は,機能ゲノム解析がどのようにヒト疾患の発症機構解明に役立つか,さらに独自に構築,公開された免疫細胞を多く含む機能ゲノムデータベースImmuNexUTの有用性について述べられている(藤尾の稿).西川博嘉先生らはがん免疫におけるCTL細胞の基礎と応用,さらには腫瘍検体の解析を通じて腫瘍内で制御性T細胞(Treg)が優位になる最新の知見についてご紹介されている(種子島らの稿).森尾友宏先生には先天性免疫異常症から明らかになるヒト免疫についてご寄稿いただいた.分子異常による新規機能障害の発見のみならず,遺伝子変異の感染免疫への関与,遺伝子変異部位の差による臨床表現型の差異など,この分野のヒト免疫理解への貢献の大きさが大変よくわかる内容になっている(森尾の稿).吉富啓之先生には筆者との共著で,マウスには存在しないCXCL13+ peripheral helper T(Tph)細胞の発見と分化機構,ヒト関節リウマチでの病態関与についてご執筆いただいた.自家製の関節リウマチの炎症滑膜と関節液中CD4+細胞のscRNAseqのデータも紹介されている(吉富・上野の稿).山村隆先生にはヒト中枢神経系炎症性脱髄疾患研究の歴史と最新の知見についてご寄稿いただいた.ヒト神経免疫研究は脳検体採取が難しくヒト免疫学展開が容易でない分野であるにもかかわらず,ヒト免疫学的アプローチでの成功例の非常に多い領域であることがとてもよくわかる(山村の稿).坂口志文先生にはヒトにおけるTregと疾患との関連についてご執筆いただいた.自己免疫疾患に関連する一塩基多型SNPとヒトTreg関連遺伝子エンハンサー部位の非常に興味深い最新の知見にも触れられている(坂口の稿).最後に,新技術開発研究として石井優先生らにより,ヒト生体ライブイメージング解析の現状と今後の展開についてご執筆いただいた(宮本らの稿).
おわりに
奇しくもSARS-CoV-2新型コロナウイルス感染症COVID-19によるパンデミックは,いかにヒト免疫解析が重要かを分野を超えて世界が再認識する機会となった.わが国は世界と比較してワクチン開発,COVID-19免疫研究で出遅れた感は否めない.筆者も2020年2月から感染患者血液検体の入手を試みたが,かなり多くの方々に手伝っていただいたにもかかわらず実際に検体を入手できるようになるまでかなりの月日を要した.今後はヒト免疫学を推進するうえでのインフラを含めた体制作りが重要となるだろう.
しかし,ヒト免疫学を推し進める技術はすでに十分なレベルに達していると考えられる.今後のさらなる技術革新,体制の改善により,ヒト免疫学はその発明,発見がよりダイレクトに患者に還元できる,とても魅力的で充実した実りの多い研究分野に育っていくことは疑う余地はない.
さあ,新しいヒト免疫学の時代の幕開けです.皆さん,一緒にヒト免疫学をはじめませんか?
 ヒト免疫学と私
ヒト免疫学と私
文献
- Zinkernagel RM & Doherty PC:Immunol Today, 18:14-17, doi:10.1016/s0167-5699(97)80008-4(1997)
- Davis MM & Brodin P:Annu Rev Immunol, 36:843-864, doi:10.1146/annurev-immunol-042617-053206(2018)
- Brennan FM, et al:Lancet, 2:244-247, doi:10.1016/s0140-6736(89)90430-3(1989)
- Pulendran B & Davis MM:Science, 369:doi:10.1126/science.aay4014(2020)
- Mestas J & Hughes CC:J Immunol, 172:2731-2738, doi:10.4049/jimmunol.172.5.2731(2004)
- Shay T, et al:Proc Natl Acad Sci U S A, 110:2946-2951, doi:10.1073/pnas.1222738110(2013)
- Scott AC, et al:Nature, 571:270-274, doi:10.1038/s41586-019-1324-y(2019)
- Horiuchi S, et al:Sci Adv, 7:eabj1249, doi:10.1126/sciadv.abj1249(2021)
- Ueno H, et al:Nat Immunol, 16:142-152, doi:10.1038/ni.3054(2015)
- Lin S, et al:Proc Natl Acad Sci U S A, 111:17224-17229, doi:10.1073/pnas.1413624111(2014)
- Yue F, et al:Nature, 515:355-364, doi:10.1038/nature13992(2014)
- Carr EJ, et al:Nat Immunol, 17:461-468, doi:10.1038/ni.3371(2016)
- Beura LK, et al:Nature, 532:512-516, doi:10.1038/nature17655(2016)
- Masopust D, et al:J Immunol, 199:383-388, doi:10.4049/jimmunol.1700453(2017)
- Graham AL:Nat Immunol, 22:111-117, doi:10.1038/s41590-020-00857-2(2021)
- Masopust D & Soerens AG:Annu Rev Immunol, 37:521-546, doi:10.1146/annurev-immunol- 042617-053214(2019)
本記事のDOI:10.18958/6941-00001-0000001-00
著者プロフィール
上野英樹:1992年京都大学医学部卒業,小児科に入局.2000年博士号取得後,’01年より米国テキサス州ダラスのベイラー免疫研究所にてポスドク,’04年より主任研究員となる.’16年米国ニューヨーク州マウントサイナイ医科大学,微生物学教室教授.’19年7月,京都大学大学院医学研究科免疫細胞生物学 教授に,クロスアポイントメントで着任.’21年4月より京都大学専属となる.研究の専門はヒト免疫学.ヒト検体を用いたヒト基礎免疫,臨床免疫学を行っている.












