概論
痛みのしくみと新たな役割,そして真の病態の理解へ
Recent advances in our understanding of pain mechanisms, new roles of the pain system and pathological pain
津田 誠
Makoto Tsuda:Department of Life Innovation, Graduate School of Pharmaceutical Sciences, Kyushu University(九州大学大学院薬学研究院ライフイノベーション分野)
痛みは,組織損傷などを生じるような有害な刺激から身を守るために必要な警告的感覚である.近年の神経科学的研究技術の発展によって,これまでわからなかった末梢での感覚センシング,脊髄後角での情報処理,脳での痛み生成に関する理解が,飛躍的に進展している.一方で,がんや糖尿病など多くの疾患で慢性化する痛みは,痛覚信号の持続的発生ということだけでなく,多種多様な変化による感覚伝達系の機能破綻が原因であることも分かってきた.さらに最近,痛覚神経が末梢組織や臓器,免疫系やがん細胞にも大きな影響を及ぼすという新しい役割も明らかになった.すなわち,痛覚システムの生体調節機構における幅広い役割は,生体の恒常性や病態メカニズムの解明に新しい切り口となる可能性がある.
はじめに
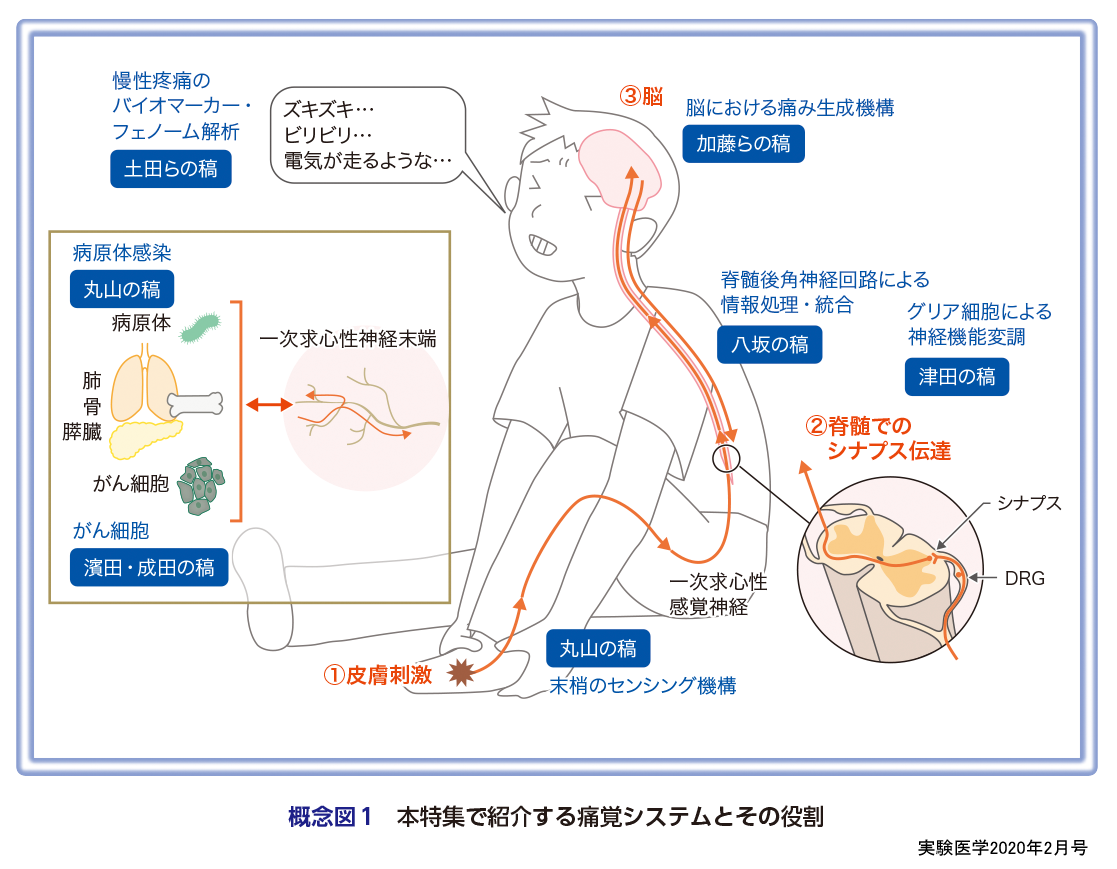
痛みは,われわれにとって安全に生きるために必要な生体警告系として役割を担い,多くの生物種が共通に保有する生体防御システムである.その役割が成立するためには,痛みを起こす有害な刺激(侵害刺激)を,非侵害刺激と区別して受容・伝達・処理・認知する必要がある.皮膚など末梢組織に加わる侵害刺激は,一次求心性神経の自由終末で受容され,その信号は電気信号に変換され脊髄後角※2へと入力し,さらに脳へと伝達される.この一連の流れは古くから知られているものの,外界からの多様な刺激に対して生物がどのようにそれらを区別して受容・伝達しているのか,そして侵害受容信号によって「痛み」はどのように生成されるのか,いまだ分からないことがじつは驚くほど多い.そのようななか,近年の神経科学領域で目覚ましく発展している光遺伝学等の細胞機能操作技術やシングルセル解析などから,末梢での感覚センシング,脊髄後角での情報処理,脳での痛み生成機構の理解が飛躍的に進んでいる.加えて,神経系には数多くのグリア細胞が存在し,神経活動そのものに大きな影響を及ぼしていることがわかり,神経-グリア相互作用から痛覚システムや慢性疼痛を考える必要が出てきた.これらの新しい知見から,慢性疼痛の治療に向けた新しい戦略も考案・実践されている.さらに最近,痛覚システムは,侵害受容と痛みの発生という役割を担うだけでなく,末梢組織や臓器,免疫系やがん細胞にも大きな影響を及ぼすという新しい側面を有することも示され,痛覚システムが幅広い生体調節機構に関与することが明らかになってきている.本特集では,基礎および臨床研究から得られた,生理および病態における痛覚システムに関する最新知見を紹介する(概念図1).
1一次求心性神経での侵害刺激センシング
外界からの侵害刺激による痛み発生プロセスは,一次求心性神経の侵害受容器の興奮からスタートする.1997年にカプサイシンや侵害性熱刺激を感知するTRPV1が発見されたのを契機に,刺激感受センサーの分子実体が次々と同定された.メルケル細胞の触覚センシングを担うメカノセンサーPIEZO2もその代表例といえる.シングルセル遺伝子解析では,一次求心性感覚神経は少なくとも10種類以上のサブセットに分類される.それぞれの役割が今後明らかになれば,多様な外界刺激に対するセンシング機構の理解が大きく前進するであろう.
また,病原体感染への警告信号としても痛みが利用される.従来は,感染による炎症応答の結果とされてきたが,じつは病原体由来成分や放出因子が直接侵害受容器に作用し痛みを誘発することがわかり,病原体感染においても痛覚神経が最前線で生体防御を担うことが示された.また興味深いことに,一次求心性神経は,真菌感染に伴う破骨細胞融合やマクロファージの炎症,膵β細胞からのインスリン放出や耐糖能異常,アレルギー性気道炎症にも関与することがわかり,骨免疫や代謝系など幅広い生体機能を調節するという痛覚システムの新しい役割が世界的に注目されている(丸山の稿).
さらに,がん細胞が放出する因子も侵害受容器を刺激して痛みを起こす.加えて,増殖したがん細胞による物理的な神経圧迫などもがん性疼痛の原因とされている.近年,がん患者への疼痛治療の早期介入は,患者のQOLのみならず,予後にも直接影響を及ぼすことから,疼痛緩和はがん治療の一環として重要な位置付けとされている.一方で,がん細胞は神経栄養因子(NGF)を放出し,腫瘍組織内へ一次求心性神経を誘引し,そこから放出される神経由来因子をがん細胞が自身の成長や微小環境リモデリングに利用しているという興味深いエビデンスも示されている.がん細胞はPD-L1を介してT細胞免疫応答に対する自己防衛システムを発揮するが,じつは侵害受容性一次求心性神経にもPD-1が発現しており,そのシグナルの活性化で痛覚伝達が抑制される.すなわち,がん細胞は生体警告系を抑制して,あたかも自身の存在を隠すかのような利己的システムを有する.その振舞にはただただ驚くばかりである.今後,痛覚神経-がん細胞-免疫細胞間の局所的なクロストークに関する研究から,がんの新しいメカニズムの解明と治療戦略の創出につながる成果が生まれる可能性が期待できる(濱田・成田の稿).
2脊髄後角での侵害受容信号の処理・統合
一次求心性神経を介した感覚情報は脊髄後角に入力し,同部位の神経回路で処理・統合される.脊髄後角は層構造(第Ⅰ層からⅤ層)を成し,脳へ侵害受容信号を伝達する投射神経(第Ⅰ層に局在)と局所回路を形成する介在神経が存在する(数的にはほとんどが介在神経).末梢からの機械性や熱性などの質の異なる感覚信号は,脊髄後角においても区別される必要があるため,対応する神経回路(あるいは活動パターン)が存在することが推察できる.神経細胞の形態や分子発現の違い,また近年のシングルセル遺伝子解析から,脊髄後角神経には数多くのサブセットが存在し,想定以上に複雑であることが最近明らかになった.それらが形成する神経回路と機能の全容解明に向けて,神経サブセットの可視化や機能制御技術などを駆使した研究が精力的に進められ,感覚種類別の処理メカニズムが徐々に明らかになってきている (八坂の稿).また,本特集ではとり上げないが近年では痒みに特化した神経回路についても研究が進んでいる1).
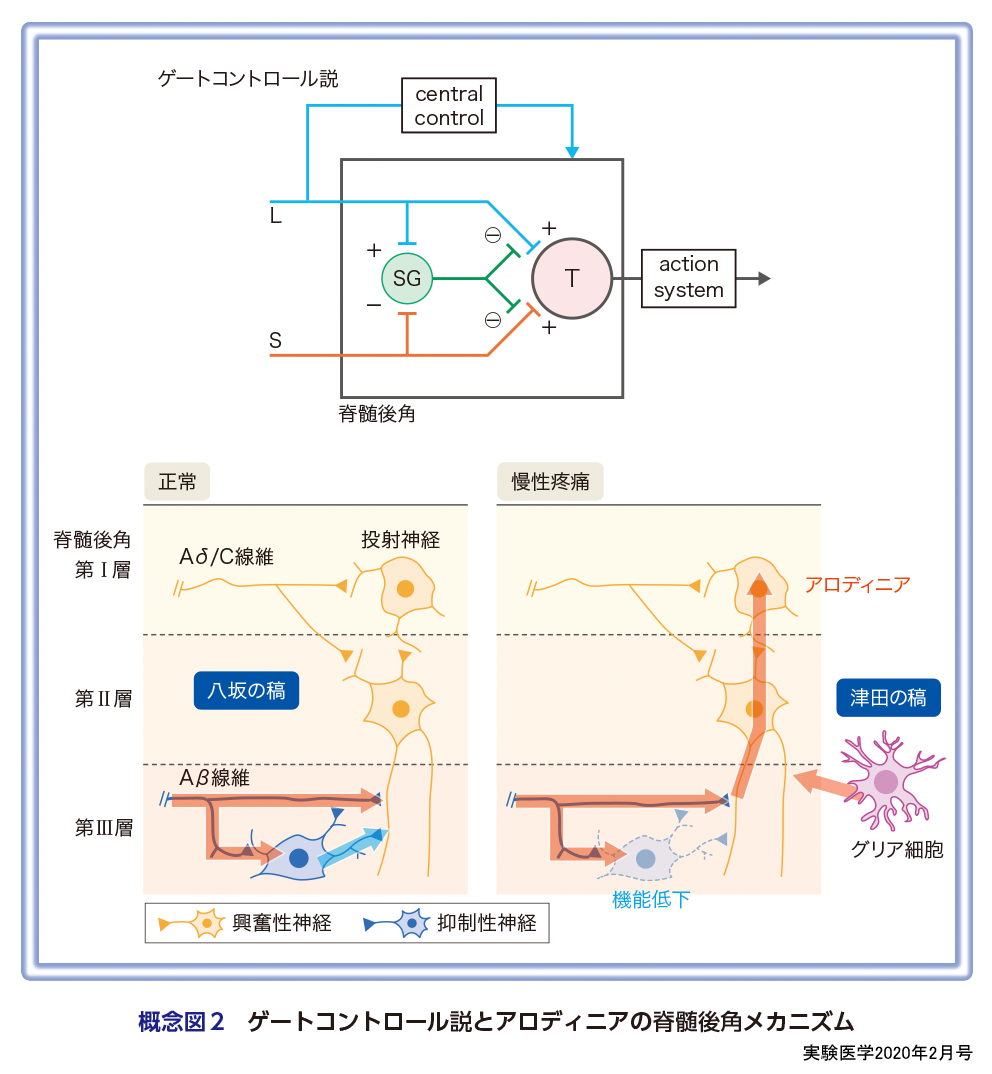
痛覚が生体警告系として役割を担うためには,侵害受容信号が脊髄後角で正確に処理・統合され脳へ伝達される必要があり,非侵害性信号が痛覚神経回路に入ってしまうことはあってはならない.しかし,がんや糖尿病,帯状疱疹後など神経系の損傷や機能不全が原因の神経障害性疼痛では,触刺激で痛みが出るアロディニア(異痛症)が発症する.アロディニアはどこでどのように起こるのであろうか? 1965年にMelzackとWallが提唱したゲートコントロール説2)では,末梢からの侵害受容信号の流入をコントロールするゲート機能が脊髄後角にあり,それを担うのが第Ⅱ層(膠様質)にある抑制性介在神経(SG神経)と報告している.SG神経は,Aβ線維(L)により活性化し,AδやC線維(S)から投射神経(T)への痛覚信号の入力を抑制する(概念図2).長らくSG神経の実体は不明であったが,その候補になりうるサブセットが最近複数特定された3).さらに,これら抑制性介在神経の機能低下により,遮断ゲートが開き,結果としてAβ線維からの入力が興奮性介在神経を介して第Ⅰ層投射神経に流れ込み,痛み,すなわちアロディニアが起こるというメカニズムが提唱されている(八坂の稿)(概念図2).
アロディニアに直結する脊髄後角神経の機能異常は,神経細胞自律的なメカニズムだけでなく,グリア細胞(ミクログリアやアストロサイト)からのシグナルも重要である4).ミクログリアは,神経障害性疼痛モデル動物の脊髄後角で著明に活性化し,細胞外ヌクレオチドで活性化するP2受容体など細胞膜受容体の発現を増加させ,その刺激で放出される液性因子(炎症性サイトカインやカテプシン,神経栄養因子など)が脊髄後角神経に作用して神経の異常興奮を引き起こす.ミクログリアは疼痛の発症に関与し,その維持には神経損傷後に遅れて活性化するアストロサイトが関与する.すなわち,グリア細胞の長期的活性化が,神経の機能異常を長引かせ,痛みが慢性化すると考えられている(津田の稿)(概念図2).
3侵害受容信号による痛みは脳でつくられる
国際疼痛学会IASPによる痛みの定義「An unpleasant sensory and emotional experience associated with actual or potential tissue damage, or described in terms of such damage」からわかるように,痛みは不快な感覚および情動体験であり,すなわち,脊髄後角まで到達した侵害受容信号は脳に運ばれた後,不快情動を生むことではじめて「痛み」となる.侵害受容信号からどのように痛みがつくられるのか? 脊髄後角から脳へ上行したシグナルは,脳の広範な領域を活性化する.この領域は痛みネットワークとよばれ,視床や体性感覚野に加え,島皮質,前帯状回,扁桃体,中脳水道周囲灰白質,側坐核など,不快情動の生成に重要な脳部位が含まれる.またこれらの脳部位では,慢性疼痛時にシナプス伝達の可塑的な変化が起こる.加藤らの稿では,負の情動の処理と記憶に関与する扁桃体中心核でのシナプス伝達が慢性疼痛時に可塑的に増加し,それが侵害受容と情動生成の連合を強め,また下行性疼痛制御ネットワークにも影響を及ぼすことで,痛みの中枢性感作が形成されることを紹介する.また,前帯状回や体性感覚野などの脳部位から脊髄後角へのトップダウン調節機構も最近注目されており,従来の末梢→脊髄→脳という一方向性のシグナルだけでなく,脳-脊髄後角間のシグナル増幅機構を含めて慢性疼痛メカニズムを包括的に考える必要性があると思われる.
4慢性疼痛の治療に向けた新しい戦略
がん領域を中心に,患者個人から得られた精密な情報をもとに病態・疾患をより詳細に階層化し,最適な診断と治療法を提案する精密医療(precision medicine)が実現化しつつある.また,マルチオミクス解析から得られた情報を包括・統合的に分析して病態について解き明かすバイオインフォマティクスに加え,患者から抽出した臨床症状・徴候をもとにしたフェノーム解析も併せた,より精密な個別化(personalized)医療が展開されている.痛み領域においても,precision medicineによる患者の発症機序や治療法の階層化が提案されている.痛みは主観的なものであるため,従来の分子生物学的なバイオマーカーに加え,臨床症状によるフェノーム解析も発症機序の解明や客観的評価および治療法の選定に非常に重要であることを,土田らの稿で紹介する.
おわりに
本特集では,痛みが生み出される神経科学的しくみ,痛覚システムが有する新しい側面,その異常による慢性疼痛,そして痛みの克服に向けた先端研究を紹介した.侵害刺激の受容・伝達・処理・認知メカニズムが徐々に明らかにされてきたが,「痛み」の理解にはいまだ道半ばである.また,痛覚システムというと,一般的には障害や炎症,疾患に付随する痛みを出すしくみとして捉えられるが,本特集で紹介したように,最近では末梢組織や臓器,免疫系やがん細胞にも大きな影響力を及ぼすという新しい側面も明らかになり,今後は,生体調節機構として痛覚システムの役割をより幅広く考える必要がある.それによってこれまで未解明であった生体の恒常性や病態メカニズムを痛覚システムから紐解ける可能性があるのではないだろうか.また,慢性疼痛においては,神経系の多くの領域で可塑的変化が起こり,それが脳機能障害を招き,さらにその固定化で全身に及ぶ二次的影響に波及し,それが痛みをさらに悪化させるという非常に複雑な様相を呈する例が少なくない.加えて,人は五感を通して絶えず外界からの感覚をとり入れているわけだが,五感と痛みの相互作用やその神経科学的メカニズムはほとんど分かっていない.したがって,痛みの慢性化のしくみを多角的に研究することでこれらの課題を解明し,さらに早期的な疼痛治療や新しい介入法を確立することが,慢性的な痛みからの解放に繋がる有効な戦略になるであろうと思われる.
文献
- Dong X & Dong X:Neuron, 98:482-494, 2018
- Melzack R & Wall PD:Science, 150:971-979, 1965
- Koch SC, et al:Annu Rev Physiol, 80:189-217, 2018
- Inoue K & Tsuda M:Nat Rev Neurosci, 19:138-152, 2018
著者プロフィール
津田 誠:1998年星薬科大学大学院博士課程修了,’99年JST特別研究員(国立医薬品食品衛生研究所配属),2002年トロント小児病院博士研究員,’04年厚生労働省入省(国立医薬品食品衛生研究所配属),’05年九州大学大学院薬学研究院助手,’06年助教授(’07年より准教授),’14年より教授.グリア-ニューロン相互作用を切り口にした痛みや痒みなどの体性感覚情報伝達と制御のしくみとその破綻による慢性感覚異常メカニズムに関する研究を行っている.