概論
体内と外界の境界ではたらく粘膜免疫の巧妙なシステム
Mucosal immunity: Complex immune system at the interface between the inside
and outside of the body
鎌田信彦
Nobuhiko Kamada:Laboratory of Microbiology and Immunology, Immunology
Frontier Research Center, Osaka University 1)/Division of
Gastroenterology and Hepatology, Department of Internal Medicine, University
of Michigan Medical
School 2)(大阪大学免疫学フロンティア研究センター免疫微生物学1)/ミシガン大学医学部消化器内科2)
消化管や呼吸器などをはじめとする粘膜組織は体内と外界との境界に位置し,「粘膜免疫」とよばれる全身性免疫とは異なる免疫機構を発達させている.粘膜組織はウイルスなどの感染性微生物の侵入口であると同時に常在微生物叢を有している.すなわち,粘膜免疫は「感染性微生物の排除」と「常在微生物との共生」という相反するタスクを同時に担っており,複雑かつ巧妙なシステムにより制御されていることがうかがい知れる.本稿では,粘膜免疫の組織特異的機能や,生体恒常性維持および生体防御の制御における役割について概説する.
はじめに
鼻咽頭,呼吸器,口腔,胃,腸管などの粘膜組織は生体内部に存在しているにもかかわらず,常に体外環境に晒されている.そのため,粘膜組織は感染性細菌やウイルスなどの病原性微生物の外界からの侵入口となる.粘膜組織では,こういった感染リスクから生体を保護するため,「粘膜免疫」とよばれる全身性免疫とは異なる特殊な免疫系が発達している.粘膜免疫はさまざまな方法で病原体の侵入や増殖を阻止し,また炎症性免疫反応を誘導することで病原体の排除を促進する.同時に,粘膜組織には食事由来の抗原や常在微生物叢など非病原性の環境物質も存在している.これらの抗原は非自己であるものの,生体恒常性に必須の役割を果たしている.当たり前ではあるが,食事由来の栄養素は生体の生命維持に必須である.また,共生微生物は栄養素の消化吸収や病原性微生物に対する競合,粘膜免疫系の発達など多岐にわたる役割を担っている1).そのため,生体はこれらの有益な非自己物質に対しては病原体に対するような炎症性免疫応答を誘導せず,抗炎症的な免疫応答や免疫寛容を誘導し,巧みに共生関係を維持している.このように,粘膜組織では外来物質に対し相反する免疫反応を巧みに使い分け,外来物質との「共生」と「排除」という相反する2つのタスクを同時にこなしながら,外界からの環境刺激に柔軟に対応し,生体恒常性を維持している.しかしながら,この巧妙なバランスが崩れると,生体防御免疫が弱まることで外来微生物への感染リスクが高まったり,本来共生するはずの常在細菌や食事性抗原などに対して強い免疫反応を引き起こし,炎症性腸疾患や食物アレルギーなどの疾患の発症につながる.本特集では,生体防御,恒常性維持に必須の役割を果たす粘膜免疫の理解を深めるため,世界をリードする粘膜免疫研究者による最新の知見を紹介する.
1粘膜免疫組織の構造
前述のように,粘膜組織は外来異物に対する生体防御の最前線に位置している.そのため,粘膜組織ではさまざまな機能を駆使し,外来異物の体内への侵入を防いでいる.粘膜臓器の管腔面は上皮細胞に覆われており,管腔側(体外)と粘膜固有層(体内)を物理的に隔てている.上皮細胞は物理的なバリアとしてだけでなく,抗菌物質や粘液などの分泌を介して,化学的バリアとして外来の感染性微生物や常在共生微生物の侵入を防いでいる2).一方で,上皮細胞は水分や電解質,栄養素などを吸収する生理的役割も同時に有している.また,上皮細胞は体外からのシグナルを粘膜固有層などに存在する免疫細胞や神経細胞に伝達するシグナルハブとしての役割も担っている.興味深いことに,上皮細胞は外来抗原の無秩序な侵入を阻止する一方,適切な免疫応答を誘導するために,小腸パイエル板などのリンパ濾胞を覆う濾胞関連上皮に存在するmicrofold(M)細胞から一部の抗原を取り込み,粘膜固有層の免疫細胞へと受け渡している.上皮細胞により隔てられた粘膜固有層にはIL-22を分泌する3型自然リンパ球や,Th17細胞,制御性T細胞など多種多様な免疫細胞が存在している.また,免疫グロブリンは感染防御に重要な役割を果たしていることが知られているが,粘膜組織には分泌型IgA抗体を産生するB細胞が多く存在している.分泌型IgA抗体は上皮基底膜から取り込まれて粘膜面へと分泌され,感染防御や常在細菌の制御にかかわる1).これら免疫細胞の粘膜組織における役割や常在微生物による分化制御などの詳細は各論でも触れるため,ここでは割愛する.
2粘膜免疫の部位特異性
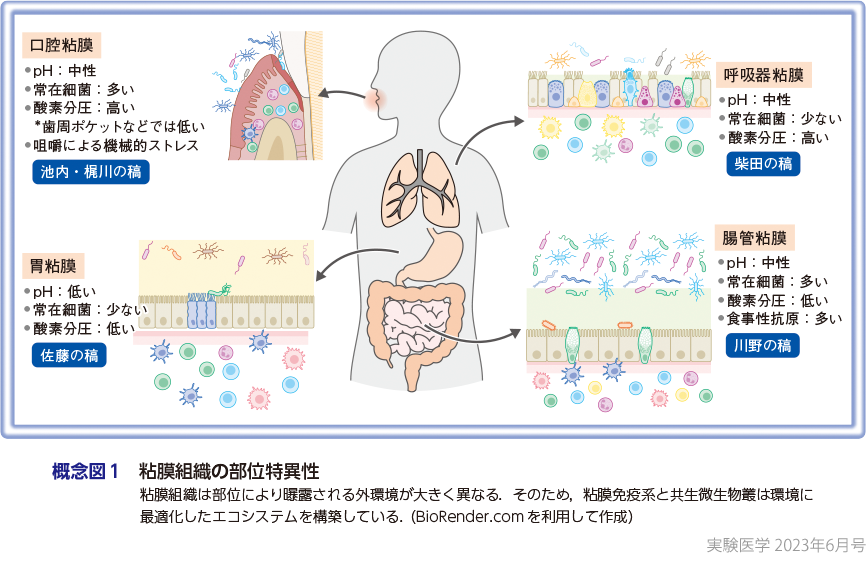
ここまで “粘膜組織” と一括りにして説明してきたが,粘膜組織は体内のさまざまな部位に分布しており,それぞれの粘膜組織を取り巻く外環境は当然異なる.例えば,常在細菌や食事由来物質などの常在抗原の種類や量は粘膜の部位によって大きく異なる3)4).また,酸性度や酸素分圧などの環境も部位ごとに大きく異なっている.他にも,口腔粘膜では咀嚼による機械的な刺激が免疫細胞の分化調節にかかわるなど,多様な組織特異的免疫制御因子が報告されている5).こういった外環境の違いが,部位特異的な粘膜免疫の発達に寄与することは想像に難くない.実際に,近年の単一免疫細胞解析技術の進歩により,さまざまな組織で詳細な免疫細胞の解析が行われ,それぞれの粘膜組織に特異的な免疫細胞の構成や機能が同定されてきている6)7).最近では,単一免疫細胞解析に加え空間的遺伝子発現解析技術も格段に進歩しており,それぞれの粘膜組織における形態学的情報を合わせた免疫機能解析が進むことも期待される.多くの病原体において,その感染(侵入)は特異的な粘膜部位からであることはよく知られている.そのため,部位特異的な粘膜免疫の最適化は生体防御において重要な役割を果たしていると考えられる.また,炎症性腸疾患などの臓器特異的な自己免疫性炎症性疾患の病態理解・治療法開発にも部位特異的な粘膜免疫の制御機構を明らかにすることは重要であると考えられる(概念図1).本特集では,最も研究が進んでいる腸管粘膜(川野の稿)に加え,口腔粘膜(池内・梶川の稿),胃粘膜(佐藤の稿),呼吸器粘膜(柴田の稿)などにおける部位特異的な免疫制御について解説いただく.
3異所粘膜組織間ネットワーク
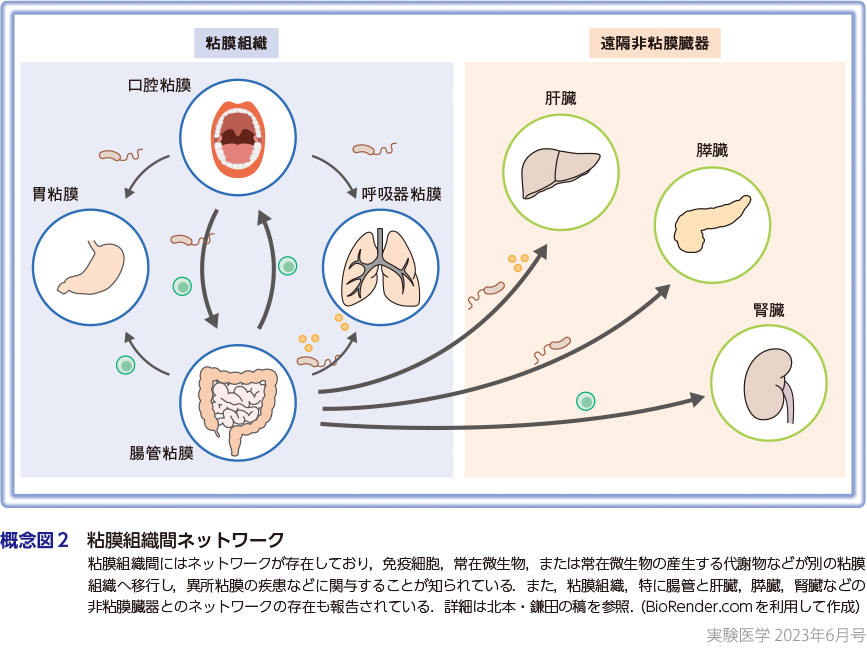
前項で述べたように,それぞれの粘膜組織には部位特異的な免疫系と微生物叢が発達しており,固有の共生エコシステムが確立されている.一方で,異所粘膜組織間には粘膜免疫・常在微生物を介したネットワークが存在していることも明らかになってきた.例えば,腸管粘膜組織で分化誘導された免疫細胞や常在細菌代謝物が,さまざまな遠隔臓器(口腔や呼吸器といった異所粘膜組織,ならびに肝臓,膵臓,腎臓などの非粘膜臓器)へ移動し,異所での炎症誘導などに関与することが報告されている(北本・鎌田の稿).他にも,口腔粘膜常在細菌や口腔粘膜で分化誘導された炎症性免疫細胞が腸管粘膜へ移行し,炎症性腸疾患や大腸がんなどの病態に寄与していることも明らかとなってきた(北本・鎌田の稿).このように,臓器連関・粘膜組織連関はさまざまな疾患病態に関与していることがわかってきた.一方で,臓器連関・粘膜組織連関は病態形成のみに関与しているのか,生体恒常性にも寄与しているのかは解明されておらず,今後さらなる研究が必要である(概念図2).
4粘膜免疫を制御し,疾患を防ぐ
このように粘膜免疫は生体防御,恒常性維持に必須の役割を担っている.そのため,粘膜免疫を適切に制御することで,われわれはさまざまな疾患に対し立ち向かうことができると考えられる.最もわかりやすい例としては,粘膜免疫の強化による感染防御である.前述のように,粘膜組織はさまざまな病原体の侵入口であるため,粘膜組織に適切な免疫応答を誘導することで,病原体感染を防ぐ,もしくはすみやかな排除を促すことができる.近年,新型コロナウイルスを含むさまざまな病原体に対する粘膜ワクチンの開発が進められており,注目を集めている(森山・岩崎の稿).また,粘膜免疫の調節因子としての「食事」も注目されている.例えば,食事に含まれる脂肪やショ糖などが直接,あるいは腸内細菌への影響を介して腸管粘膜免疫のバランスを破綻させ,炎症性免疫優位な状態へシフトさせることが報告されている.腸管粘膜免疫の炎症性シフトは肥満や糖尿病などの代謝性疾患のリスクを高める(川野の稿).逆に,食物繊維や発酵食品などは腸内細菌や腸管粘膜免疫のバランスを改善し,代謝性疾患や炎症性疾患のリスク低下や病原菌感染防御能を上昇させることも知られている8).また,前述の粘膜臓器間のネットワークを利用し,例えば腸管の粘膜免疫を調節することで,異所粘膜や非粘膜遠隔臓器における疾患を予防・治療することも可能になるかもしれない.
おわりに
近年の単一細胞免疫機能解析技術や細菌叢解析技術の飛躍的な進歩により,組織特異的な粘膜免疫-共生微生物エコシステムをより深いレベルで “見る” ことが可能なった.次の課題として,この情報をもとに粘膜免疫を “操る” ことができれば,新型コロナウイルスなどの新興感染症の制圧や,生活習慣病やアレルギー,自己免疫性炎症性疾患の予防などへ一歩近づくことが期待される.
文献
- Kamada N, et al:Nat Rev Immunol, 13:321-335, doi:10.1038/nri3430(2013)
- Odenwald MA & Turner JR:Nat Rev Gastroenterol Hepatol, 14:9-21, doi:10.1038/nrgastro.2016.169(2017)
- The Human Microbiome Project Consortium:Nature, 486:207-214, doi:10.1038/nature11234(2012)
- Lloyd-Price J, et al:Nature, 550:61-66, doi:10.1038/nature23889(2017)
- Dutzan N, et al:Immunity, 46:133-147, doi:10.1016/j.immuni.2016.12.010(2017)
- Williams DW, et al:Cell, 184:090-4104.e15, doi:10.1016/j.cell.2021.05.013(2021)
- Domínguez Conde C, et al:Science, 376:eabl5197, doi:10.1126/science.abl5197(2022)
- Desai MS, et al:Cell, 167:1339-1353.e21, doi:10.1016/j.cell.2016.10.043(2016)
本記事のDOI:10.18958/7281-00001-0000481-00
著者プロフィール
鎌田信彦:2007年慶應義塾大学にて博士号(医学)取得.’07年より慶應義塾大学医学部内科学(消化器)助教.’09年よりミシガン大学医学部病理学 Research Fellow.’13年より同大学内科学(消化器)Assistant Professor.’20年より同Associate Professor(with Tenure).’21年より大阪大学免疫学フロンティア研究センター特任教授(クロスアポイントメント).研究テーマは炎症性腸疾患,大腸がんなどの消化管疾患における宿主免疫と共生細菌の役割.













