概論
新しいがん研究領域としてのRNAスプライシング異常
Aberrant RNA splicing in cancer -A new area in cancer research-
吉見昭秀
Akihide Yoshimi:Division of Cancer RNA Research, National Cancer Center
Research Institute(国立がん研究センター研究所がんRNA研究分野)
がんにおけるRNAスプライシング異常の研究は,最近10年ほどで活発になってきた,がん研究のなかでも比較的新しい分野である.本特集では,スプライシング異常ががんの病態形成にどのようにかかわり,またスプライシング異常をどのように治療標的として狙い得るのか,という点に焦点を絞り,基礎研究から臨床試験まで,研究・開発に取り組み活躍されている研究者に,最近の知見の概説と新しい研究成果について寄稿をご依頼した.この研究分野に関する研究の潮流や最近の動向について,大まかに把握していただけると幸いである.
はじめに
RNAスプライシングとは,ゲノムDNAから転写されたメッセンジャーRNA(mRNA)前駆体(pre-mRNA)からイントロン配列を除去し,エキソン配列同士をつなぎ合わせるプロセスを指す.遺伝子異常を起点とするがんのスプライシング異常は,シス制御配列の異常によるものとトランス制御因子の異常によるものに大別され,有望とされる治療戦略も両者により異なる.本特集ではこの両者について取り上げるが,本概論では,各論同士をつなぎ,全体の理解が進む手助けとなるように心がけつつ,がんのスプライシング異常を起点とした病態と治療について俯瞰したい.
1RNAスプライシングのしくみ
RNAスプライシングは非常に精緻なシステムによってなされる.この際にsnRNA(small nuclear RNA)とタンパク質からなる複数のsnRNP(small nuclear ribonucleoprotein)がpre-mRNA上のエキソン-イントロン構造を認識して,イントロンの除去とエキソン同士の再結合を行う1).スプライシングの機序は複雑であるが,5′側スプライシング部位(5′splice site)をU1 snRNPが,U2AFヘテロ二量体を含むタンパク質複合体が3′側スプライシング部位(3′splice site),ポリピリミジン領域(poly-Y tract)を認識し,その後分岐点配列(BPS:branch point sequence)を介してSF3B1を含むU2 snRNP複合体がリクルートされて,2回のエステル基転移反応によってイントロンが除去される(図1A).このような目印となるような配列はコンセンサス配列とよばれ,特に哺乳類のほとんどのイントロンの配列はGU(一部はGC)ではじまり,AGで終わる(メジャーイントロンあるいはU2型イントロンとよばれる).一方,一部にAUではじまりACで終わるマイナーイントロン(U12型イントロン)が存在し,ヒトではイントロン全体の約0.1%を占める.最近になって,メジャーイントロンだけでなく,マイナーイントロンの制御異常も発がんにかかわることがわかってきた(雜賀・井上の稿).
また,前述のコンセンサス配列以外にも,エキソンやイントロンの包含について正・負に働く「シス配列」が存在する.これらは位置と働きに応じて,ESE/ESS(exonic splicing enhancer/silencer),ISE/ISS(intronic splicing enhancer/silencer)とよばれる.一般的に,SRタンパク質群はESEやISEに結合してエキソンの包含(exon inclusion)に働き,一方でhnRNP群がESSやISSに結合してスプライシングを抑制するとされる(図1B).
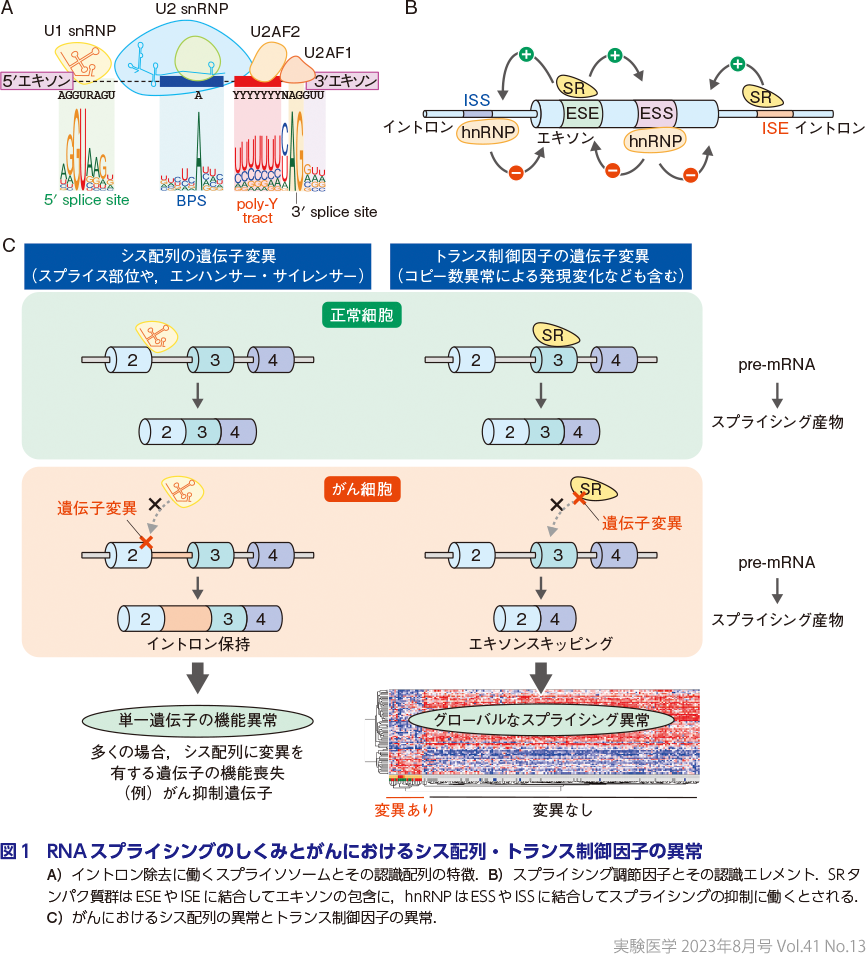
2がんにおけるシス配列の異常とトランス制御因子の異常
がんにおけるRNAスプライシング異常は,その原因としてシス配列(スプライシングされる側の遺伝子)の異常とトランス制御因子(スプライシングする側の因子)の異常に大別される(図1C).個々の遺伝子のスプライシング変化と発がんの関係については古くから研究がされてきたが,これらはいずれも個々の遺伝子やスプライシング因子に注目したものであった.例えば,シス配列の異常としては,肺腺がんのおよそ3~4%を占めるMET遺伝子のエキソン14スキッピングが報告されており,エキソン14の脱落によりユビキチンによる分解が抑制されることで,MET活性が亢進することが示されている2).トランス制御因子の異常では,SRタンパク質群がその代表例であり,例えばSRSF1,SRSF3遺伝子のコピー数増加と過剰発現による発がん作用が示され3)4),SRSF6遺伝子についても過形成誘導によるがん病態への寄与が示唆されている.
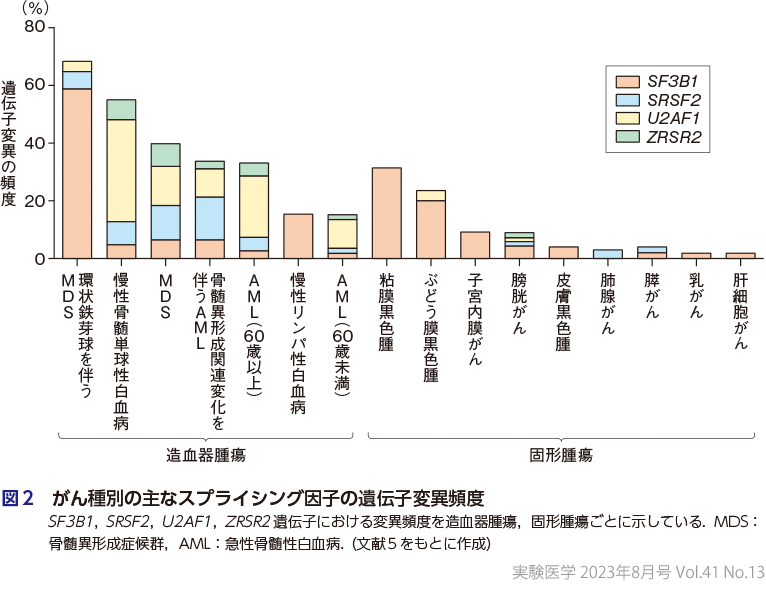
一方,次世代シークエンサー(NGS)の登場によって,がん細胞におけるスプライシング制御異常の理解は飛躍的に進んだ.NGSの活用により,網羅的ゲノム解析が可能になり,スプライシング因子(SF:splicing factor)における遺伝子変異(SF変異),すなわちトランス制御因子の異常がさまざまながんで高頻度に生じていることが発見されたこと,RNAシークエンス(RNA-seq)によってゲノムワイドにスプライシング解析が可能となったこと,さらにexomeシークエンスとRNA-seqの組み合わせあるいはRNA-seq単独のデータに基づいて,スプライシング異常を誘導するシス配列の変異を網羅的に同定できるようになったこと(飯田らの稿)などが,その大きな要因である.2011年に,ゲノム解析の結果として,骨髄異形成症候群検体の変異解析からスプライシング因子をコードするSF3B1,SRSF2,U2AF1,ZRSR2の4遺伝子を中心に変異が発見された(図2)6)(昆の稿).その後,こうしたSF変異は造血器腫瘍にとどまらず,さまざまな固形腫瘍にも同定されることがわかってきた(西村の稿).SF3B1,SRSF2,U2AF1の3遺伝子は主にエキソンあるいはメジャーイントロンのスプライシングにかかわり,またいずれの遺伝子変異もホットスポット※を形成する.また,これらの遺伝子変異は,相互排他的かつヘテロな変異であることから,機能変化型の遺伝子変異と考えられる7)8).一方,ZRSR2遺伝子はマイナーイントロンのスプライシングにかかわり,機能喪失型の遺伝子変異である.
3スプライシング異常を標的としたがん治療法
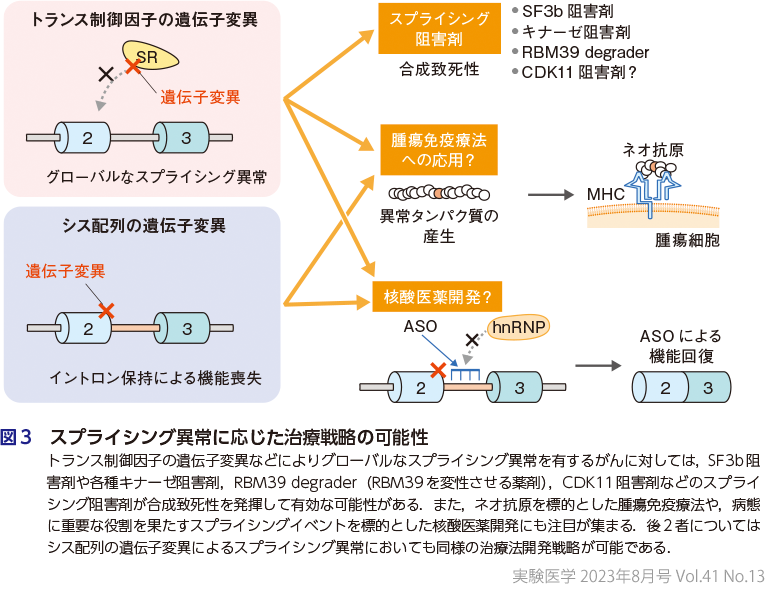
がんにおけるスプライシング異常を標的とした治療についても,シス配列,トランス制御因子の異常に大別すると捉えやすい.とはいうものの,執筆時点でスプライシング異常を標的として承認された治療法はなく,基礎的検討段階のものから臨床試験中のものまで,いずれも開発途上の治療コンセプトであることにご留意いただきたい.本項では,そのなかからいくつかの治療アプローチについてご紹介したい(図3)(Leeの稿).
❶ スプライシング阻害剤
SF変異は相互排他的かつヘテロな変異として検出される.このことは,複数の変異がスプライソソームに生じると細胞の生存が困難であることを示唆する.実際に,Sf3b1K700EとSrsf2P95Hの両変異を有する条件的ノックインマウスモデルにおいては著しい骨髄再構築能の低下が認められた9).すなわち,SF変異を有するがん細胞の生存は野生型SFに依存しており,合成致死性を有すると考えられる.以上の観察結果から,SF変異を有するがんに対しては,スプライシング阻害剤を用いて残存する野生型SFの機能を阻害することによって合成致死を誘導する治療法の開発が進んでいる.スプライシング阻害剤の作用機序としては,主にコアスプライソソームを標的とするものと,スプライシング調整タンパク質を標的とするものに大別される.SF3b阻害剤は前者の代表例であり,Pladienolide誘導体であるE7107やそのアナログであるH3B-8800は,U2 snRNPとpre-mRNAの結合を阻害してスプライシングを抑制する10).骨髄性腫瘍患者を対象としたH3B-8800の第Ⅰ相試験が実施され,その結果が最近報告されたところである11).一方,スプライシング調整タンパク質を標的とする阻害剤として,CLKやSPRKなどのSRSF2キナーゼやDYRKなどのSF3B1キナーゼを標的としたものがあげられる.これらのキナーゼによるスプライシング調整タンパク質のリン酸化は,スプライシングの制御に重要であると考えられている12).これらのキナーゼ阻害剤の開発が進んでおり,特に最近ではCLK阻害薬であるCTX-712について国内で臨床試験が進んでおり,今後,CLK阻害剤を含むスプライシング調整タンパク質を標的とする阻害剤の開発が進むと思われる(森下の稿).また,RBM39をDCAF15と結合させる分子糊として働くIndisulam(その結果RBM39がユビキチン化され,変性する)13)14)や,CDK11に対する阻害剤15)もスプライシング阻害剤として開発が進む可能性がある.
❷ 核酸医薬のがん治療への応用の可能性
近年,さまざまな疾患に対して核酸医薬を用いた治療開発が活発に行われている.その一部はすでに上市されており,COVID-19のmRNAワクチンは最も身近な一例と言える.また,これまでに有効な治療法に乏しかった脊髄性筋萎縮症や筋萎縮性側索硬化症などの神経変性疾患に対して核酸医薬は劇的な効果を示している.一方,がん領域ではこれまでに承認された核酸医薬は存在しないものの,多数の臨床試験が実施され,その有効性が証明されつつある.核酸医薬は,その構造や作用機序により分類され,アンチセンスオリゴヌクレオチド(ASO),siRNA,microRNA,アプタマー,デコイなどがあげられる.なかでも,ASOはがん領域で最も開発が進んでおり,シス配列の変異によるスプライシング異常に対するASOの開発が期待されている.同時に,トランス制御因子の異常により生じたグローバルなスプライシング異常の一部には,発がんに寄与する重要なイベントが含まれていると考えられ,特定のスプライシングイベントを標的とした核酸医薬の開発にも期待がかかる.
❸ がん免疫治療法への応用の可能性
がん細胞が生体内の免疫監視機構により認識・排除されるプロセスががん免疫応答であり,そのしくみを活用したがん免疫治療法が確立されてきた.がん細胞で特異的に産生されるタンパク質は,がん免疫療法の標的ネオ抗原の候補となることから,がんにおけるスプライシング機構の異常や,スプライシングに影響を及ぼす薬剤は,ネオ抗原産生の源とも考えられ,最近注目が集まりつつある研究領域である(網代の稿).
おわりに
がん横断的なスプライシング解析により,SF変異を有するがんはもちろんのこと,SF変異のないがんにおいても明確なスプライシング変化が起きていることがわかってきた.このことからも,スプライシング異常は,従来考えられていた以上に,がんに普遍的な現象であることが示唆される.その分子病態の理解は依然として不十分であり,臨床実装につながるような創薬開発もはじまったばかりである.今後,スプライシング異常という新しいがんの切り口から当該分野の研究が発展し,がん診療に資する成果へとつながることを切に願う.
文献
- Yoshimi A & Abdel-Wahab O:Clin Cancer Res, 23:336-341, doi:10.1158/1078-0432.CCR-16-0131(2017)
- Paik PK, et al:N Engl J Med, 383:931-943, doi:10.1056/NEJMoa2004407(2020)
- Ajiro M, et al:Nucleic Acids Res, 44:1854-1870, doi:10.1093/nar/gkv1500(2016)
- Karni R, et al:Nat Struct Mol Biol, 14:185-193, doi:10.1038/nsmb1209(2007)
- 「mRNAの制御機構の解明と治療薬・ワクチンへの活用」(横田隆徳,他/著),技術情報協会,2023
- Yoshida K, et al:Nature, 478:64-69, doi:10.1038/nature10496(2011)
- Liu Z, et al:Cancer Discov, 10:806-821, doi:10.1158/2159-8290.CD-19-1330(2020)
- Yoshimi A, et al:Nature, 574:273-277, doi:10.1038/s41586-019-1618-0(2019)
- Lee SC, et al:Cancer Cell, 34:225-241.e8, doi:10.1016/j.ccell.2018.07.003(2018)
- Seiler M, et al:Nat Med, 24:497-504, doi:10.1038/nm.4493(2018)
- Steensma DP, et al:Leukemia, 35:3542-3550, doi:10.1038/s41375-021-01328-9(2021)
- Prasad J, et al:Mol Cell Biol, 19:6991-7000, doi:10.1128/MCB.19.10.6991(1999)
- Han T, et al:Science, 356:eaal3755, doi:10.1126/science.aal3755(2017)
- Uehara T, et al:Nat Chem Biol, 13:675-680, doi:10.1038/nchembio.2363(2017)
- Hluchý M, et al:Nature, 609:829-834, doi:10.1038/s41586-022-05204-z(2022)
本記事のDOI:10.18958/7309-00001-0000536-00
著者プロフィール
吉見昭秀:2003年3月東京大学医学部医学科卒業.’11年東京大学大学院医学系研究科修了,博士(医学)取得.東京大学医学部附属病院無菌治療部助教を経て’15年Memorial Sloan Kettering Cancer Centerに留学.以降がんにおけるスプライシング異常の研究に携わる.’20年帰国と同時に独立し,’22年9月より現職.スプライシング異常を中心に据えつつ,さまざまな観点からがん創薬に取り組んでいる.

がん以外でのスプライシングも大変なことに!?











