概論
現代の創薬における抗体医薬の位置づけ
Current status of antibody therapy in the drug development
津本浩平
Kouhei Tsumoto:School of Engineering, The University of Tokyo/Institute of Medical Science, The University of Tokyo(東京大学大学院工学系研究科/東京大学医科学研究所)
ゲノム創薬の成果の一つが抗体医薬といっても過言ではない.2,000にものぼる候補品の提案はその最たる証拠であろう.標的枯渇,医療経済における問題など,解決すべき課題は多いものの,ターゲットバリデーションに基づく新薬開発,革新的分子設計,細胞療法や免疫療法を強力にサポートする分子設計など,抗体医薬が今後も拡大の一途をたどることは想像に難くない.本特集では,このような背景のもと,今再び盛り上がる抗体創薬について最先端の状況をまとめ,今後を議論したい.
はじめに
ここ数年来,製薬業界で,モダリティという言葉を耳にする機会が多く,モダリティ研究所という名称の研究所をもつ企業も増えている.モダリティとは,創薬においては,いわゆる低分子化合物,ペプチドなどの中分子薬から,抗体医薬を含むタンパク質医薬,核酸医薬,細胞医薬,再生医療といった治療のための手段を意味する.よく知られているように,最近に至るまで,低分子化合物をその開発対象とする創薬がほとんどであった.しかしながら,近年では,抗体医薬を中心としたタンパク質医薬,さらに最近では,核酸医薬,細胞医薬,再生医療のモダリティとしての研究開発がさかんになっている.治療対象に対する創薬モダリティの選択肢が増えた,ということができる.
創薬モダリティとしての抗体は,バイオ医薬品のなかでも,現時点で最も実績のある形態の一つである.その高い治療効果から幅広く適用されつつあるものの,例えば高額な薬価による医療経済の圧迫のように,問題点も多く指摘されている.しかしながら,ターゲットバリデーションによる新たな標的の提案,抗体分子に関する物質科学としての精緻な分析といわゆる作りこみから,その次世代医薬品開発への具体的展開,臨床サンプルの精査が導く個別化医療への展開と新たな標的の発見,そして情報科学の積極的取り込みによる人工抗体の設計など,抗体医薬をとり巻く状況は,今まさに新しい段階を迎えている.産業界とアカデミア,さらには医療機関が完全に連携した研究体制の構築の必要性が声高に叫ばれているのも,このような研究開発が全世界的に展開されつつあることによる.
1各種イノベーションと抗体工学の発展
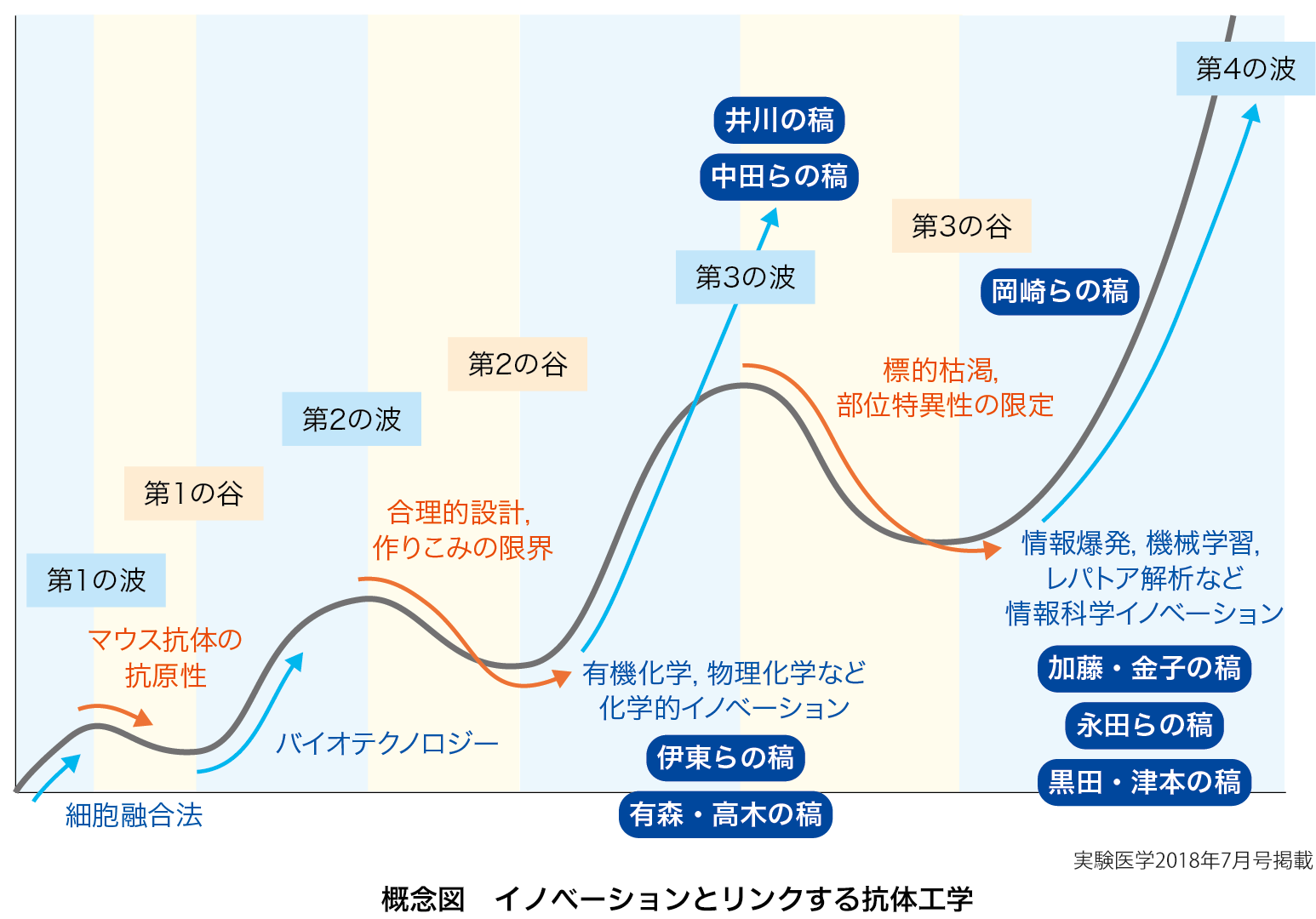
抗体医薬品開発は,時代の最先端イノベーションを積極的にとり入れて発展してきた,ということができる.その流れには,大きく以下のような波(山といってもよいが)と谷があった,とまとめることができる(概念図).
第1の波:イノベーションとして細胞融合法があり,マウスモノクローナル抗体産生細胞の樹立が可能になった.
第1の谷:マウス抗体の抗原性により治療抗体が自在には作製できなかった.
第2の波:イノベーションとしてバイオテクノロジーがあり,ヒト化抗体,ヒト抗体設計と組換えタンパク質としての発現が可能になった.例えば,ヒューミラ,ハーセプチン,リツキサン等が上市された.
第2の谷:例えば合理的設計が困難であった.成熟度が不十分なものも多く,上市される分子種に限りがあった.
第3の波:イノベーションとして有機化学,物理化学など化学的知見の取り込みがある.これによって,drug conjugation,親和性向上,物性,特に会合凝集体形成に関する分析が可能になり,いわゆるバイオベター(従来品から物性を改良),バイオスペリア(従来品に高機能を付加)とよばれる分子種が提案されるようになった.二重特異性(バイスペシフィック)抗体など高機能化抗体の構築が現実のものとなった.
第3の谷:抗体医薬品開発における標的の枯渇,実験動物などから創出される抗体分子の標的部位特異性の限定が,モダリティとしての可能性を制限した.
第4の波:イノベーションとして情報科学の取り込みがある.標的分子と抗体分子に関する情報爆発,機械学習,レパトア解析から
2本特集の各論の位置づけ
本特集では,これらのイノベーションをフルに活かした医薬品開発とその周辺に関して最近の状況をまとめていただいている.
まず,第3の波で大きな進展を遂げたのが,血友病治療に劇的な進展をもたらし,世界的にきわめて高い評価を受けている,中外製薬の二重特異性抗体の上市であろう(井川の稿).技術的に常に最先端にあるグループが,質的にも量的にも他を圧倒する研究成果に基づいて完成されたものである.二重特異性抗体に関する設計概念は,治療薬開発を志す抗体工学者は皆が考えてきたことであり,30年前に抗体のドメインレベルでの工学が可能になってからはその概念提唱がさかんにおこなわれた.すでに上市されているBiTEはその成功例の一つである.そのようななか,井川らは難しいとされていた技術を見事に確立させ,血友病の有力な治療薬を上市するに至った.技術を不断に高めるのは前提で,むしろ治療という観点で患者様目線での分子の作りこみを常に意識すべき,という内容は,技術を世界最先端に高めている井川らの成功に基づくもので,強い説得力がある.
もともと抗体は,第1の波の頃からいわゆるミサイル療法への展開を大きく期待されたモダリティであった.直接標的を捕捉するモダリティとしては今なお最も優れたものであることは,改めて指摘しておくべきだろう.しかしながら,例えば,drug deliveryへの応用が期待されていたにもかかわらず,薬剤結合に関する化学,薬剤を結合させた抗体分子の安定性,抗体一分子あたりの薬剤結合数の制御,など,主に物質科学的な問題を抱え,わずかな成功例を見るに過ぎなかった.第一三共の我妻らは,薬剤と抗体の間のリンカーの作りこみ,抗体の物性制御を強く意識した結合様式に関する技術革新を与え,antibody drug conjugation(抗体-薬物複合体,ADC)の位置づけを大幅に高めるに至っている(中田らの稿).これも第3の波における化学的イノベーションがもたらした福音ということができる.戦略は異なるが,Fc領域特異的なペプチドを用いた部位特異的修飾技術も,さまざまな応用を期待させる新しい分子設計である(伊東らの稿).その作りこみは,さすがタンパク質化学研究者,と驚嘆する内容が含まれている.drug conjugationの一つのフォーマットとして,今後の適用例の拡大を期待したいところである.
一方,第3の谷を大きく克服し,賛否両論であったがん免疫療法に標準的位置づけを与えた抗体医薬研究として,PD-1特異的抗体の医薬品開発としての成功(岡崎らの稿)を挙げることができる.CD28など同様な機能を有する分子への関心は高かったものの,いわゆるアゴニスト抗体の劇的な副作用が,抗体医薬研究者の関心を遠のかせていたのは事実である.そのようななか,がん細胞に対する免疫寛容に着目し,免疫チェックポイントそのものを標的とする治療薬開発は,まさにイノベーションの真骨頂というべきものである.標的の枯渇,という第3の谷を克服するに十分な成功例といえるだろう.作用機序の解明が,この領域をさらに拡大させるものと期待させる.
抗体の分子フォーマットそのものを改変し,新しい形態を提案する試みは,可変領域(Fv)のとり出しにはじまる.可変領域間相互作用が抗原特異性・親和性創出に決定的な役割を果たすことは,私自身の抗体工学研究でも長く経験してきたことであり,ヒト化による抗原親和性低下や部位特異的変異導入効果の熱力学的相殺のほとんどは,可変領域間相互作用の変化によるものであった.この弱いながらも重要な相互作用を制御するために,一本鎖抗体(single-chain Fv,scFv)やジスルフィド安定化抗体(dsFv)の構築が提案されてきた.しかしながらこれらの人工形態は,想像以上に精緻な理解と分子としての作りこみが必要であり,今なお多くの工学研究者の研究対象となっている.そのようななか,Fv分子としての有用性を最大限に高めうる技術が高木らによって開発されたFv-claspである(有森・高木の稿).モダリティとしてのFv領域の利用に大きな期待がかかる分子形態である.
第3の谷を越えるイノベーションがほかにも現れてきている.細胞外分子あるいは細胞表面分子をその標的とする限り,糖鎖修飾をどう克服するかは避けて通ることのできない課題である.例えばがん細胞表面特異的な糖鎖,糖鎖不全などは以前から指摘されてきたことであるが,バイオテクノロジーのイノベーションにも限界があり,若干の閉塞感があった.それを,ゲノム編集技術などの導入により打開し新しい局面を迎えさせたのが,CasMab法の提案(加藤・金子の稿)である.抗体産生細胞の整備と精緻な機能評価により,糖鎖は回避するべきものでなく,むしろ積極的に取り組むべき標的になりつつある,といえる.抗体開発研究の経験豊富な加藤による標的枯渇に関する記述は,説得力がある.
また,さまざまな分子種が医薬品候補として提案されるなかで,重要になってきているのが,標的となっている抗原部位,いわゆるエピトープの同定である.ある分子が標的として提案された場合,その分子の徹底的な精査,いわゆるターゲットバリデーションが必須である.エピトープに関する理解を制する者は,抗体医薬品開発を制する,といっても過言ではない.そのようななか,永田,鎌田は,その長年の抗体開発研究にかかわる実績と経験から,エピトープに関する本質的理解が治療薬診断薬開発に決定的な位置づけとなることと考え,その分類に関して,エピトープ均質化抗体パネルという概念を提唱している(永田らの稿).受容体や細胞表面マーカーを標的とした抗体創薬において,標的エピトープ構造の微妙な相違が活性に決定的な役割を果たすことは,よく経験することであるが,彼らのパネルという概念は,そのような問題に決定的な解決策を与えるだけでなく,例えば,最近,医薬基盤・健康・栄養研究所の秋葉らが提案している,抗原の異なる部位を認識して分子内あるいは分子間架橋を可能にする,バイパラトピック二重特異性抗体の作製などに大きな貢献をするはずである.
そして今,第4の波が,第4次産業革命といわれる現代における次世代抗体開発研究にも訪れつつある.1983年にUlmerがScience誌にタンパク質工学という概念を提唱して35年が過ぎた.バイオテクノロジーの劇的な進展によって,当時の研究者が考えていた概念を大幅に超える段階にきているといえるだろう.中村春木(大阪大学蛋白質研究所)らが,先駆的にめざしてきた完全人工合成分子設計(いわゆる
おわりに
本特集でとり上げた内容以外にも,新たな標的に対する創薬,特にタンパク質間相互作用阻害剤にみられるような戦略,抗体医薬品製造に関する連続培養法や精製法におけるイノベーション,溶液・乾燥製剤開発におけるイノベーションなど,抗体医薬品開発研究は,さまざまな分野が真に融合して,日々発展している.他方,各種モダリティとの融合的発展も見逃せない.国の健康・医療戦略においても,重点政策として重要な位置づけにある.低分子・中分子創薬における新しい息吹はすでに見えはじめている.治療手段としての本質を見極めた,かつ真に血の通った次世代創薬への期待も,高まるばかりである.産業界とアカデミア,医療機関が一体となった,基盤技術開発から医療現場までの一気通貫の体制構築が,いよいよ本格化しつつある.
文献
- JST-CRDS「(調査報告書)調査検討報告書 革新的バイオ医薬品/CRDS-FY2013-RR-03」(https://www.jst.go.jp/crds/report/report04/CRDS-FY2013-RR-03.html)
- JST-CRDS「(研究開発の俯瞰報告書)ライフサイエンス・臨床医学分野(2017年)/CRDS-FY2016-FR-06」(https://www.jst.go.jp/crds/report/report02/CRDS-FY2016-FR-06.html)
- Kumagai I, et al:Structural consequences of target epitope-directed functional alteration of an antibody. The case of anti-hen lysozyme antibody, HyHEL-10. J Biol Chem, 278:24929-24936, 2003
- Yumura K, et al:Use of SpyTag/SpyCatcher to construct bispecific antibodies that target two epitopes of a single antigen. J Biochem, 162:203-210, 2017
- Akiba H & Tsumoto K:Thermodynamics of antibody-antigen interaction revealed by mutation analysis of antibody variable regions. J Biochem, 158:1-13, 2015
著者プロフィール
津本浩平:東京大学大学院工学系研究科バイオエンジニアリング専攻 教授,同研究科医療福祉工学開発評価研究センター センター長,東京大学医科学研究所兼務.博士(工学).1991年東京大学工学部工業化学科卒業,’95年東北大学大学院工学研究科助手,同講師,助教授,2005年東京大学大学院新領域創成科学研究科准教授を経て,’10年より東京大学医科学研究所疾患プロテオミクスラボラトリー教授.’13年より現職.専門は分子医工学,タンパク質工学,生命物理化学.自在にタンパク質分子を設計できるようになるのが当面の夢ですが,現実味を帯びてきました.











