概論
リピート病研究の新展開
Expanding the repeat expansion disease world
永井義隆
Yoshitaka Nagai : Department of Neurotherapeutics, Osaka University of Graduate School of Medicine(大阪大学大学院医学系研究科神経難病認知症探索治療学)
リピート病は,遺伝子翻訳領域のリピート配列の異常伸長を原因とするポリグルタミン病などいわゆるコーディングリピート病を中核に研究が進展してきた.ポリグルタミン鎖の異常伸長によるタンパク質ミスフォールディング・凝集を介した病態メカニズムが明らかにされ,タンパク質凝集阻害薬,核酸医薬などの治療法開発研究が進んでいる.一方,ノンコーディングリピート病では,従来からのRNA毒性の研究に加えて,最近新規のRAN翻訳機構が発見され,新たな病態メカニズム研究が展開されている.また,最近のロングリードシークエンス技術により遺伝子非翻訳領域内のリピート伸長変異が次々に発見され,疾患概念が拡大している.本特集では,リピート病研究の新展開について,RAN翻訳を中心に,最近話題の非古典的翻訳,液-液相分離との関連にも触れて,最新の研究を紹介する.
はじめに
リピート病とは,遺伝子内のリピート配列の異常伸長変異を原因とする疾患群の総称である.1991年に,脆弱X症候群(fragile X syndrome,FXS)の原因遺伝子変異としてFMR1(FMRP translational regulator 1)遺伝子内のCGGリピート配列の異常伸長が発見され1),続いて球脊髄性筋萎縮症(spinal-bulbar spinobulbar muscular atrophy,SBMA)においてアンドロゲン受容体遺伝子内のCAGリピート配列の異常伸長変異が発見された2).後者のSBMAでのCAGリピート伸長変異を発見したFischbeck博士によると,健常人においても多型性を認めるリピート配列の単純な伸長が疾患の原因となることは当時はなかなか信じてもらえずに,論文は先に投稿したが論文発表はFXSの後塵を拝したという.それ以来,このようなリピート配列の異常伸長変異を原因とするリピート病は,現時点で30以上の疾患が発見されており,多くが神経・筋疾患である(表1,2)3)4).
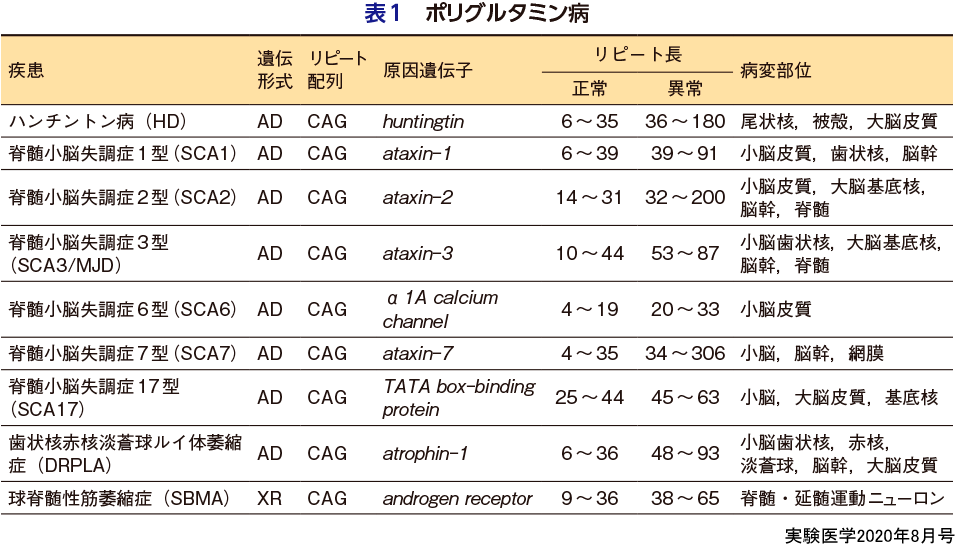
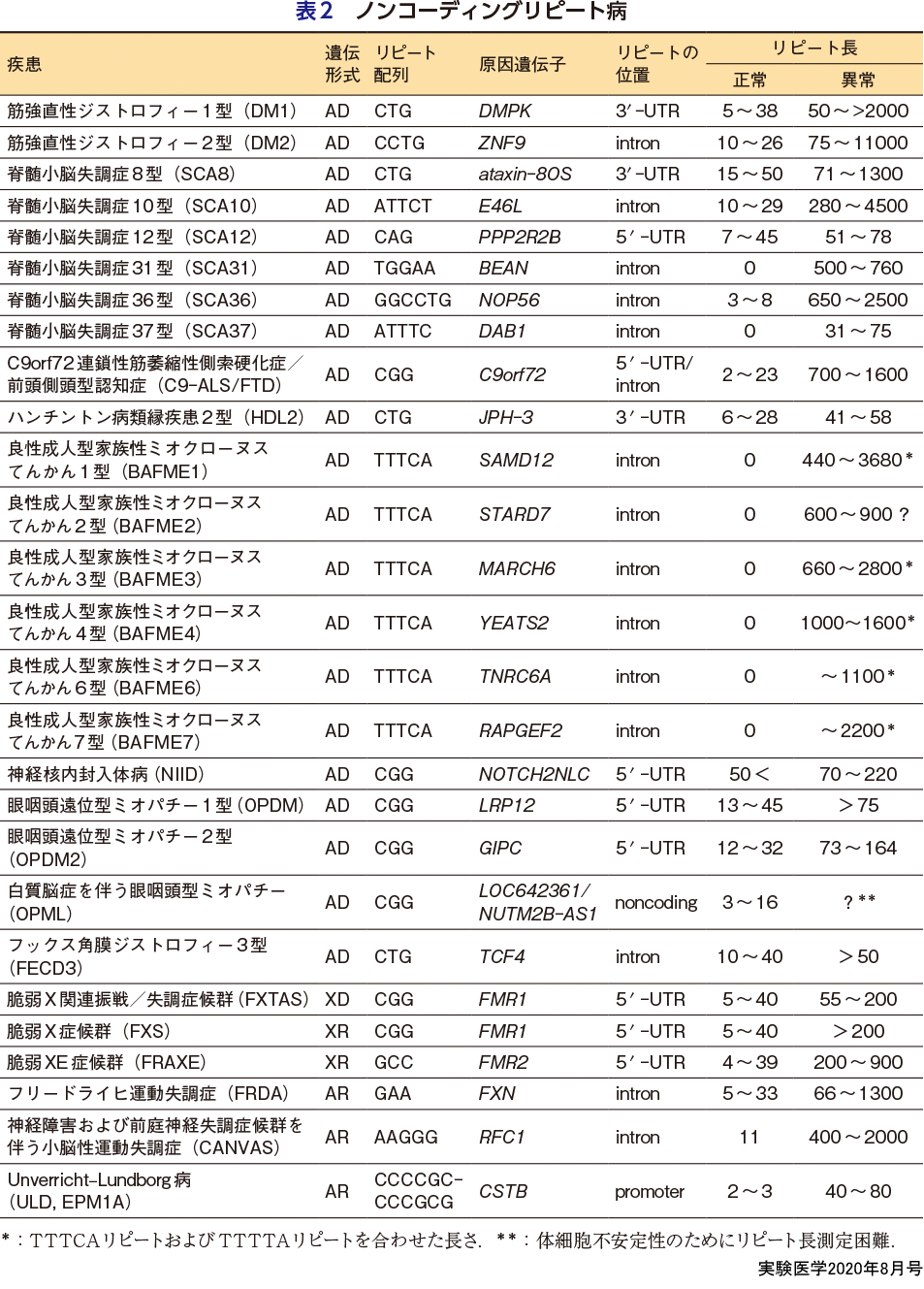
リピート病は,リピート配列の遺伝子内の位置により大きく2つの群に分類される.1つは,リピート配列が遺伝子翻訳領域内にある疾患群で,後述するポリグルタミン病,ポリアラニン病が含まれる.もう1つは,リピート配列が遺伝子非翻訳領域内にある疾患群で,ノンコーディングリピート病ともよばれている.前者のコーディングリピート病では,変異遺伝子から翻訳される異常伸長ポリグルタミン(polyQ)鎖をもつ変異タンパク質による病態メカニズムの解明,治療法の開発を中心に研究が進展してきた.一方,ノンコーディングリピート病においては,当然伸長リピート配列は翻訳されないと考えられていたため,これまで異常伸長リピート配列を含む変異RNAによる病態メカニズムの研究がメインであった.しかし最近,異常伸長リピートRNAは開始コドンATGをもたないにもかかわらず,これらを鋳型としてリピート関連非ATG依存性(repeat-associated non-ATG,RAN)翻訳※1によりペプチドが翻訳されることが発見され,翻訳されたリピートペプチドによるノンコーディングリピート病の新たな病態メカニズムが明らかになりつつある.そしてRAN翻訳の発見をきっかけに,それぞれタンパク質毒性,RNA毒性を中心に別々に研究されてきたコーディングリピート病とノンコーディングリピート病とが再び出会い,共通の病態メカニズムが示唆されるようになった.
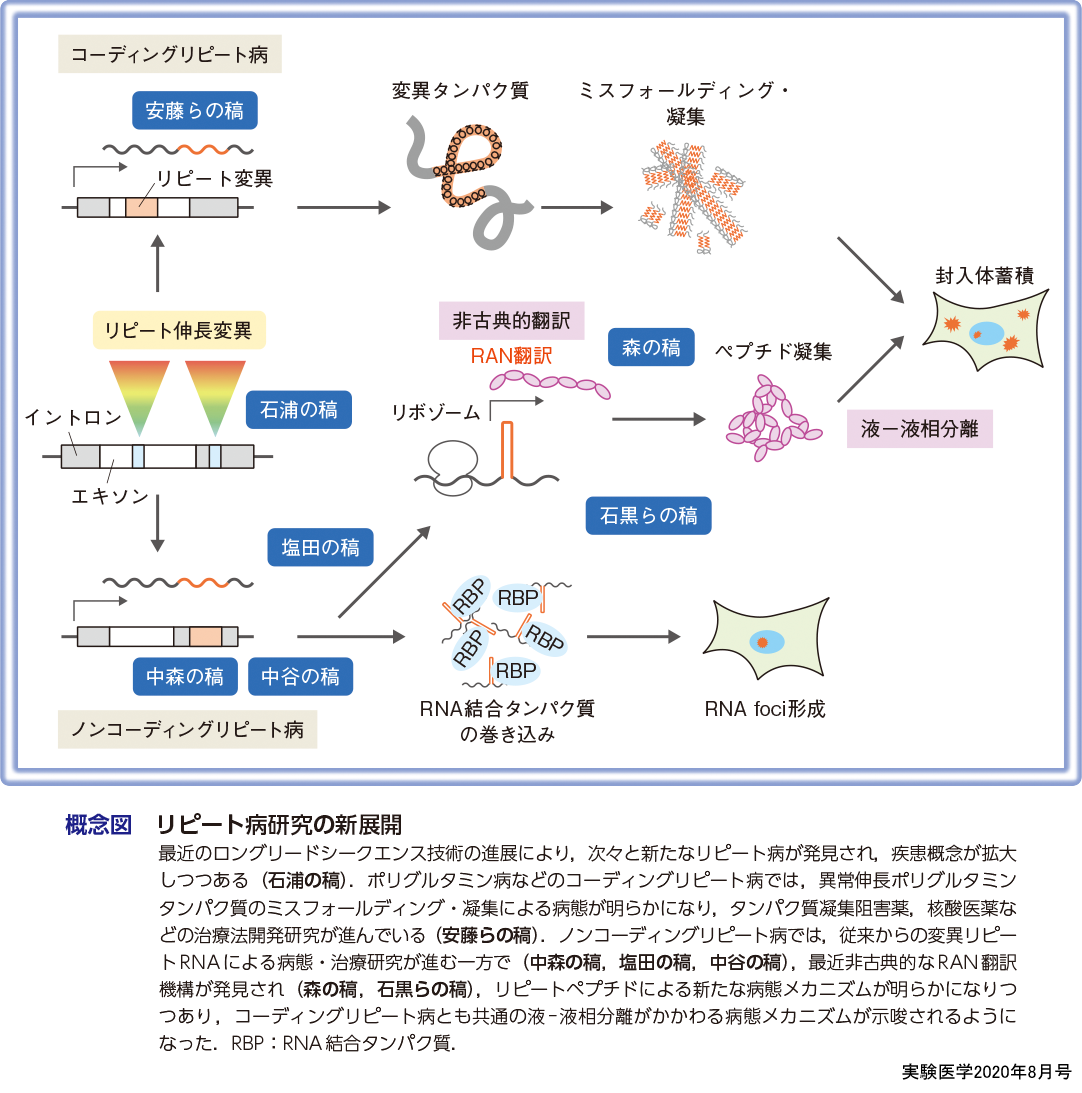
本概論では,リピート病の発見からその病態・治療研究の変遷,そして生物学的にも新しい非古典的翻訳機構であるRAN翻訳の発見以降,急展開を見せている新規の病態メカニズムについて,本誌でも昨年特集が組まれた非古典的翻訳(実験医学2019年11月号),液-液相分離(実験医学2019年6月号)との関連にも触れながら,企画者の視点から概説し,各論での最近のホットトピックスへの導入としたい(概念図).
1コーディングリピート病
異常伸長リピート配列が遺伝子翻訳領域内にあるコーディングリピート病は,ポリグルタミン病,ポリアラニン病が知られているが,主にポリグルタミン病を中心に研究が進んできた.ポリグルタミン病は,グルタミンをコードするCAGリピート配列の異常伸長が原因となる疾患で,前述のSBMAの発見を皮切りに,ハンチントン病,脊髄小脳失調症(spinocerebellar ataxia,SCA)1,2,3,6,7,17型,歯状核赤核淡蒼球ルイ体萎縮症の9疾患が知られている(表1)5).ポリグルタミン病では,異常伸長CAGリピート数の閾値(35~40回)が各疾患でほぼ等しく,CAGリピート数と疾患の発症年齢・重症度との強い相関が認められる.また,9つの原因遺伝子には相同性や機能的類似性が認められず,多くが顕性遺伝(優性遺伝)性で発症することから,異常伸長polyQ鎖自体が毒性を獲得するというgain of toxic functionのメカニズムにより発症すると考えられている.その発症メカニズムとして,polyQ鎖の異常伸長により原因タンパク質のミスフォールディングを引き起こしてβシート構造への異常構造転移を獲得し,その結果アミロイド線維様の凝集体を形成して神経細胞内で封入体として蓄積し,細胞・個体レベルでさまざまな神経機能障害をきたして発症すると考えられている(概念図).われわれは詳細なタンパク質構造解析を行い,重合する前のβシートモノマーの段階でpolyQタンパク質が細胞毒性を発揮することを明らかにした6).このようなタンパク質のミスフォールディング→凝集→神経変性という病態カスケードは,ポリグルタミン病だけでなく,アルツハイマー病やパーキンソン病,筋萎縮性側索硬化症などの他のさまざまな神経変性疾患に共通する普遍的な発症メカニズムであると考えられている.
したがって,このようなタンパク質のミスフォールディング・凝集を標的としたタンパク質凝集阻害薬や変異遺伝子の発現を抑制する核酸医薬,ゲノム編集技術などの治療法開発研究が進んでいる.われわれは,独自のpolyQ凝集濁度アッセイ系(US特許取得済み)を用いた低分子化合物ライブラリー(46,000化合物)のスクリーニングにより約100種類の新規polyQ凝集阻害化合物を同定し,そのうちタンパク質安定化作用をもつ化学シャペロンであるL-アルギニンについて,異常伸長polyQタンパク質のβシート構造転移・凝集を阻害することを示した.そして最近,L-アルギニンがポリグルタミン病モデルショウジョウバエおよび2種類のポリグルタミン病モデルマウスにおいて,polyQタンパク質封入体および神経変性,運動障害を抑制することを明らかにし,さらに発症後からの投与でも有効性を確認した7).以上の結果から,人体への安全性が確立された既存薬であるL-アルギニンについて,新潟大学・小野寺理博士らとともにポリグルタミン病のうち比較的患者数の多いSCA患者を対象とした医師主導治験の準備を進めている.
また,変異遺伝子の発現を抑制するアンチセンスオリゴヌクレオチド(ASO)の開発も進んでいる.リピート病ではないが,難治性神経変性疾患の一つ脊髄性筋萎縮症(spinal muscular atrophy,SMA)に対する核酸医薬ヌシネルセン(スピンラザ®)はすでに臨床応用されており,またポリグルタミン病のうち欧米で患者数の多いハンチントン病に対するASOもすでに臨床治験が行われており8),近い将来の臨床応用が期待されている.さらに,CRISPR/Cas9システムなどの最新のゲノム編集技術を用いて,変異遺伝子そのものを補正するという治療法の開発が試みられている(安藤らの稿).
一方,ポリアラニン病は,アラニンをコードするGCNリピート配列の異常伸長を原因とする疾患で,眼咽頭型筋ジストロフィー(oculopharyngeal muscular dystrophy,OPMD)の他,合多指症,X連鎖性精神発達遅滞など8つの先天性疾患が知られている9).OPMDでは,ポリグルタミン病と同様に異常伸長ポリアラニン鎖をもつ変異PABPN1〔Poly(A)-binding protein nuclear 1〕タンパク質が患者筋細胞内に封入体を形成しており,gain of toxic functionの病態メカニズムが考えられているが,8先天性疾患の原因遺伝子はいずれも転写因子であり,ミスセンス変異も見つかっているため,loss of functionのメカニズムにより発症するという考えが優勢である.
2ノンコーディングリピート病
遺伝子非翻訳領域内に存在するリピート配列の異常伸長を原因とするノンコーディングリピート病としては,前述のFXSをはじめとして,筋強直性ジストロフィー(myotonic dystrophy,DM)1,2型,SCA8,10,12,31,36,37,C9orf72連鎖性筋萎縮性側索硬化症/前頭側頭型認知症(C9orf72-linked amyotrophic lateral sclerosis/frontotemporal dementia,C9-ALS/FTD)など約20疾患を数える(表2).さらに,最近のロングリードシークエンス技術の進展により,遺伝子非翻訳領域内の遺伝子変異検索が進み,次々と新たなノンコーディングリピート病が発見され,疾患概念が拡大しつつある(石浦の稿).
これらの疾患のうち,FXS,フリードライヒ運動失調症など潜性遺伝(劣性遺伝)性疾患では,ミスセンス変異が見つかっているものもあり,loss of functionのメカニズムにより発症すると考えられている.一方で,多くの顕性遺伝性疾患では,比較的初期にリピート伸長変異が発見されたDM1,SCA8などを中心にgain of toxic functionの病態メカニズム研究が進んできた.これらの異常伸長リピート配列は,ポリグルタミン病とは異なって非翻訳領域にあるため,異常伸長リピート配列を含む変異RNAが病態のキー分子であると考えられてきた.実際にこれらの変異RNAは,リピート配列に結合するRNA結合タンパク質を巻き込んで神経・筋細胞内でRNA fociとして蓄積し,これらのRNA結合タンパク質の機能喪失によるさまざまなRNA代謝異常を引き起こすことが明らかにされた(概念図).したがって,このような変異RNAを標的として低分子化合物や核酸医薬などによる治療法開発研究が進んでいる(中森の稿).
一方,2011年にRanum博士らはSCA8,DM1の培養細胞,マウスモデルおよび患者組織において,開始コドンATGをもたないCTG/CAGリピート配列から3フレームの翻訳産物が産生されることを明らかにし,リピート関連非ATG依存性(repeat-associated non-ATG,RAN)翻訳と名付けた(概念図)10).続いて,2013年に脆弱X関連振戦・失調症候群(fragile X-associated tremor/ataxia syndrome,FXTAS)においてCGGリピート配列から,次いでC9-ALS/FTDにおいてもGGGGCC リピート配列からのRAN翻訳によるリピートペプチドの産生が報告され(森の稿),その他現在までにSCA31,DM2やコーディングリピート病であるハンチントン病など8疾患にてRAN翻訳が確認されている.
RAN翻訳のメカニズムはいまだ十分には解明されていないが,最近のプロテオミクス解析技術の革新,リボソームプロファイリング技術の進展により,RAN翻訳に限らずこれまで認識されていなかった新規ORFからの翻訳産物,開始コドンATGに依存しない類似開始コドンからの翻訳などが多数見つかっている16)17).RAN翻訳の鋳型となるリピートRNAはヘアピン構造やグアニン四重鎖構造などの構造をとりやすいことから,リピートRNAの高次構造が関与する可能性が指摘されている(塩田の稿).やはり鋳型RNAのヘアピン構造依存的に翻訳が開始されるIRES(internal ribosome entry site)※2翻訳との類似性も議論されており,IRES翻訳にかかわる40Sリボソームサブユニットの構成因子RPS25がRAN翻訳をも制御することが報告されている18).われわれは,東京医科歯科大学・石川欽也博士らとの共同研究にてSCA31におけるRAN翻訳を報告し,UGGAAリピートRNAに結合するRNA結合タンパク質TDP-43が,UGGAAリピートRNAの構造を変化させてRAN翻訳を制御することを見出し,RNAシャペロンという概念を提唱した(石黒らの稿)19).この概念に基づき,リピートRNAに結合する化合物を用いて,RNA構造の変化,RNA結合タンパク質の蓄積抑制,RNA分解などによる治療法の開発研究が進んでいる(中谷の稿).
RAN翻訳により産生されるリピートペプチドは1~数種類のアミノ酸の単純なくり返し配列であり,いわゆる低複雑性(low complexity,LC)ドメインを形成する.LCドメインはRNA結合タンパク質などに多く認められ,特定の構造をとらない天然変性領域(intrinsically disordered region,IDR)と考えられており,液-液相分離(liquid-liquid phase separation,LLPS)により核小体やストレス顆粒などの膜のないオルガネラの形成に関与することが知られている11)12).C9-ALS/FTDにてRAN翻訳により産生されるリピートペプチドのうち特にアルギニンを含むpolyGR,polyPRは,他のLCドメインを含むタンパク質との相互作用を介して毒性を発揮することが明らかにされている(森の稿).RAN翻訳によらないpolyQやpolyAもいわばLCドメインであり,ataxin-2がLLPSによりストレス顆粒を形成し,そのpolyQ鎖長がALSの発症にもかかわることが明らかにされた13)14).また最近,HOXD13のpolyA鎖がLLPSにより転写因子複合体を形成し,polyA鎖のわずかな伸長による転写調節障害が合多指症の原因となることが報告された15).
おわりに
これまで述べたように,リピート病の研究はその原因リピート配列が遺伝子翻訳領域内にあるか,非翻訳領域内かによって,それぞれタンパク質毒性,RNA毒性を中心に長い間別々に研究されてきたが,RAN翻訳の発見を契機に,リピートペプチドを介した共通の病態メカニズムが明らかになりつつある.このようなリピートペプチドはLCドメインをもつタンパク質と相互作用しやすく,これらが液-液相分離を介して形成する膜のないオルガネラの生理的機能を障害することが想定される.このような病態メカニズムは,やはりLCドメインをもつTDP-43やFUSなどのRNA結合タンパク質によるALS/FTDの研究から解明されてきたものであり,これがリピート病にも共通する可能性を示唆している.このように考えると,前述のataxin-2のpolyQ鎖長がALSの発症にもかかわること14)や,polyQタンパク質の凝集体からFUSが発見されたこと20)などにも合点がいく.またRAN翻訳の発見は,生物学的にも開始コドンATGに依存しない新しい翻訳機構の研究への道を拓き,古典的なORFの見直し,未知のタンパク質世界の開拓にもつながるであろう.本特集を通じて,疾患研究から新しい生命現象の発見につながるという研究の面白さを感じていただき,特に若手の読者の方々の疾患研究への参入を期待したい.
【謝辞】表2の作成にあたって,貴重なご助言をいただきました石浦浩之先生(東京大学)に深謝いたします.
文献
- Kremer EJ, et al:Science, 252:1711-1714, 1991
- La Spada AR, et al:Nature, 352:77-79, 1991
- Paulson H:Handb Clin Neurol, 147:105-123, 2018
- Rodriguez CM & Todd PK:Neurobiol Dis, 130:104515, 2019
- Takeuchi T & Nagai Y:Brain Sci, 7:128, 2017
- Nagai Y, et al:Nat Struct Mol Biol, 14:332-340, 2007
- Minakawa EN, et al:Brain, 143:1811-1825, 2020
- Tabrizi SJ, et al:N Engl J Med, 380:2307-2316, 2019
- Hughes JN & Thomas PQ:Methods Mol Biol, 1017:135-151, 2013
- Zu T, et al:Proc Natl Acad Sci U S A, 108:260-265, 2011
- Aguzzi A & Altmeyer M:Trends Cell Biol, 26:547-558, 2016
- 実験医学2019年6月号「細胞内の相分離」(加藤昌人,廣瀬哲郎/企画),羊土社,2019
- Nonhoff U, et al:Mol Biol Cell, 18:1385-1396, 2007
- Elden AC, et al:Nature, 466:1069-1075, 2010
- Basu S, et al:Cell, 181:1062-1079.e30, 2020
- Chen J, et al:Science, 367:1140-1146, 2020
- 実験医学2019年11月号「再定義されるタンパク質の常識」(田口英樹/企画),羊土社,2019
- Yamada SB, et al:Nat Neurosci, 22:1383-1388, 2019
- Ishiguro T, et al:Neuron, 94:108-124.e7, 2017
- Doi H, et al:J Biol Chem, 283:6489-6500, 2008
著者プロフィール
永井義隆:1990年大阪大学医学部卒業,’95年同大学院医学系研究科博士課程修了,博士(医学).米国デューク大学ポスドク,大阪大学大学院医学系研究科助手・准教授,国立精神・神経医療研究センター・室長を経て,2016年より大阪大学大学院医学系研究科教授.大学院に入学した1991年にSBMAのCAGリピート伸長変異に出会い,以来リピート病に限らず神経変性疾患全般を対象として,分子生物学・タンパク質科学からショウジョウバエ遺伝学,マウス,マーモセットなど多彩な技術を駆使し,神経難病の克服をめざして研究を進めている.












