概論
種々の生命現象にかかわるリソソームの新たな姿
Novel aspects of lysosomes involved in various biological phenomena
中村修平
Shuhei Nakamura:Institute for Advanced Co-Creation Studies, Osaka
University(大阪大学高等共創研究院)
リソソームは内部に多種の消化酵素をもつ酸性の細胞小器官(オルガネラ)であり,細胞内外の種々の成分の分解を担う.最近の相次ぐ発見から,リソソームに対する見方は従来の分解に特化した静的なものから,刺激に応じて活性・動態をダイナミックに変化させ,シグナル伝達を媒介することで細胞・個体の恒常性維持に関与する,きわめて動的なオルガネラであるとの認識に置き換わりつつある.また,従来知られる希少疾患であるリソソーム病に加え,炎症性疾患,神経変性疾患,がん,細胞や個体の老化との新たな関連も見つかっており,リソソームの制御や役割にますます注目が集まっている.本特集では各分野の第一線で活躍されている国内の研究者に最新のトピックをご提供いただくことで,近年見えてきたリソソームの新たな姿の一端を紹介したい.
はじめに
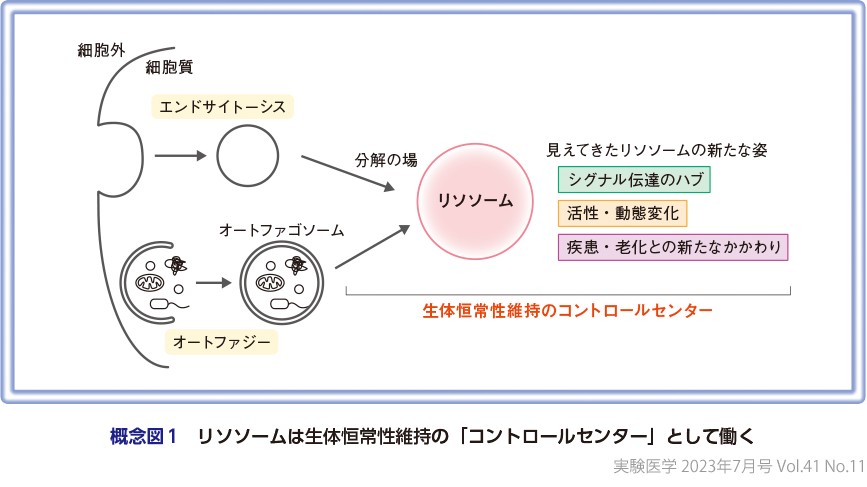
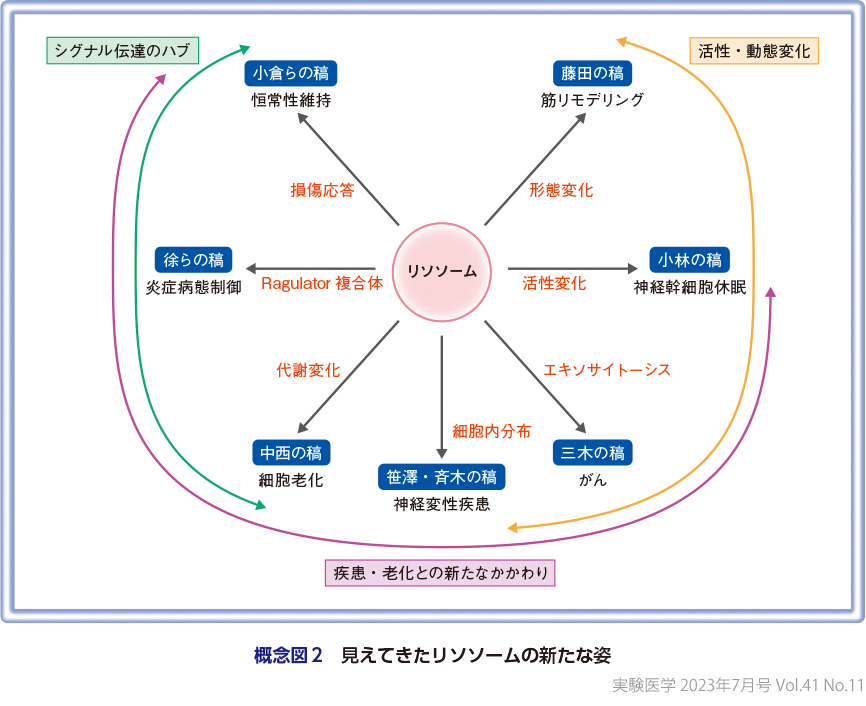
リソソームは1950年代にChristian de Duve博士によって発見された直径0.1〜1 μmほどの細胞小器官(オルガネラ)である.リソソーム内部は酸性に保たれ,酸性領域に至適pHをもつプロテアーゼ,ヌクレアーゼ,リパーゼ,サルファターゼなど60種類以上の加水分解酵素が存在し,これらがタンパク質,核酸,脂質,糖質などの生体高分子の分解を担っている1).リソソームへの物質の輸送は主にエンドサイトーシス経路や細胞内大規模分解システムであるオートファジー経路が担う.これまでの研究ではリソソームは分解の場として,これら輸送経路の終末処理場として扱われることが多かったが,最近の相次ぐ発見からリソソームは種々の生命現象に積極的に関与し生体恒常性維持の「コントロールセンター」として働くことがわかってきた2)(概念図1).本稿では特に最近のリソソーム研究から見えてきた,シグナル伝達のハブとしてのリソソーム機能,リソソーム活性・動態変化の制御と役割,リソソーム機能不全と老化や疾患との新たなかかわりについて概説し,リソソームが見せる新たな姿の一端を紹介したい(概念図2).
1シグナル伝達のハブとしてのリソソーム
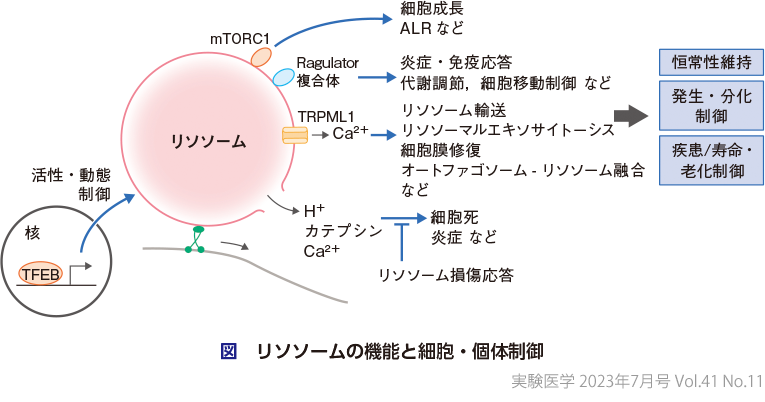
最近の研究から,リソソーム由来のさまざまな要素,例えばリソソーム膜上タンパク質,リソソーム内イオン,脂質などがシグナルとして働き,種々の生命現象に関与することがわかってきている(図).
❶ リソソーム膜上タンパク質によるシグナル伝達
分解,リサイクルを担うリソソームは細胞の栄養状態を検知する場としても適している.実際,栄養センサーとして知られるmTORC1が特定条件下でリソソーム膜上にリクルートされて活性化されることがわかり,リソソームによる栄養センシングの分野は大きく発展した.mTORC1は,栄養や成長因子の存在下で細胞の同化と成長をサポートしつつ,ULK1や後述の転写因子TFEBのリン酸化を通じて,オートファジーなどの異化経路を抑制する.一方で,mTORC1は長期飢餓のオートファジーの間に起こるリソソーム再生ALR(autophagic lysosome reformation)にも必要となる(藤田の稿).mTORC1の膜上へのリクルートと活性化は,アミノ酸に依存したヘテロ二量体RAG GTPaseの活性化とRagulator複合体との相互作用によって媒介される.その他詳細なmTORC1の活性化機構については多くのレビューが出ており,そちらを参照されたい3).このRagulator複合体もリソソーム膜上で働くが,最近の研究からmTORC1以外にもさまざまなタンパク質と相互作用することでインフラマソームの活性化,代謝調節,免疫細胞の移動などへ関与することが明らかとなり,炎症制御におけるシグナル伝達のハブとしての新たな役割が注目されている(徐らの稿).
❷ リソソームからのカルシウム放出によるシグナル伝達
リソソームからのCa2+シグナルも多岐にわたるリソソーム機能の制御にかかわる.複数あるリソソームのCa2+チャネルの中でも最も解析が進んでいるのは,ムコリピン1としても知られるTRPML1である4).TRPML1は,早期発症と進行性の神経変性を特徴とするリソソーム病の一つであるムコリピドーシスⅣ型の原因遺伝子としても知られている.TRPML1は,リソソーム内腔から細胞質へのCa2+放出を仲介し,飢餓や活性酸素を含むいくつかの刺激,ホスファチジルイノシトール-3,5-二リン酸(PI(3,5)P2)などによって活性化される.TRPML1を介したCa2+シグナルはリソソームの輸送(笹澤・斉木の稿),リソソームの内腔物質を細胞外に放出するリソソーマルエキソサイトーシス(三木の稿),ESCRTによる細胞膜修復,オートファゴソーム-リソソーム融合,エンドソーム-リソソーム融合,リソソームサイズ調節,融合後のハイブリッドオルガネラからのリソソーム再形成など多くのリソソーム機能,動態制御に関与する.また,TRPML1は後述のリソソームマスター制御因子TFEBの活性調節を担うとともに(小倉らの稿),TFEBのターゲットでもあるため,リソソーム機能,動態制御の正のフィードバックループ形成の中心的な役割を果たしている.
❸ 脂質によるシグナル伝達
リソソームはまた脂質を介したシグナル伝達のハブにもなっている.リソソーム膜に存在する種々のホスホイノシチドがリソソームの分布,生合成,オートファゴソームとの融合,オルガネラコンタクトサイトでの脂質移動の機能など,リソソームの動態や機能のさまざまな側面を制御する.さらに,線虫を用いた最近の研究からリソソームリパーゼであるlipl-4(ヒトのLIPAのホモログ)活性化によって生じた脂質オレオイルエタノールアミド(OEA)が個体寿命を延長させることが示されている5).
❹ リソソーム損傷を引き金とするシグナル伝達
リソソームは細胞内外のさまざまな要因でしばしば損傷を受けることがわかっている.損傷したリソソームからはプロトンやカテプシンが漏出してこれがシグナルとなって細胞死や炎症を引き起こす.最近の研究から,細胞にはこの有害な損傷リソソームに対処するため「リソソーム損傷応答」と総称される機構が備わっていることがわかってきた(小倉らの稿).リソソーム損傷応答には選択的なオートファジーの一つであるリソファジーやESCRTタンパク質による膜修復の経路,転写因子TFEBによるリソソーム生合成経路などがあり,これらが協調して働きリソソーム恒常性が保たれる6).これまでにリソソーム損傷に伴うCa2+流出,リソソーム膜タンパク質のユビキチン化,脂質スクランブルなどの複数の要素がリソソーム損傷応答のトリガーとなることがわかってきている.興味深いことに,老化した細胞ではリソソーム膜損傷に伴う細胞質の酸性化を防ぐ機構が備わっており,これが老化細胞の生存に必須であることが明らかとなった(中西の稿).逆に,この経路の遮断は新しいセノリティクス(老化細胞除去)のターゲットとしても着目されている.
2リソソーム活性・動態変化の制御と役割
教科書的にリソソームは細胞内に単独で存在する球形の構造として描かれることが多いが,近年,さまざまな環境や刺激に応じてその活性や動態(数,形態,細胞内分布など)がダイナミックに変化することが示され,これが細胞の恒常性維持や発生・分化の制御,さらには特定の疾患や寿命・老化の制御とも密接にかかわることがわかってきた.
リソソーム活性や動態を転写レベルで制御する因子としてMiT-TFEファミリーに属するTFEBが同定され,リソソーム研究の分野は大きく進展した.はじめはin silicoの解析でリソソーム関連遺伝子の多くのプロモーター領域にCLEAR(coordinated lysosomal expression and regulation)とよばれる領域が存在することがわかり,この領域に結合してこれら遺伝子の発現を上昇させる転写因子としてTFEBが同定された7).その後の解析からTFEBは多くのオートファジー関連因子の発現制御も担うことが示され,オートファジー・リソソーム機能のマスターレギュレーターとして働くことがわかった8).近年TFEB活性化はオートファジーあるいはリソソームの活性や数などの動態,もしくはその両方の制御を介して神経変性疾患や代謝疾患を含む多くの疾患の抑制,寿命延長にもつながることが明らかとなり,治療や介入のターゲットとしてTFEB制御機構や役割が注目されている.さらに最近ではTFEBが細胞老化9),概日リズム10),神経幹細胞の分化や休眠維持の制御等にも関与することが示され(小林の稿),リソソーム活性・動態変化の広範な生命現象への関与がTFEBの機能解析を通して明らかとなってきている.TFEBの活性は主にそのリン酸化状態とこれに伴う核-細胞質間の局在変化によって制御される11).通常TFEBはリン酸化されて細胞質に留まっているが,飢餓やさまざまなストレス,細胞の分化段階や環境刺激によって脱リン酸化され,核移行・活性化し,ターゲット遺伝子の転写をオンにする.TFEBのリン酸化を担う因子としてmTORC1が,一方脱リン酸化にはカルシニューリン等が関与することがわかっているが,種々の環境・刺激に応じて異なる活性化機構があることも見え始めており,全容解明に向けた今後の解析が期待される.
リソソームの活性や数に加え,形態や細胞内分布も刺激や環境に応じてダイナミックに変化することがわかってきた.以前から一部の細胞では刺激に応じてリソソーム形態が変化することがわかっていたが,最近新たにショウジョウバエの変態期にみられる筋細胞リモデリングの際に管状のリソソームネットワークが形成されることが報告された(藤田の稿).リソソーム形態を一過的に大きく変化させることで表面積や体積を増加させ効率的な分解を可能にしているのかもしれない.このダイナミックな変化の制御機構や役割の解明が一層進むことで,筋機能維持につながる新たな知見が得られる可能性がある.リソソームの細胞内局在も刺激に応じてダイナミックに変化し,この分布の違いがmTORC1の活性,リソソームのpH,オートファジー活性,がんの浸潤などに必須の働きをもつことがわかってきている.ダイニンやその活性化因子ダイナクチンによるリソソームの核近傍への輸送(逆行輸送)によってオートファゴソームとの効率的な融合が起こり,オートファジー活性が亢進する(笹澤・斉木の稿).一方,核近傍から細胞周辺へのリソソーム輸送(順行輸送)はいくつかのキネシンが担い,これがリソソーマルエキソサイトーシスを介した細胞膜の修復や,がん細胞の浸潤や生存に働いている(三木の稿).
3リソソーム機能不全と疾患,老化との新たなかかわり
リソソームの機能不全がヒトの病気を引き起こす典型的な例としては早期発症の神経変性を伴う遺伝子疾患であるリソソーム病が知られている.これらの疾患では,リソソームの遺伝子またはリソソーム機能にかかわる遺伝子の変異により,リソソームを介した分解・リサイクルのプロセスが障害され,分解されない基質がリソソームに徐々に蓄積する.最近の研究から,リソソームはこれら希少疾患だけでなく,より一般的な疾患,さらには個体および細胞老化ともかかわりがあることがわかってきた.前述のシグナル伝達ハブとして働くRagulator複合体はインフラマソームの活性化を介して多くの炎症性疾患の制御に関与する(徐らの稿).また,損傷リソソーム応答の破綻が,神経変性疾患や結晶性腎症などのリソソーム損傷を伴う疾患の進展につながることや(小倉らの稿),損傷リソソームと細胞老化や加齢に伴う慢性炎症との新たな関連も報告されている(中西の稿).以前から,オートファジー・リソソーム機能不全によるタンパク質凝集は多くの神経変性疾患の要因となることが示されている.また,神経細胞は長い軸索をもつことからリソソームやオートファゴソームの適切な細胞内分布の制御が効率的なオートファジー・リソソーム機能の活性亢進に特に重要となる.事実これらの輸送障害が神経変性疾患の進展につながることが示されている.さらに最近はパーキンソン病で上昇するアルデヒドであるアクロレインによるリソソーム輸送の新たなメカニズムが明らかとなり,これがオートファジーの効率的な活性化と酸化ストレスに対する生体防御に働く可能性が示された(笹澤・斉木の稿).また,近年の研究からリソソームはがん細胞に栄養を供給し,高い栄養要求性を満たすのに必須の役割を果たすことがわかってきた.いくつかのがん細胞ではMiT-TFE遺伝子群の発現亢進を伴っており,これによりオートファジー・リソソーム系による栄養の供給とmTORC1による生合成経路の両方が活性化することでがんの高い栄養要求性を満たしている.さらに最近,がん細胞の酸性環境下での生存・増殖にリソソーマルエキソサイトーシスが必須の働きをすることが示されている(三木の稿).一般的に加齢に伴いリソソームの機能が低下することが報告されており,これが組織の機能低下,加齢性疾患や個体の寿命の短縮につながることが示唆されている12)13).一方でTFEBの過剰発現によるリソソーム機能の亢進は線虫の寿命を延長させ,哺乳類では免疫細胞や組織幹細胞の若返りにも寄与することから(小林の稿)14)〜16),リソソームは個体,および細胞レベルでの老化の制御の中心的な役割を果たしている可能性がある.
おわりに
最近の研究から見えてきたリソソーム機能の一部について紹介した.ただし,ここで触れなかった知見も含め,これまでにわかっているリソソームの働きは氷山の一角に過ぎないだろう.実際,リソソーム膜には何百ものタンパク質が存在し,その多くは機能未知なままである.加えてリソソーム膜上タンパク質,イオン,分解産物(アミノ酸,核酸,脂質など)などリソソームに関連するさまざまな要素に思いもよらない機能や役割が隠れている可能性が高い.また組織や細胞種,発生や分化のタイミングによっても活性・動態やその制御の違いが見え始めており,リソソームの全容を知るにはさらなる解析が必要となる.新たに見えてきたリソソームと疾患の関連から,これらをどのように治療に応用するかも今後の課題となるだろう.本特集が多くの読者にとってリソソームに対するイメージを再考し,リソソーム研究へ興味をもつきっかけとなれば幸いである.
文献
- De Duve C, et al:Biochem J, 60:604-617, doi:10.1042/bj0600604(1955)
- Ballabio A & Bonifacino JS:Nat Rev Mol Cell Biol, 21:101-118, doi:10.1038/s41580-019-0185-4(2020)
- Liu GY & Sabatini DM:Nat Rev Mol Cell Biol, 21:183-203, doi:10.1038/s41580-019-0199-y(2020)
- Di Paola S, et al:Cell Calcium, 69:112-121, doi:10.1016/j.ceca.2017.06.006(2018)
- Folick A, et al:Science, 347:83-86, doi:10.1126/science.1258857(2015)
- Yang H & Tan JX:Trends Cell Biol, doi:10.1016/j.tcb.2023.01.001(2023)
- Sardiello M, et al:Science, 325:473-477, doi:10.1126/science.1174447(2009)
- Settembre C, et al:Science, 332:1429-1433, doi:10.1126/science.1204592(2011)
- Curnock R, et al:EMBO J, 42:e111241, doi:10.15252/embj.2022111241(2023)
- Pastore N, et al:EMBO J, 38:e101347, doi:10.15252/embj.2018101347(2019)
- Puertollano R, et al:EMBO J, 37:e98804, doi:10.15252/embj.201798804(2018)
- Carmona-Gutierrez D, et al:Ageing Res Rev, 32:2-12, doi:10.1016/j.arr.2016.04.009(2016)
- Sun Y, et al:Elife, 9:e55745, doi:10.7554/eLife.55745(2020)
- Zhang H, et al:Mol Cell, 76:110-125.e9, doi:10.1016/j.molcel.2019.08.005(2019)
- Leeman DS, et al:Science, 359:1277-1283, doi:10.1126/science.aag3048(2018)
- Lapierre LR, et al:Nat Commun, 4:2267, doi:10.1038/ncomms3267(2013)
本記事のDOI:10.18958/7277-00001-0000508-00
著者プロフィール
中村修平:2003年北海道大学理学部卒業,’08年北海道大学大学院理学研究科生物科学専攻博士課程修了 博士(理学),’08年基礎生物学研究所研究員,’11年Max Planck Institute for Biology of Ageingポスドク,’16年大阪大学大学院医学系研究科助教を経て’18年より大阪大学高等共創研究院准教授.この間,日本学術振興会特別研究員(DC1),海外特別研究員,マリーキュリーフェローシップなど.











