企画(所属は掲載時)
- 谷上賢瑞(東京大学分子細胞生物学研究所)
- 八谷剛史(岩手医科大学いわて東北メディカルメガバンク機構)
- 西塚 哲(岩手医科大学医学部外科)
- 中川英刀(理化学研究所統合生命医科学研究センター)
本コンテンツは,実験医学同名コーナーからの転載となります(2016年4月号〜).
患者さん由来の核酸情報をもとに精密な医療を行うクリニカルシークエンスは,感度・効率・侵襲性の面でがんの診断・治療に飛躍をもたらす可能性が注目されています.特に血中DNAに焦点を当て,研究最前線の熱気を紹介いただいています.
実験医学誌面上での1年にわたる連載を,たくさんの方にご愛読いただくために,イントロダクションにあたる第1~3回をWEBで公開いたします! ご興味をお持ちいただけた方は,より深い議論が展開される第4回以降をぜひ誌面でお楽しみください.(編集部)
第1回 がん診断の新たなマテリアル,ctDNA
著/西塚 哲,谷上賢瑞,八谷剛史,中川英刀
ポイント
- がんゲノム情報の充実とともに,腫瘍由来循環DNA(ctDNA)によるがん診断法が注目されている.
- 従来の腫瘍マーカーに比べ,ctDNAは由来が明確で早期での検出が可能である.
- ctDNAは体内腫瘍量,薬剤耐性,早期発見マーカーとしての有用性が示唆されている.
- 極めて微量であるctDNA検出のため,サンプル処理,装置,解析の技術開発が進んでいる.
連載のはじめにあたって
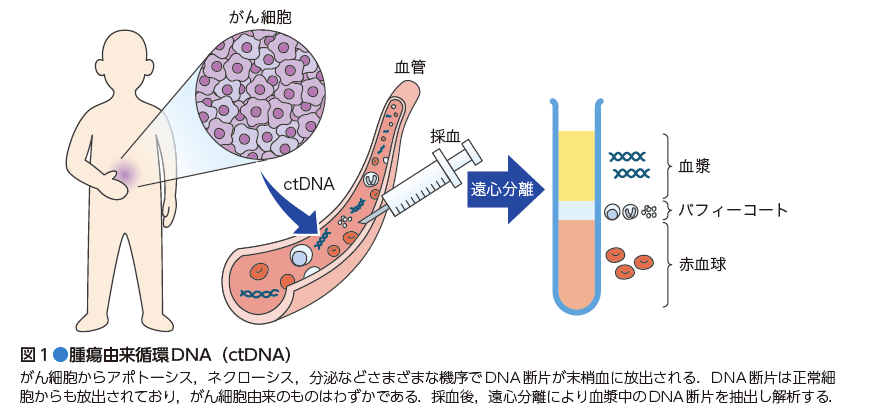
定期健診で行われる血液検査で,がんの有無や種類,さらには再発・転移の可能性を評価できる時代が来れば,がん医療の未来が著しく好転するであろう.現在用いられている多くの血清腫瘍マーカーは,その感度・特異度が十分ではなく,単独で病勢の指標とするのは難しい.末梢血中に含まれる腫瘍細胞由来の循環DNA (circulating tumor DNA:ctDNA) は(図1),がんの種類ごとに特異的な体細胞変異を確認することが期待できるため,近年注目を浴びている.がんのクリニカルシークエンス※1,特にこのctDNAをがん診断へ利用する試みはすでに行われており,がんの早期発見,術後評価の指標,およびコンパニオン診断薬としての有用性が期待され,米国ではベンチャー企業が続々と設立されている.われわれは,2013年9月に神戸で『次世代シークエンサー(NGS)現場の会,第3回研究会』,2014年5月に東京で『NGS現場の会,第1回血液核酸マーカー分科会』,2015年7月につくばで『NGS現場の会,第4回研究会』を開催し,がんゲノムシークエンス,ctDNA研究の議論を重ねてきた.本連載では,第1〜3回でctDNA解析技術の現状を紹介し,第4回以降では現在国内で進行中のctDNA研究に焦点を当てる.読者の皆さんがctDNA研究の実情を把握し,新しい研究アイデアを生み出すことの一助になれば幸いである.
がんゲノム情報による腫瘍マーカー変革
「Deciphering Nature’s Alphabet」(DNA)は,デオキシリボ核酸(DNA)の構造が明らかにされてから50周年の節目にヒトゲノム計画が完了したことを記念して,2003年に米国立ヒトゲノム研究所(NHGRI)で行われたイベントのタイトルである.4種類の塩基を指すAlphabetという単語に,ゲノム解析により生物を構成する基本ユニットから生命現象を理解できるようになるだろうという期待が込められていることがわかる.
代表的ゲノム解析の対象であるがんでは,その後の約10年以上をかけて,種類によって異なった変異セットがあること,どのがんにも共通して起きる変異はまれであること,全体では低頻度の変異が1つのがんに多数蓄積していることなどがわかってきた1).また,これらのうち本当にがんの発生・進展・治療抵抗性にかかわっているものは全ゲノムと比較すると極めて少数であり,多くの場合は直接的な機能には関連が薄いと想定されているパッセンジャー変異であることも判明した2).このことは個々のがんの成り立ちに応じた,特有の変異が蓄積していることを示唆している.蓄積した変異遺伝子のなかには悪性度や薬剤感受性の情報を含むものがあるため,遺伝子産物の機能に対応した変異を検出することは腫瘍マーカーとして有用であると考えられるようになった.
いわゆる腫瘍マーカー※2研究は,PubMed検索では20万件を超える巨大な分野である.一方で,由来を確定できない分子や再現性に乏しい腫瘍マーカー候補も少なくなく,研究の成果はそのごく一部が臨床に反映されるのみである.がんゲノムは個人のがん特有の情報であり,生体材料からの検出は直接的にがんの存在を意味する.がんゲノム情報を臨床的需要に対応させ使用することで,従来の腫瘍マーカーとは異なった診断精度が現実のものとなりつつある.
ctDNAによるがん診断
すでに1970年代には,がん患者の血液中には有核細胞分画由来のDNAとは別に,血中を循環しているDNAが健常人よりも多く存在することが知られていた3).しかしPCR産物を断片ごとにカウントする原理であるデジタルPCR(dPCR)※3技術導入以前は,ctDNAの検出自体が不安定であると考えられていた.血中に遊離しているDNAの塩基配列決定法が確立されたことで,ごくわずかながら原発腫瘍と同じ変異をもつDNA断片が血中を循環していることがわかってきたのである.このわずかな分画がctDNAであり,これを定量的に解析したがん診断法が近年相次いで報告されている4).さらに,がんゲノム情報の充実とシークエンス技術の進歩により,臨床的重要性が高い薬剤耐性遺伝子に限定した方法や,各種がんで変異が報告されている数十〜数百個のホットスポットのターゲットシークエンスにより効率的に変異を検出できるパネルも登場した.
現在,臨床的に有用な腫瘍マーカーとしてのctDNAの使用法は,
- 体内腫瘍量のモニタリング
- 薬剤耐性遺伝子の判定
- 超早期がんの発見
に集約されつつある.体内腫瘍量のモニタリングは,現在は血清腫瘍マーカーが最も簡便なツールとして用いられることが多い.実際,腫瘍マーカーは再発がある程度進んだ場合や時系列の変動が治療を反映している場合は有用な補助診断ツールである.一方で,感度・特異度の限界に加え,再発の確認にはCTスキャンなどの画像診断が必須であるため,さらなるマーカーが求められている.ctDNAによる変異検出を用いれば,特異性が高い結果が得られ,かつ早い時期に再発を発見できることが期待されている.肺がんなどで研究が進んでいる薬剤耐性遺伝子獲得については,特定の酵素に対する分子標的薬の耐性が耐性関連遺伝子変異と対応する性質を利用し,侵襲の大きい再生検の必要なしに治療戦略を構築できる.がん検診などで威力を発揮する可能性がある超早期がんの発見は,後述する技術開発と密接に関連しているが,採血のみで高精度のがん検診を提供できるようになる可能性がある.
いずれの場合も採血に関する制約や,0.1%以下ともいわれる超低頻度変異を正確に計測するための技術の成熟など課題もある.しかしながら,将来的にはctDNAによって日常のがん診断が「見るもの」から「測るもの」へ変化してゆく可能性があるのだ.
ctDNAのサンプリング
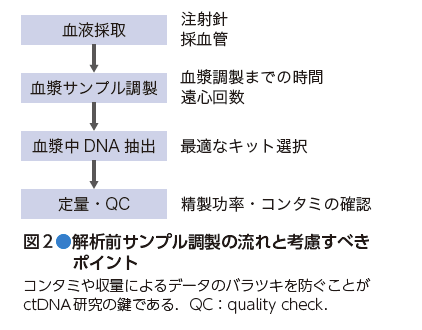
ctDNA研究において,正確な実験結果を得るには,試料の収集法と解析前サンプル調製の標準化は非常に重要な問題である5).不純物の混入や収量によるデータのばらつきを防ぐために,次世代シークエンサーやdPCRを用いて解析を行う前に,患者間,実験者間,組織間から生じるバイアスを極力減らす必要がある.解析前サンプル調製の過程は大きく分けて,患者からの血液採取,遠心による血漿分離,血漿DNA抽出,および抽出DNAの定量/Quality Checkの4段階である (図2).特に,血漿を遠心分離するまでの時間がサンプルの品質に大きく影響するため,院内および研究組織内での共通理解が極めて重要となる.採血後時間が経過するに従い,血中有核細胞由来DNA量が増加し,相対的にctDNA量が減少する.そのため,採血後の検体を凍結することなく2時間以内に血漿の遠心分離を行うよう推奨されているが,実務上この条件は実現困難である場合も多い.血中有核細胞からのDNA放出を防ぐctDNA 解析専用の採血菅も開発されているが,広く普及するには至っていない6).1本の患者血液検体から,ctDNAと白血球(バフィーコート)※4由来DNAが得られる.バフィーコート由来DNAから生殖細胞系列変異を確認したうえで,血漿由来のDNA(ctDNA含む)からがんの体細胞変異を探索する.両サンプルをきちんと分離して解析できるよう細心の注意を払いたい.サンプリングについては連載第2回でも詳しく解説する.
ctDNAの解析技術
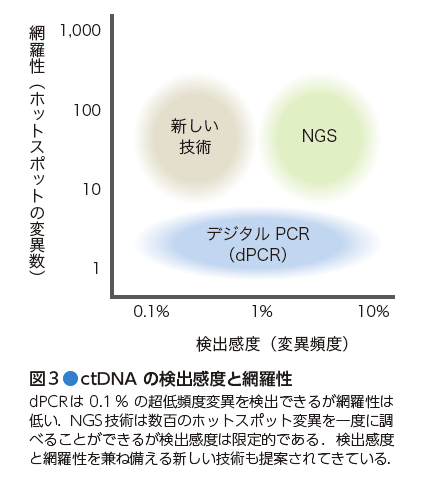
ctDNAの解析技術は,「検出感度」と「網羅性」の双軸で捉えることが大切である(図3).血漿中のctDNAをシグナル(S),白血球由来DNAをバックグラウンド(B)とすると,求められる「検出感度(S/[S+B])」よりも技術的な測定ノイズ(N)は小さくなければいけない.われわれの経験の範囲内では,がんの部位やステージにも依存するが,ctDNAは通常,0.1〜1%(多くても5%)の低頻度で含まれている.そのため,最低でも1〜5%の低頻度変異を検出する感度が必要であり,また,場合によっては0.1%程度の超低頻度変異を検出できる感度が求められる.
また,ゲノム中のいずれの塩基が,がん特有の体細胞変異であるかは,本来であれば原発巣や転移がんの手術検体のゲノム解析を行わないとわからない.そのため,手術検体が入手できない場合には,国際がんゲノムコンソーシアムなどの成果で明らかになった「がん変異ホットスポット」(がん変異が起こりやすいゲノム中の塩基)を網羅的に調べることも考えられる.がん変異ホットスポットは数百カ所(数十〜数百遺伝子にまたがる)知られている.
残念ながら,執筆時点(2016年1月)において,「検出感度」と「網羅性」を両立する技術は普及していないため,ctDNAの解析技術の観点から「検出感度」と「網羅性」のどちらかを優先しなければならない.手術検体が入手できる場合など,「網羅性」は必要としないが「検出感度」を追求したい場合にはdPCR技術が適している.一方,「検出感度」を犠牲にしてでも「網羅性」が必要となる場合にはNGS技術が適している.また,「検出感度」と「網羅性」を両立する技術も提案されてきており,市販キットや委託サービスとして普及する日もそう遠くないと見込まれる.解析技術については第3回で詳しく解説する.
おわりに
1987年にがん由来DNAが血液中を循環していることが発見されて以来7),ctDNAをがんの低侵襲バイオマーカーとして利用するアイデアは早くから提案されていた.そして,2000年にヒトゲノムのドラフト配列が解読され8),2010年にはがんの全ゲノム配列を調べることが現実的になり9),2015年にはがんのホットスポットがリストアップされた1).30年の時を経て,そのアイデアにゲノム解析技術が追いつきつつある.ctDNAの解析技術が発展中であり,その臨床的有用性の検証が国内外で急速に進んでいる今,ctDNAをマテリアルとするがん診断はエキサイティングな研究の最前線となってきており,さらには多くの企業が参入しようとしている.本連載は1年間を予定しているが,連載中にも次々と新しい解析技術,新しい臨床研究が報告される可能性が高い.著者らにとっても激動の1年間を,リアルタイムな興奮を,連載を通じて伝えられたら幸いである.
文献
- Lawrence MS, et al:Nature, 505:495-501, 2014
- McFarland CD, et al:Proc Natl Sci USA, 110:2910-2915, 2013
- Leon SA, et al:Cancer Res 37:646-650, 1977
- Diaz LA & Bardelli A:J Clin Oncol, 32:579-586, 2014
- El Messaoudi S, et al:Clin Chim Acta, 424:222-230, 2013
- Norton SE, et al:Clin Biochem, 46:1561-1565, 2013
- Stroun et al:Eur J Cancer Clin Oncol, 23:707–712, 1987
- Lander et al:Nature, 409:860–921, 2001
- Fujimoto et al:Nat Genet, 44:760–764, 2012
著者プロフィール(執筆時)
- 西塚 哲
- 1994年,岩手医科大学医学部卒業.1998年,同大学院修了.医学博士.同年よりカリフォルニア大学アーバイン校博士研究員,米国国立がん研究所リサーチフェロー,同分子トランスレーショナル技術開発部門長およびフレデリック研究所上級研究員を経て,2007年より現職.2014年より逆相タンパクアレイ国際会議会頭.がん再発予防と見えないがんの診断に挑戦中.
- 谷上賢瑞
- 2010年3月 東京大学理学部生物化学専攻修了.博士(理学).2010年4月 東京大学分子細胞生物学研究所分子情報研究分野博士研究員を経て,2011年7月より同助教.機能未知なlncRNAを,がんに関わる様々な生命現象に紐付けしていくことを目標としている.
- 八谷剛史
- 2005年,慶應義塾大学理工学部卒業.2010年,同大学博士課程修了.理学博士.同年より慶應義塾大学大学院理工学研究科特別研究助教,同研究科特任助教を経て,2013年より現職.バイオインフォマティクスの力で,Deciphering Nature’s Alphabet (DNA)をめざしながら,デオキシリボ核酸(DNA)と日々格闘中.
- 中川英刀
- 1991年,大阪大学医学部卒業.8年間の外科医のトレーニングと研究の後,1999年オハイオ州立大学で大腸癌のゲノム・エピゲノム研究.2003年より東大医科研ヒトゲノム解析センター,2008年より理研にて,マイクロアレイ,GWAS,そしてNGSでのがんのゲノム研究,そしてゲノムの臨床への応用を主題としている.ICGC/TCGAの肝癌ゲノムおよびPanCancer全ゲノム解析のPIとして活動中.
脚注
- ※1 クリニカルシークエンス
- 臨床応用を前提としたDNA塩基配列(シークエンス)の解析およびそのデータを指す.がん医療においては,すでに肺がんや大腸がんなどで分子標的治療の効果予測に応用されている.近い将来,さまざまながんでの再発モニタリング,治療効果判定や予測,あるいは,超早期がんの発見にも有用であると期待されている.
- ※2 腫瘍マーカー
- 腫瘍の存在を推定できる血中の分子を指す.感度・特異度には課題もあるものの,治療効果の判定や再発モニタリングに広く使用されている.代表的なものとして,大腸がんのCEA(癌胎児性抗原),前立腺がんのPSA(前立腺特異抗原)などがある.
- ※3 デジタルPCR(dPCR)
- 従来のPCR法では,PCR産物を集団で検出していたのに対し,デジタルPCRは増幅前の分子を分別し,1分子ごとに対象配列の増幅ありなしをカウントする.測定単位が1分子であることで(結果は二値化されるので「デジタル」である),アレル頻度を正確に計測することができる.
- ※4 バフィーコート
- 全血を遠心分離した際に見られる白色の層.主に白血球と血小板からなる.ほとんどの血中有核細胞はこの層に集まるため,ctDNA研究では血漿分画に混入させないよう注意が必要である.
実験医学 2016年4月号 Vol.34 No.6
明かされる“もう1つの臓器”
腸内細菌叢を制御せよ!
宿主との相互作用のメカニズムから便移植の実際、バイオベンチャーの動向まで
腸内細菌叢を制御せよ!