概論
HLAの新展開
New aspects of HLA
荒瀬 尚
Hisashi Arase:Department of Immunochemistry, Research Institute for Microbial Diseases, Osaka University/Laboratory of Immunochemistry, WPI Immunology Frontier Research Center, Osaka University(大阪大学免疫学フロンティア研究センター免疫化学研究室/大阪大学微生物病研究所免疫化学分野)
HLAはペプチドをT細胞に提示することで,免疫応答の中心的な役割を担っている.一方,HLAは非常に多型性に富んだ遺伝子であり,個人差が非常に大きい.HLAの個人差は免疫応答の差を決定する大きな要因であり,感染症に対する抵抗性を大きく左右する一方,自己免疫疾患,アレルギー疾患等の感受性に最も強く影響を与える要因でもある.したがって,HLAがどのように疾患発症に関与するかを解明することは,疾患の発症の原因解明や治療法,予防法の開発に重要であるが,HLAがどのように疾患発症に関与しているかは依然として明らかでない.一方,近年,次世代シークエンサーの進歩等による新たなHLAの解析法の開発やHLAの新たな機能が明らかになり,従来考えられてきたのとは異なる側面が明らかになってきた.本稿では,HLAに関する最近の知見を紹介する.
はじめに
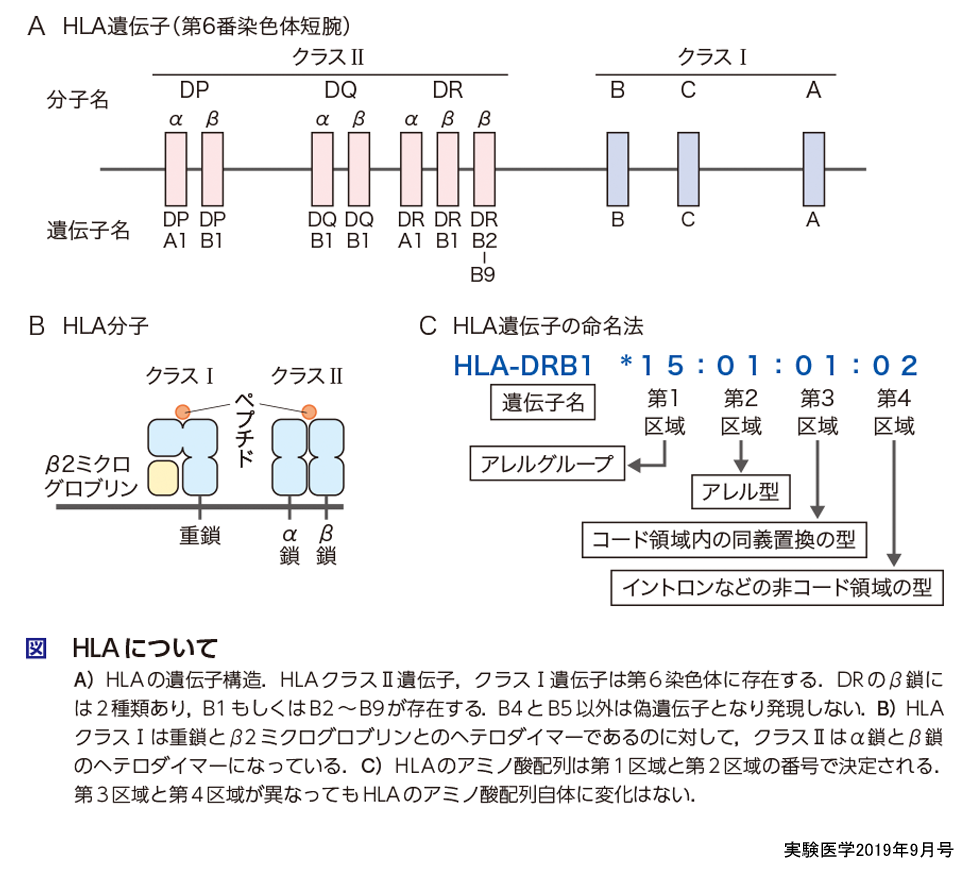
HLAはクラスⅠとクラスⅡからなり,それぞれキラーT細胞,ヘルパーT細胞に抗原を提示することで,T細胞の分化と認識に必須の分子である.HLAクラスⅠは体中のほとんどの細胞に発現が認められる一方,HLAクラスⅡは樹状細胞やB細胞等の一部の細胞のみに認められる.HLAは主要組織適合抗原(major histocompatibility complex,MHC)ともよばれるが,それは,マウスにおける移植の適合性を決定する分子として見出されたことに由来する.その後,ヒトの白血球上の分子として同定されたHLAにMHCと同様な機能があることが判明した.しかし,移植という自然界には存在しない人工的な処置に対して生じた免疫応答であることから,HLAは他人の組織を拒絶するための分子ではない.したがって,MHCというよび方は最も一般的に使われているが,本来の機能を表現しているとは言えない(HLAの基礎知識については本誌2248ページ,コラム「HLAのキホン」を参照).
HLAが多様性を獲得した最も大きな環境要因は,さまざまな致死的な感染症であると考えられる1).つまり,HLAが異なると特定の抗原に対する免疫応答が異なり,感染症に対する抵抗性が変わる.長い人類の歴史のなかで何度も致死的な感染症が流行した結果,特定のHLAをもっている集団のみが生き残るということがくり返されて,現在のHLAの多様性が形成されたと言える.HLAにおける多様性の獲得は移植医療を困難にした一方,個々の感染症に対する抵抗性に差をつけ,感染症による種の絶滅を防ぐことに貢献している.一方,HLA型はがんの抵抗性にも関与するが,一般にがんの発症年齢は生殖年齢よりかなり高いことから,HLAはがんに対する免疫応答を惹起するには最適化されて進化してきた分子ではない.このことが腫瘍に対する免疫応答が十分機能しない原因かもしれない.また,HLAが感染症に抵抗するために獲得した多様性の副作用が,後述のように自己免疫疾患やアレルギーの非常に強い遺伝的背景になってしまっている1).したがって,HLAがどのように免疫疾患の発症に関与しているかを完全に理解することが,自己免疫疾患,アレルギー疾患,がんに対する治療法,予防法を開発するうえで重要である.
1HLAアレルと疾患
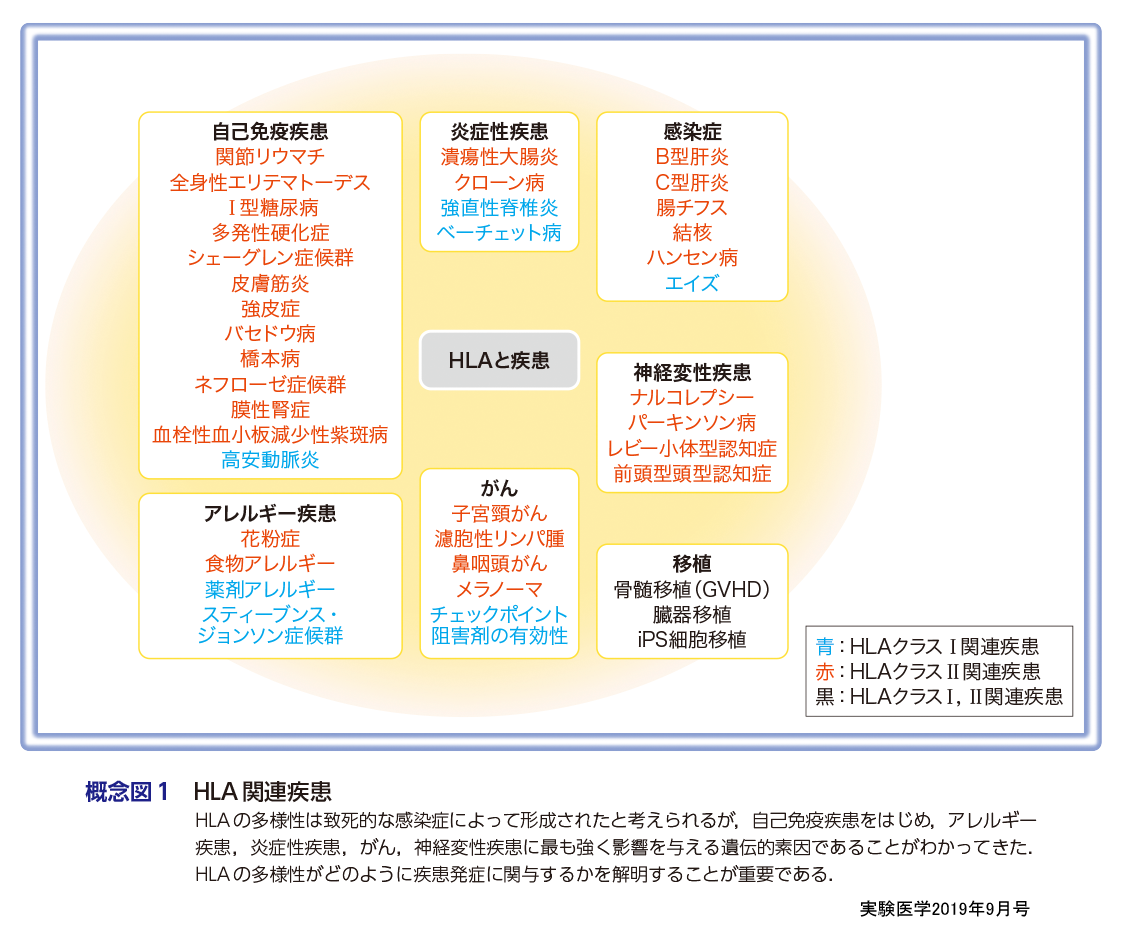
特定のHLAアレルは関節リウマチ等の自己免疫疾患の発症に大きな影響を与える1).一般に典型的な自己抗体の産生が認められる多くの自己免疫疾患では特定のHLAクラスⅡアレルが関与する(概念図1).一方,自己抗体の産生が認められない強直性脊椎炎2),乾癬3),ベーチェット病4)などの疾患ではHLAクラスⅠアレルが関与する.また,食物アレルギー5)や薬剤アレルギー6)も特定のHLAアレルが非常に強く関与する.しかし,疾患感受性と言われるHLAアレルをもっていても,ほとんどの人は疾患を発症することはない.当初は,HLA以外に疾患発症に関与する遺伝子があるのではないかと考えられ,大規模な全ゲノム関連解析がさかんに行われてきた.しかし,HLAより強く疾患発症に関与する遺伝子は見つからないどころか,逆にHLAは他の遺伝子よりも格段に強く疾患発症に関与するということが明らかになった.したがって,特定のHLA型をもっている遺伝的背景にどの様な環境要因が加わることで発症するかを解明することが重要である.特定のHLAアレルの関与が異常に高い疾患としては,ナルコレプシー7)と強直性脊椎炎2)があげられ,それぞれの感受性アレルであるHLA-DQB1*06:02とHLA-B27のオッズ比は100以上にもなる.典型的な自己免疫疾患である関節リウマチ8)やⅠ型糖尿病9)等の自己免疫疾患における特定のHLAクラスⅡアレルのオッズ比が4〜5程度であることと比較すると圧倒的に高い.一方,ナルコレプシーや強直性脊椎炎は,明らかな免疫異常が認められず,これらの疾患が免疫疾患であるかを含めて依然として不明である.また,大規模な全ゲノム関連解析の結果,予想外にもパーキンソン病10),レビー小体型認知症11),前頭側頭型認知症12),急性冠症候群13)においてもHLAクラスⅡアレルが関与しているが明らかになってきている.これらの神経変性疾患や循環器疾患にHLAがどのように関与しているかを解明することも今後の高齢化社会において重要であると思われる.
2新たなHLA解析手法
前述のように特定のHLAアレルは疾患感受性に非常に強く関連している.したがって,正確にHLAの遺伝型を同定することが重要である.古くは特定のHLAアレルに対する抗体を用いて血清学的にHLAアレルを決定していたが,その後,遺伝子レベルでの解析法が開発され現在ではPCR-SSOP(sequence specific oligonucleotide probe)法やSBT(sequence based typing)が主流になっている.HLAのペプチド結合部位の配列が自己免疫疾患の感受性に影響を与えることから,これらのHLAタイピング法はペプチド結合部位を含むエキソン2とエキソン3領域を中心に解析されている.
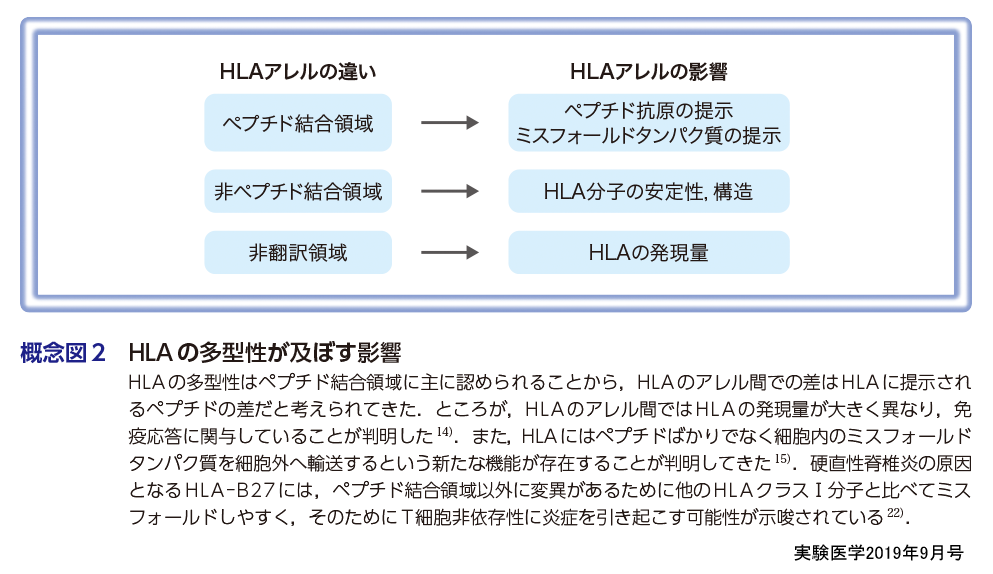
一方,次世代シークエンサーの発展により,HLA遺伝子領域をエキソンばかりでなく,イントロン領域までの全シークエンスを解析できるようになってきた.その結果,ペプチド結合領域の多様性ばかりでなく,イントロン部分の多様性によりHLAの発現量が異なることが明らかになってきた(椎名・細道の稿).さらに,HLAクラスⅡ遺伝子の非翻訳領域も骨髄移植の際のGVHD(移植片対宿主病)に関与していることが判明した(森島らの稿).したがって,HLAの機能を考えるうえでペプチド結合領域の配列ばかりでなく,発現量も重要な要素であると考えられる.実際,エイズの発症にはHLA-Cの発現量が関与することが報告されている14).また,従来までのSNPの解析結果を利用して,HLAハプロタイプを高い確率で予測するインピュテーション法が開発されている(平田・岡田の稿).インピュテーション法により今まで蓄積されてきた遺伝子解析結果を利用してHLAの関連解析をできることから,今後さらに多くの疾患におけるHLAの関与が明らかになると期待される(概念図2).
HLAの基本的な機能は,T細胞へのペプチド抗原の提示である.したがって,疾患発症に関与するペプチドの同定が重要である.従来より,HLAに提示されたペプチドの同定は,HLAを免疫沈降し,それに含まれるペプチドを質量分析にて同定するという手法が用いられている.近年,質量分析機の感度が非常に高くなったが,依然として解析には多くの細胞が必要であるため,HLAに提示されたペプチドの同定は容易ではない.一方,HLAに結合するペプチドの予測については,簡単に利用できるwebサイトがあり,ある程度正確に特定のアレルのHLAに結合するペプチドを予測することが可能である(http://tools.immuneepitope.org/main/tcell/).また,HLAはα鎖とβ鎖からなるが,ペプチドによってヘテロダイマーは安定化する.その性質を利用したHLAとペプチドの結合性の評価は,さまざまなペプチドの親和性を解析するのに有用であることが判明してきた(宮寺の稿).HLAに結合するペプチドの評価はこれらの手法を多角的に利用して解析するのが重要であると思われる.
3HLAによる新たな抗原提示能
HLAはペプチド抗原をT細胞に提示するという基本概念をもとに研究されてきた.したがって,特定のHLAが関与する疾患はT細胞の異常によって引き起こされると考えられてきた.しかし,疾患発症にかかわるペプチド抗原の同定には至っておらず,どのように病原性のT細胞が活性化するかは明らかになっていない.一方,HLAクラスⅡ分子のペプチド結合部位の両側は開いているため,HLAクラスⅡ分子は長いペプチドも提示できる.そのため,通常小胞体内で新たに合成されたHLAクラスⅡ分子にはリソソーム移行シグナルをもったインバリアント鎖のペプチド様の領域(CLIP)が結合し,HLAクラスⅡ分子はリソソームへ輸送される.ところが,小胞体内にインバリアント鎖のCLIP領域より親和性の高いペプチド様の構造をもったミスフォールドタンパク質が存在すると,それらがインバリアント鎖の代わりにHLAクラスⅡ分子に結合してしまい,ミスフォールドタンパク質の結合したHLAクラスⅡ分子は直接細胞表面に輸送されることが判明した(末永・荒瀬の稿).つまり,HLAクラスⅡ分子には細胞内のミスフォールドタンパク質を細胞外へ輸送するというシャペロン様の機能があることが明らかになってきた15).
HLAクラスⅡ分子によって輸送されたミスフォールドタンパク質は自己免疫疾患で産生される多くの自己抗体の標的になっている16).特に,疾患感受性の高いアレルのHLAクラスⅡ分子に結合した自己抗原が標的になっていることから,ミスフォールドタンパク質・HLAクラスⅡ分子複合体の形成が自己免疫疾患の発症とも密接な関連があると考えられる.したがって,HLAクラスⅡ分子の機能を考える場合,ペプチドばかりでなく,タンパク質が提示されているという点も考慮する必要がある.
4自己免疫疾患とがん
多くの自己免疫疾患には標的となる特異的な抗原や組織が存在し,特徴的な自己抗体が産生される疾患が多い.なぜ,自己免疫応答が破綻するのかは,免疫学における長年の謎でもある.特異的な自己抗体の産生機構として,細菌やウイルスに対する交差反応性や,自己抗原に対する免疫寛容の破綻等が考えられている.しかし,関節リウマチでは,リウマトイド因子と抗シトルリン化抗体という少なくとも2種類の特異性の異なる自己抗体の産生が認められるし,バセドウ病ではTSHレセプターに対する自己抗体に加えて,サイロペルオキシダーゼやサイログロブリンといった異なる抗原に対する自己抗体の産生が認められる場合が多い.全身性エリテマトーデスにおいても抗DNA抗体に加えて,ヒストンタンパク質に対する自己抗体が同時に産生される.全く抗原性の異なる複数の自己抗体が一つの自己免疫疾患で産生されることは,交差反応性や特定の自己抗原に対する免疫寛容の破綻では説明できない.一方,バセドウ病の標的組織は甲状腺特異的であり,関節リウマチの標的組織は関節であるというように,疾患によって標的組織はおよそ限定されている.したがって,自己免疫疾患は,特定の組織,細胞に何らかの異常が起こり,それに対する免疫応答が惹起されるていると考えると,多くの自己抗体の産生パターンは説明できるのではないかと思われる.実際,多くの自己免疫疾患の標的組織では,異所性のHLAクラスⅡ分子の発現が認められることから17),HLAクラスⅡ分子によって形成されたミスフォールドタンパク質・HLAクラスⅡ分子複合体が自己免疫応答に関与している可能性も考えられる.今後は,各組織,細胞にどのような異常が起こり,自己免疫応答が惹起されるかを解明することが重要であると思われる.
一方,自己免疫疾患は単なる免疫システムの副作用なのだろうか? 腫瘍細胞は,自己の細胞から発生したものであり,腫瘍細胞の抗原性は正常細胞とほとんど同じである.正常細胞と同様な抗原性をもった腫瘍細胞を攻撃するには,腫瘍細胞に対する特異的な自己免疫応答が必要である可能性がある.自己免疫疾患のひとつ皮膚筋炎の患者では悪性腫瘍を合併することがあるし,逆にメラノーマの患者では自己免疫疾患が関与する白斑が認められることもある.実際,HLAクラスⅡ分子の発現が誘導されているメラノーマの予後がよいという報告もあることから18),HLAクラスⅡ分子の異所性発現によって腫瘍細胞に対する自己免疫応答が誘導されている可能性も考えられる.
腫瘍細胞における遺伝子変異のあるタンパク質は,正常タンパク質とは抗原性の異なるネオ抗原とよばれ,抗腫瘍免疫応答の惹起に重要である.特に,次世代シークエンサーを用いて網羅的に腫瘍細胞における変異抗原を見つけ出し,それぞれの腫瘍細胞に最適な免疫応答を誘導する次世代の方法も提案されている(西村の稿).一方,腫瘍細胞においては,HLAクラスⅠの全欠損19),片アレルの欠落20),抗原提示部位の変異21),さらにはHLAクラスⅡ分子の発現誘導の欠落22)等の免疫逃避機構が認められることから,これらの解除法の開発も重要である.このように,腫瘍免疫においてもHLAの関与が非常に大きいと考えられ,HLAを標的にした効果的ながん免疫誘導法の開発が期待される.
おわりに
HLAは免疫応答で重要な役割を担う一方,免疫疾患から神経変性疾患までさまざまな疾患の遺伝的素因として最も強く影響を与えることが明らかになってきた.したがって,HLAは疾患の原因解明ばかりでなく,治療薬,予防薬の開発のための標的分子として重要であるが,HLAの高い多様性のために依然として不明な点も多く,現状ではHLAを標的とした医薬品の開発は成功していない.本特集では最近の新たなHLAの解析方法の進歩とともに,新たなHLAの機能を紹介する.これらのHLAの新たな知見が今後の自己免疫疾患,アレルギー疾患,がん,臓器移植,感染症,神経変性疾患等に対する新たな創薬に貢献することを期待する.
文献
- Matzaraki V, et al:Genome Biol, 18:76, 2017
- Colbert RA, et al:Mol Immunol, 57:44-51, 2014
- Genetic Analysis of Psoriasis C, et al:Nat Genet, 42:985-990, 2010
- Remmers EF, et al:Nat Genet, 42:698-702, 2010
- Hong X, et al:Nat Commun, 6:6304, 2015
- Ozeki T, et al:Hum Mol Genet, 20:1034-1041, 2011
- Hor H, et al:Nat Genet, 42:786-789, 2010
- Eyre S, et al:Nat Genet, 44:1336-1340, 2012
- Bjørnvold M, et al:Diabetologia, 51:589-596, 2008
- Hamza TH, et al:Nat Genet, 42:781-785, 2010
- Peuralinna T, et al:Ann Clin Transl Neurol, 2:920-931, 2015
- Ferrari R, et al:Lancet Neurol, 13:686-699, 2014
- Sinisalo J, et al:Circ Cardiovasc Genet, 9:55-63, 2016
- Apps R, et al:Science, 340:87-91, 2013
- Arase N & Arase H:J Biochem, 158:367-372, 2015
- Jin H, et al:Proc Natl Acad Sci U S A, 111:3787-3792, 2014
- Hanafusa T, et al:Lancet, 2:1111-1115, 1983
- Chen YY, et al:Diagnostics (Basel), 9:doi:10.3390/diagnostics9020059, 2019
- Rodríguez JA:Oncol Lett, 14:4415-4427, 2017
- McGranahan N, et al:Cell, 171:1259-1271.e11, 2017
- Shukla SA, et al:Nat Biotechnol, 33:1152-1158, 2015
- Satoh A, et al:Oncogene, 23:8876-8886, 2004
著者プロフィール
荒瀬 尚:1990年北海道大学医学部卒業後,同大学院医学博士課程(小野江和則教授)にてNKT細胞の研究に従事.’94年より千葉大学医学部高次機能制御研究センター遺伝子情報分野(斉藤隆教授)助手,2000年よりカリフォルニア大学サンフランシスコ校にてNK細胞のウイルス感染細胞認識機構の研究に従事.’02年より千葉大学大学院医学研究院遺伝子制御学助教授,’04年大阪大学微生物病研究所免疫化学分野助教授を経て,’06年より同教授,’07年より大阪大学免疫学フロンティア研究センター免疫化学研究室教授を兼任し,’19年より同副拠点長.宿主病原体相互作用の研究からHLAクラスⅡ分子の新たな機能を見出した.今後は疾患発症機構の解明による疾患の新たな治療法,予防法の開発をめざしている.
 HLAのキホン
HLAのキホン