- [SHARE]
- ツイート


第2回 変性ポリアクリルアミドゲル電気泳動(Ⅰ)
前回のエタノール沈殿と同様に頻繁に行われる操作が,変性ポリアクリルアミドゲルを用いた核酸断片の電気泳動であろう.最近はレディメイドのゲルも市販されるようになったが,実験に適した電気泳動を行うには,各研究者が最適なゲルを作製することも重要である.そこで本稿から数回に分けてポリアクリルアミドゲル電気泳動について,その原理などを解説したい.今回は変性ポリアクリルアミドゲルの作製法である.
核酸断片の電気泳動の原理
鎖長の違いによる複数の核酸断片の分離や解析に最も適した手法がゲル電気泳動である.核酸は,中性条件でそのリン酸部分が解離しているので,水溶液中で負の電荷を有する.そこで,網目構造を有するゲル状のポリマー中に核酸断片を入れて,このゲルに電流を流すと,核酸断片が陽極側に移動する.この時,短い核酸断片ほどゲルの網目構造中を早く移動するので(分子ふるい効果),長さの違いにより核酸断片を分離することができる.また核酸断片の高次構造の違いも泳動の移動度に影響するので,鎖長に依存した電気泳動を行う場合には,変性剤をゲルに加えたり,高温下で泳動を行ったりする.
電気泳動に用いるゲルには,ポリアクリルアミドやアガロースが通常用いられる.またゲルに添加する変性剤としては,尿素やホルムアミドなどがある.本稿では最も一般的な,尿素を用いた変性ポリアクリルアミドゲルの電気泳動について解説したい.
電気泳動でカギとなるのは,ゲルの作製である.何の目的で電気泳動を行うのか,例えば目的とする核酸断片を大量に精製したいのか,あるいは鎖長の異なる複数の核酸断片を解析したいのかなどにより,準備するゲルも異なってくる.これは実験の目的に応じてゲルの組成を変えられるというゲル電気泳動法の長所でもある.
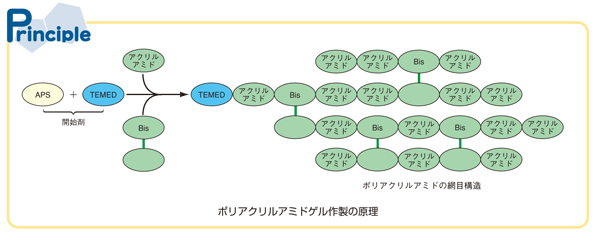
ポリアクリルアミドのゲルは,ラジカル連鎖重合という化学反応によって作られる.その反応の詳細に関しては次回に解説するが,過硫酸アンモニウム(APS)とN,N,N´,N´- テトラメチルエチレンジアミン(TEMED)による開始剤がアクリルアミドと反応し,さらに連鎖的にアクリルアミドが順次反応することによりポリマーとなる.アクリルアミドだけでは直鎖状のポリマーになってしまうが,二価性架橋剤のN,N´- メチレンビスアクリルアミド(Bis)(2つのアクリルアミド分子がメチレンを介して連結した分子)を反応中に加えることにより,枝分かれした三次元構造のポリマーになる(Principle).
核酸断片の移動速度の違いは,障害物となるこのゲルの架橋構造中の網目の大きさに起因する.網目の大きさ(ポアサイズ)は,重合に用いるアクリルアミドの濃度〔% T =(アクリルアミド+ Bis)× 100(w/v): Total %の略〕と架橋剤Bis の混合比〔% C =Bis × 100/(アクリルアミド+ Bis):Cross-linker %の略〕によって調節できる.一般的に2本鎖DNAの電気泳動では,% C = 3.33(アクリルアミド: Bis = 29 :1)にして,100 ~500bp では% T =5,50 ~ 300bp では% T = 10,40 ~ 200bp では% T =12,25 ~ 150bp では% T = 15 を用いる.もちろんこの場合には変性剤は加えない.1本鎖DNAやRNAの電気泳動では,% C =5(アクリルアミド:Bis = 19 :1)にして,45 ~ 120-merでは% T = 10,25 ~ 50-mer では%T = 15,30-mer 以下では% T = 20 を用い,核酸の高次構造を変性させるために7 M 尿素を加える.
変性ポリアクリルアミドゲルの作製方法
一般的な手法をベースにしたわれわれの研究室のゲルの作製方法をProtocol に示した.まず,% C =5の40 %アクリルアミド溶液(アクリルアミド: Bis = 19 :1)と10 × TBE(もしくは5× TBE)のストック溶液を作製する.40 %アクリルアミド溶液は冷蔵庫で保存する.特定の濃度(%T = 20,15,10)のゲルを多用する場合は,尿素(最終濃度7 M)を混合したそれぞれの% T のストック溶液を調製しておけばよい.これは冷蔵庫で1カ月程度保管できる.このストック溶液を使用する直前に0.22 ~ 0.45μm のフィルターで吸引濾過することにより,わずかに混在する固形物を除くと共に脱気を行う.脱気を行わないと,酸素がラジカル重合反応を阻害し,またゲルに気泡ができやすくなってしまう.
必要量のアクリルアミド溶液にAPSを加え,次いでTEMEDを加えて気泡が入らないようにかき混ぜる.室温が20 ℃以下になると反応が起こりにくくなるので,APSとTEMEDの量を増やす研究者がいるが,これはやめたほうがよい.次回に説明するが,TEMEDの量を増やすことによりポリアクリルアミドポリマーの長さが短くなる可能性がある.これは些細なことかもしれないが,このレベルのことを気にしないと長い実験の工程を経て出てきた結果の再現性を高めることはできないし,またなぜ再現性が出ないかにも気付きにくくなってしまう.
APSとTEMEDを加えた溶液は,すぐにゲル板に流し込む.気泡が入らないように連続してアクリルアミド溶液を流し込むのがコツである.気泡が入ってしまった場合に,ゲル板を軽くたたくことにより振動を与えて気泡を上方に逃がすことをするが,これはあまりお勧めしない.この操作により下の方から別の気泡が上がってくることがよくある.ゲルに気泡を入れないためには,ガラス板やスペーサーの油分などの汚れを除いておくことも重要である.最後にコームを差し込み,サランラップでコーム部分を覆い,できるだけゲル溶液が空気に触れないようにする.われわれの研究室では,分析用の場合にはゲルが固まり次第使用するが,電気泳動後に核酸断片をゲルから回収する場合には,ゲルを一晩放置させてアクリルアミドのラジカル重合反応をできるだけ完結させてから使用するようにしている.これはゲルからの核酸断片の回収の際に短いアクリルアミド重合物を混入させないためである.
実験例
核酸断片の鎖長によりゲルの濃度(% T)を変えて電気泳動を行うが,アクリルアミドとBisの割合(% C)を敢えて変えることはほとんど無いのではないだろうか. そこで, 本稿では,% C を変えると泳動がどのように変化するかを調べてみた.5´末端を32Pで標識した119-mer のRNA断片をアルカリとRNase T1(塩基配列中のG の3´側でRNAを切断する)のそれぞれで限定分解した後,これを電気泳動して種々の鎖長のバンドのラダーパターンを解析した.実験は,% T =6と10 のそれぞれで,% C を3.3,5,6.7 に変えたゲルを用いて,35 ワット,45 ℃で1.5 時間泳動して行った(Result).
一般的に120-mer 以下の鎖長の核酸はT %= 10 よりも濃いゲルを用いるが,本実験においても確かに% T =6よりも% T = 10 のゲルのほうがラダーの分離能がよかった.それでも,Bis の割合を多くすることにより,% C = 6.7では% T =6の場合も分離能がよくなることがわかった.特に50-mer より長い断片の分離が良くなっている.%C を小さくすると核酸断片は全体的に早く流れるようになるが,% T = 10 の場合には% C が3.3 ~ 6.7 の間ではラダーの分離能はそれほど変わらない.ということは% T = 10,% C = 3.3 のゲルを用いることにより,ラダーの分離能を下げることなく,% T = 10,%C = 6.7 のゲルよりも泳動時間を短縮することができそうである.
% T や% C を色々変えてポリアクリルアミドゲルのポアサイズを透過型電子顕微鏡で解析した報告があるが(Ruchel, R. J. et al.: J. Chromatogr.,166 : 563, 1978),それによると% T =10 では% C = 5 のときに網目構造のポアサイズが極小になるとある.また,2本鎖核酸断片の相対移動度からポアサイズを推定した報告でも(Holmes, D.L. & Stellwagen, N. C.: Electrophoresis,12 : 612, 1991),% T が一定(3.5 ~10.5)であれば,% C = 5 と% C = 10のポアサイズはほとんど変わらず最小となることを示している.しかし今回のわれわれの変性ゲルの結果では,%T = 6 であっても% T = 10 であっても,% C = 6.7 のほうが% C = 5 よりもRNA断片の泳動が遅くなったことから,この範囲の% C ではポアサイズも変化していると考えられる.
電気泳動のマーカーには,キシレンシアノール(XC)とブロモフェノールブルー(BPB)がよく用いられる.BPB の移動度は,% T に依存しているが% C にはそれほど影響せず,% T =6ではRNA断片の22 ~ 23-mer の位置を示し,% T = 10 では12 ~ 14-mer の位置を示す.XC は% T と% C の違いにより不規則に移動度が変わるので注意が必要だ.Result の泳動では,XCは, % T = 6 , % C = 3 . 3 で110-mer,% T =,% C = 6.7 で90-mer,% T = 10,% C = 3.3 で64-mer,% T = 10,% C = 6.7 で48-mer のRNA断片に相当する位置にそれぞれ泳動された.
まとめ
今回はポリアクリルアミドゲルの作製について,アクリルアミドとBis の量を変えて,その影響を1本鎖RNAのラダーを用いて調べた.% C の違いによるRNA断片の分離能への影響は微妙だが,% T が高い場合には% C の違いによりRNAの移動度にかなり差が出てくるので,分析したい核酸断片の鎖長に依存して% T と% C を決めてゲルを作製すれば,泳動時間の予測も確実になる.2本鎖DNAの実験例は,「電気泳動なるほどQ&A」60 ~ 62 ページ(羊土社)などを参照していただきたい.
- ※この連載はバイオテクノロジージャーナル 2007年11,12月号に掲載されたものです
Profile
- 木本 路子(Michiko Kimoto)
- 理化学研究所生命分子システム基盤研究領域
- 原田 洋子(Yoko Harada)
- 理化学研究所生命分子システム基盤研究領域
- 平尾 一郎(Ichiro Hirao)
- 理化学研究所生命分子システム基盤研究領域/タグシクス・バイオ株式会社