- [SHARE]
- ツイート


第5回 ポリアクリルアミドゲルからの核酸断片の溶出
ポリアクリルアミドゲル電気泳動後のゲルからの核酸断片の回収は,研究室によってその手法の詳細はかなり異なるのではないだろうか.今回は最も簡単な回収方法である,ゲル片を水溶液に浸してDNAを溶出する手法について解説する.
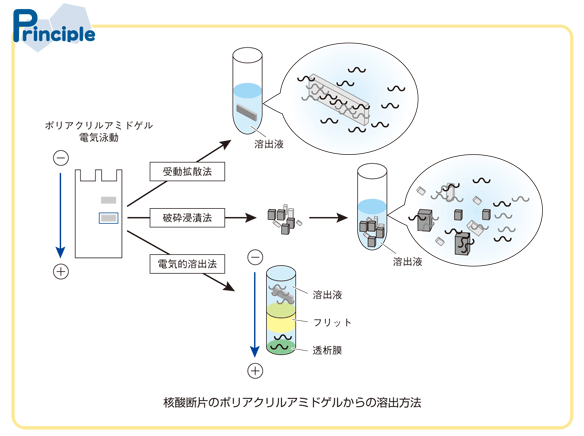
ポリアクリルアミドゲルからの核酸断片の溶出方法
電気泳動後にポリアクリルアミドのゲル片から核酸断片を溶出して回収する方法には,受動拡散法(passivediffusion),破砕浸漬法(crush and soak),電気的溶出法(electroelution)等がある(Principle).受動拡散法は切り出したゲル片をそのまま溶出液に浸し,破砕浸漬法ではゲル片を細かく粉砕してこれを溶出液に浸す.両手法とも,自然拡散により核酸断片を溶液中に溶出させる方法である.したがって溶出効率は,核酸断片の鎖長,ゲル濃度,処理スケールや温度や溶出時間,切り出したゲル片の大きさ等によって変わる.短い核酸断片ほどゲルの網目構造を通りやすくなり短時間で溶出される.また,切り出したゲル片を粉砕する破砕浸漬法は,受動拡散法と比べて溶出効率が向上する.これは,粉砕により溶液と接するゲルの表面積が増すためである.この破砕浸漬法では,ゲル片をスライドガラス上で1~2 mm程度に切り刻んだり,あるいはチューブの壁にスパーテルなどでゲル片を押し付けたりしてすり潰す. 一方, 電気的溶出法は,ゲル片を透析バッグ(チューブ)などに入れて緩衝液中で泳動することにより,ゲルから核酸が溶出される.この手法の装置も市販され,受動拡散法と比べて短時間で回収できる.しかし電気的溶出法は,装置が必要なことと処理の煩雑さという点で,手軽にできる手法ではない.そこで本稿では,簡便な受動拡散法と破砕浸漬法について解説する.
「モレキュラークローニング」(Sambrook, J., Russell,D.W.: Molecular Cloning A Laboratory Manual,3rd Edition, Cold Spring Harbor Laboratory Press.Cold Spring harbor, New York, 2001)に記載されている破砕浸漬法では,その溶出液の組成に,0.5 M 酢酸アンモニウム,0.01 M 酢酸マグネシウム,0.1 % SDS(オプショナル),1 mM EDTA(原著には0.1 mM との記載もある) を用いている. ちなみに, 本書では,Maxam とGilbert によるDNAシーケンシングの論文がDNA断片のゲルからの溶出法として引用されている(Maxam, A. M. & Gilbert, M.: Proc. Natl. Acad.Sci. USA, 74: 560, 1977/ Methods Enzymol. 65: 499,1980).原著には,酢酸アンモニウムは,核酸断片のゲルからの溶出を促進すると書かれている.またSDSやEDTAは,微量のタンパク質成分(核酸分解酵素等)が混在した場合にこれを失活させるため,そしてマグネシウムイオンは溶出した核酸断片のエタノール沈澱を促進するために用いると記載されている.
しかしこの組成の溶出液を用いて溶出した核酸断片をエタノール沈殿により回収する場合には注意を要する.たとえば,回収後の核酸断片を酵素反応に用いる際は,SDSの混在に注意し,場合によってはフェノール・クロロホルム処理でSDSを除去する必要もある.また,アンモニウムイオンはリン酸化反応で用いるT4ポリヌクレオチドキナーゼを阻害するので, 用途によっては酢酸アンモニウムの使用を避けたほうがよい.さらに, 本書のように酢酸マグネシウムとEDTAを組合わせた緩衝液はよくみかけるが,2価の金属イオンとEDTAの組合わせには疑問を感じる. 溶出液に関してはまだまだ検討の余地がありそうだ.
核酸断片のポリアクリルアミドゲルからの回収方法
核酸断片のゲルからの回収は,①核酸断片のゲルからの切り出し,②ゲル片からの核酸断片の溶出,③溶出液中の核酸断片のエタノール沈殿からなる(Protocol).以下にわれわれの研究室で行っている手法を解説する.全操作を通して核酸分解酵素の混入には十分に注意する.使用する器具(剃刀の刃,ピンセット,スパーテル)は,あらかじめエタノールで濯ぎ,ライターの火であぶっておく(エタノールの引火に注意).本稿では,未標識の核酸断片のゲルからの切り出しについて述べる.
- ① 回収用のポリアクリルアミドゲルの作製では,未反応のアクリルアミドの混入をできるだけ減らすために,一晩程度かけてゲルを固める.電気泳動後,ゲル板の水分をよく拭き取り,上面のガラス板を外してゲルの上面をサランラップで覆い,ガラス板を反転させる.スパーテルでガラス板からゲルを隅からはがしていき,サランラップ上に移す.ゲルとサランラップの間に気泡があるとバンドがみえづらいので注意する.ゲルを蛍光指示薬入りのTLCプレート(Merck 60 F254 など)に乗せ,ハンディUV ランプ(254 nm)を用いて核酸断片のバンドを検出する(UVシャドウイング).検出限界は,ゲルの厚さやバンドの幅にもよるがおよそ1 μg 前後である.バンド部分を剃刀の刃を用いて切り出す(刃を垂直にゲルに押し付けて切るとよい). 切り出したゲルの断片が少量の場合には1.5 mL マイクロチューブに,大量の場合には50 mL チューブにピンセットを用いて移す.
- ② 受動拡散法では溶出液をそのまま加え,破砕浸漬法ではスパーテルでゲル片をチューブの壁に押さえ付けて潰し,これに溶出液を加えてスパーテルに付着したゲル片を注ぎ落とす. 恒温振盪機を用いて,37 ℃で3~12時間( 核酸断片の鎖長と溶出法によって異なる), チューブを振盪させて核酸断片を溶出する. 溶出液をマイクロピペットで吸い取り,遠心式フィルター(ミリポア社製のウルトラフリーMC など)で溶液を遠心濾過することにより混入した微細のゲル片を取り除く.
- ③ この溶出液に, 1/10 倍量の3 M 酢酸ナトリウム(pH 5.2)と2倍量のエタノールを加えて(オプショナルでグリコーゲンを加えることもある),- 20 ℃で1時間放置後,13,000 rpm で30分遠心して核酸断片を回収する(エタノール沈殿については,バイオテクノロジージャーナル2007 年9-10月号を参照).
実験例
受動拡散法や破砕浸漬法のプロトコールを種々参照すると,溶出時間は37 ℃で3~4時間ないしは12 から16 時間,または65 ℃で1時間から4時間とまちまちである.そこで,これらの2つの方法について,2種類のDNA断片(43塩基と85塩基)を用いて,溶出液の種類〔0.3 M 酢酸ナトリウム,TE緩衝液,滅菌水,ならびに,「モレキュラークローニング」に記載の溶出液(0.5 M 酢酸アンモニウム,0.01 M 酢酸マグネシウム,1 mM EDTA),本稿ではこれを標準溶出液とよぶことにする〕や溶出時間(1~24時間)を変えてDNA断片の回収率を調べることにした.
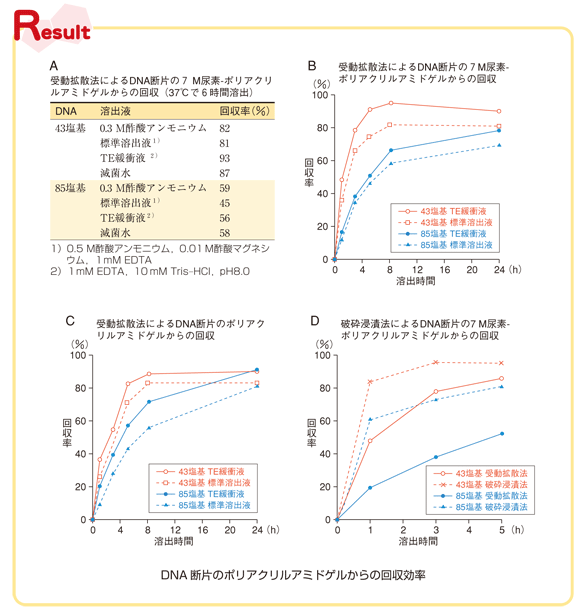
0.5 OD260nm 量のそれぞれのDNA断片( 43塩基は1057 pmol,85塩基は556 pmol)を,7 M 尿素を含む10 %のポリアクリルアミドゲル,あるいは尿素を含まないゲルで電気泳動し, 断片のバンドを切り出して,受動拡散法と破砕浸漬法のそれぞれで0.45 mL の溶出液を用いて37 ℃で溶出した. ゲル片の大きさは9×2~3 mm,ゲルの厚さは1 mm である.エタノール沈殿後に回収したDNA断片をUV 測定用の緩衝液〔100 mM NaCl,10 mM リン酸ナトリウム(pH 7.0),0.1 mM EDTA〕に溶かして,260 nm でのOD量を測定することにより, それぞれの条件におけるDNA断片の回収率を求めた(Result).
最初に7 M 尿素を含むポリアクリルアミドゲルからのDNA断片(43塩基と85塩基)の溶出を4種類の溶出液を用いて受動拡散法(37 ℃で6時間の溶出)で行い,その回収率を調べた(Result A).その結果,TE緩衝液の溶出効率が比較的高く43塩基では93 %に達した. しかし鎖長が長くなると回収率は低下し,85塩基では56 %程度であった. また滅菌水のみでも回収率は,他の溶出液と大差なかった.
次いで,TE緩衝液と標準溶出液を用いて,回収率の経時変化を調べた(Result B).やはりTE緩衝液の方が標準溶出液よりも回収率が高い傾向にある.43塩基の場合に,TE緩衝液では5時間で90 %以上が回収されているが, 標準溶出液では8時間の溶出で80 %程度であった. TE緩衝液で24 時間溶出すると48塩基の回収率がわずかに低くなる傾向が示された.この理由はわからないが,溶出時のチューブへのDNA断片の吸着などが考えられる.85塩基の回収率が24時間後でも80 %程度であるのは, 変性ゲル電気泳動中にDNA断片が一部拡散した可能性もあり,切り出したゲル片に全DNAが含まれていなかったかもしれない(85塩基と45塩基ともに同じ泳動距離にしているので85塩基の方が泳動時間が長くなり, 泳動中に拡散した可能性がある).
また7 M 尿素を含まないポリアクリルアミドゲルからの場合も7 M 尿素を含むゲルからの場合と比較してDNA断片の溶出効率はほとんど変わらないが,回収率はTE緩衝液を用いて24 時間溶出を行った場合には90 %に達している(Result C).
次にTE緩衝液を用いて破砕浸漬法での回収率を調べた(Result D).この手法は非常に効果的で,43塩基では3時間程度で回収率が90 %を超え,85塩基でも5時間で80 %に達した.
以上の結果をまとめると,TE緩衝液を溶出液に用いた破砕浸漬法がお勧めである.本手法で,40塩基程度のDNAであれば3時間で90 %以上の,また80塩基程度のDNAであっても80 %程度の回収率に達する.
まとめ
実はわれわれの研究室では,これまで溶出液に滅菌水を用いていた.ゲルからの核酸断片の溶出では恒温下で長時間振盪するため,核酸分解酵素の混在が最も気になる.この点から溶出液もできるだけシンプルなものの方が安全であるため,われわれは滅菌水を用いている.Result Aの結果からも滅菌水は溶出液として悪くない.しかし今回の執筆にあたり,やはり核酸を扱うのであれば緩衝液にしないとまずいのではないだろうかということで,TE緩衝液を実験に加えた次第である.しかしこれがなかなかよい結果を示した.核酸分解酵素のなかには2価の金属イオンで活性化されるものがあり,またリボザイムのようにマグネシウムイオンなどが活性に関与する核酸断片もあるので,TE緩衝液のようにEDTAを含む溶出溶液の方が安心である.ただし,核酸分解酵素の混入の可能性を考えると,調製の手間を取らない滅菌水も溶出液としては依然魅力的である.今回の結果を踏まえてわれわれの研究室では,今後,核酸断片の用途に合わせてゲルからの溶出にTE緩衝液あるいは滅菌水を用いようと思う.
- ※この連載は実験医学 2008年6月号に掲載されたものです
Profile
- 原田 洋子(Yoko Harada)
- 理化学研究所生命分子システム基盤研究領域
- 木本 路子(Michiko Kimoto)
- 理化学研究所生命分子システム基盤研究領域
- 平尾 一郎(Ichiro Hirao)
- 理化学研究所生命分子システム基盤研究領域/タグシクス・バイオ株式会社