- [SHARE]
- ツイート


第4回 電気泳動における変性剤としての尿素の役割
核酸の変性ポリアクリルアミドゲル電気泳動では,変性剤として尿素やホルムアミドを一般的に用いる.核酸の高次構造にこれらの変性剤はどのように働くのだろうか? 今回はその原理を考察し,二本鎖DNAの構造が尿素やホルムアミドの共存下でどの程度不安定になるかを実際に調べた.
変性剤による核酸高次構造の変性の原理
核酸などの生体分子の高次構造を不安定化させる化学物質は,カオトロピック薬剤(chaotropic agent またはchaotrope)とよばれる.カオトロピック薬剤により二本鎖DNAの熱安定性が減少することは,1962年にHamaguchi とGeiduschek により報告された(Hamaguchi, K. & Geiduschek, E. P.: J. Am. Chem.Soc., 84 : 1329, 1962).この論文ではカオトロピック薬剤としてヨウ化物イオンや過塩素酸イオンなどのアニオンが用いられているが,これらの物質は疎水性化合物の溶解度を上げる塩溶効果(salting-in effect)や水溶液中の水分子の集合体の構造を壊す性質をもっている.尿素やホルムアミドもその特質を有しているので,カオトロピック薬剤に分類することができる.
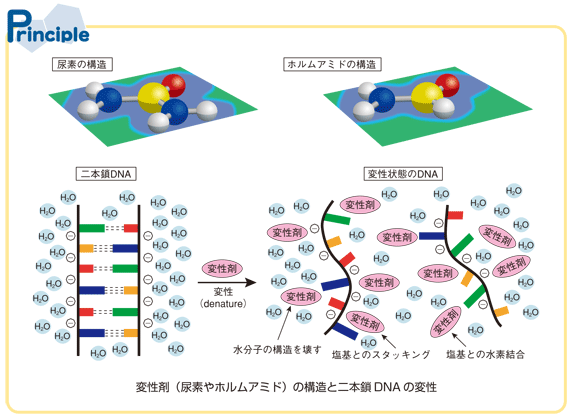
尿素(NH2-CO-NH2)やホルムアミド(NH2-CHO)はどちらも分子内にアミノ基とカルボニル基を有し,すべての原子が同一平面上に位置する(Principle).この平面性はカルボニル基と窒素原子間のアミド結合の共鳴による二重結合性に由来する.この平面構造の上下に広がる電子の共役系が疎水性を示し,さらにアミノ基はプロトン供与体として,またカルボニル基の酸素原子はプロトン受容体として,それぞれ水素結合性残基の特性である親水性を示す.この疎水性部分と親水性部分による両親媒性が核酸やタンパク質の変性剤としての重要な性質である.
DNAの二本鎖構造は,親水性の置換基や原子(リン酸基,糖部分の環内酸素原子・水酸基,塩基部分の窒素原子・イミノ基・ケト基)が水溶液中の水分子や金属イオンと溶媒和している.そして上下に隣接する塩基同士は, 互いのπ電子による疎水性の相互作用(スタッキング: stacking)により,また相補鎖間での塩基対は水素結合により安定化されている.しかし水分子が塩基対内の水素結合に割り込むことがあり,DNAの二本鎖構造は部分的に開いたり閉じたりしている(ブリージング: breathing)と考えられている.
このDNAの水溶液に尿素やホルムアミドなどの変性剤を加えると,DNAに溶媒和した水分子の集合体の構造を壊し,ブリージングに乗じて変性剤がスタッキングした塩基の間に入り込んだり,あるいは塩基対間の水素結合中に割り込んだりして,二本鎖構造を不安定化させると考えられている(Principle).ただし尿素などによる変性作用については正確にはわかっていない部分もある.
変性剤を加えた核酸の水溶液をさらに加熱(70 ~90 ℃)することにより,長鎖の二本鎖DNAや複雑な高次構造によって安定化されたDNAやRNAも効果的に変性させることができる.それでは,尿素やホルムアミドはどのくらいの濃度でDNAの二本鎖構造を不安定化させるのだろうか. そこで98塩基の二本鎖DNAを用いて,尿素(3 M, 7 M)あるいはホルアミド(20 %)共存下での二本鎖DNAの熱安定性を調べることにした.二本鎖DNAは塩基間でスタッキング相互作用が形成されるとUV 吸光度(260 nm)が小さくなる(淡色効果, ハイポクロミシティー:hypochromicity).逆に二本鎖DNAを変性するとスタッキング相互作用が弱くなるのでUV 吸光度が増す(濃色効果, ハイパークロミシティー: hyper -chromicity).この性質を利用して,二本鎖DNAの水溶液のUV 吸光度の温度依存性を調べることにより,種々の環境下での二本鎖DNAの熱安定性を調べることができる.ここで得られるUV 吸光度の変化は,温度に依存してシグモイド曲線となる.その曲線の変極点をTm値(融解温度: melting temperature)とよび,特定の条件下における固有のDNA高次構造の熱安定性の指標となっている.今回はそれぞれの変性剤共存下における二本鎖DNAのTm値を測定することにより,変性剤の効果を調べた.
電気泳動用のローディングバッファーの調製法
核酸試料を変性アクリルアミドゲルで電気泳動する際には,その核酸の水溶液に変性剤を加えて,DNAやRNAの高次構造をあらかじめ変性させておく. われわれの研究室では,核酸断片の溶液に等容量の10 M尿素溶液を加え, これを加熱した後に7 M 尿素―ポリアクリルアミドゲルにロードする方法(Protocol)を用いている.
10 M 尿素溶液は,30 g の尿素と泳動用の色素(キシレンシアノールやブロモフェノールブルー)各50 mgを1 × TBEに溶かして全量を50 mL にメスアップし,この溶液をフィルター(ミリポア社,マイレクスHA33)に通した後,1 mL ずつエッペンドルフチューブに分注して冷凍庫で保管する.使用する前に析出した尿素を溶かすために加熱するが,加熱をくり返すと尿素が一部分解するので,頻繁に使用する場合は使う量に応じて室温下で保存したほうがよい.
DNA溶液に等容量の10 M 尿素溶液を加え,よく攪拌した後,75 ~ 90 ℃で1~3分間加熱し,この溶液を冷却せずにそのままゲルにロードする.変性ゲル電気泳動の場合,泳動中はゲルの温度を45 ~ 50 ℃に保つ.高温下で泳動することにより変性効果を高められるが, 通常の軟質ガラスのゲル板では70 ℃ぐらいになるとガラス板にひびが入るので注意する必要がある.パイレックス製のガラス板を用いると70 ℃の高温でも耐えられる.非常に安定な高次構造を形成する核酸断片( 後述) を変性させるには, 70 ℃の高温下での泳動が効果的である(Hirao, I. et. al.: Nucleic AcidsRes., 20 : 3891, 1992).
ホルムアミドもローディング溶液に用いられるが,脱イオン化操作が必要であり,またホルミアミドの劣化により沈殿物が生じたりするので,われわれの研究室では通常,尿素溶液を用いている.
実験例
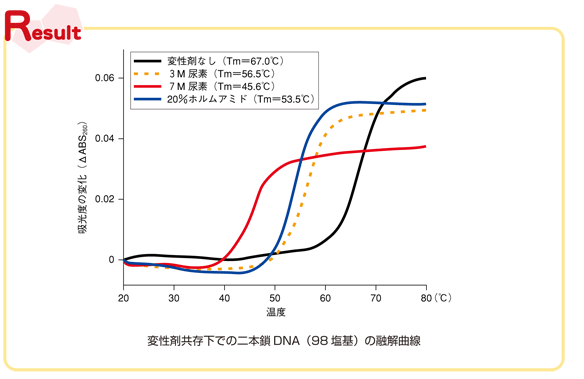
本実験では,0.2 μM の二本鎖DNA(98塩基)を3 M 尿素,7 M 尿素,もしくは20 %ホルムアミドを含む1× TBE溶液に溶かし,20 ℃から80 ℃まで温度を変化させて260 nm の吸光度を測定した.DNAを含まないそれぞれの水溶液で吸光度を補正し,得られたシグモイド曲線を一次微分してT m 値を算出した(Result).
その結果, 変性剤非共存下では, 98塩基の二本鎖DNAの1× TBE溶液中でのTm値は67 ℃,3 M 尿素共存下ではTm = 5 6 . 5 ℃, 7 M 尿素共存下ではTm = 45.6 ℃, 20 %ホルムアミド共存下ではTm =53.5 ℃となった. したがって, 7 M 尿素の添加は,DNAの高次構造の安定性を20 ℃ほど不安定化させ,また20 %ホルムアミドは3 M 尿素の添加と同程度の効果を示すことがわかった.20 %ホルムアミドは約5M溶液に相当するので,等モル数で比べるとホルムアミドよりも尿素のほうが変性剤としての効果が高いようだ. 7 M 尿素の存在下では50 ℃以上で98塩基のDNAが完全に変性されている.
ここで重要なことは, たとえ7 M 尿素共存下でも35 ℃以下では98塩基の二本鎖DNAはほとんど変性していないということである.つまり7 M 尿素の変性ゲル電気泳動を効果的に行うためには,泳動中のゲルの温度をTm値以上にする必要がある.
さらに注意点として,DNAの配列によっては異常に安定な構造を形成するものがあり, 45 ~ 50 ℃での変性ゲル電気泳動でもその高次構造が変性されず,その断片の移動度が早くなったり,遅くなったりすることがある. われわれは以前に, G C G A A A G C ,CCGAAAGG,GCGNAGC(N = A, G, C あるいはT)などの短い配列が両端の2つのG ― C塩基対とその内側のG ― A塩基対により異常に安定なヘアピン構造(ミニヘアピンと名付けられている)を形成することを見つけている(Hirao, I. et. al.: Nucleic Acids Res.,17 : 2223, 1989 / 22 : 576, 1994 / Yoshizawa, S.et al.: Biochemistry, 36 : 4761, 1997).例えばGCGAAAGCT の配列のDNA断片は,そのTm値が80 ℃以上であり,7 M 尿素共存下でもTm値は57 ℃である.したがって通常の変性ゲル電気泳動では,このDNA断片はコンパクトなミニヘアピン構造が変性されず,1~2塩基分だけ早い位置に泳動されてしまう. またG とC のみからなる10塩基ぐらいの二本鎖DNA断片の中には,7 M 尿素共存下の電気泳動で完全に変性されないものもあり,二本鎖DNA由来のバンドが認められることもある.
まとめ
今回の実験で示したように,尿素やホルムアミドなどの変性剤は,DNAの高次構造をTm値で10 ~ 20 ℃ほど不安定化させるだけで,完璧にDNAの構造を変性させるわけではない.したがって効果的な変性ゲル電気泳動を行うためには泳動中の温度コントロールが重要である.しかし注意深く泳動を観察すると,おかしな移動度を示す核酸断片が意外に多いことに気付かれるだろう.それらの配列のなかにはまだ知られていない新しい核酸の構造が潜んでいるかもしれない.
- ※この連載は実験医学 2008年4月号に掲載されたものです
Profile
- 木本 路子(Michiko Kimoto)
- 理化学研究所生命分子システム基盤研究領域
- 平尾 一郎(Ichiro Hirao)
- 理化学研究所生命分子システム基盤研究領域/タグシクス・バイオ株式会社